Relevanz von Hautschutzmaßnahmen bei Beschäftigten in Pflegeberufen
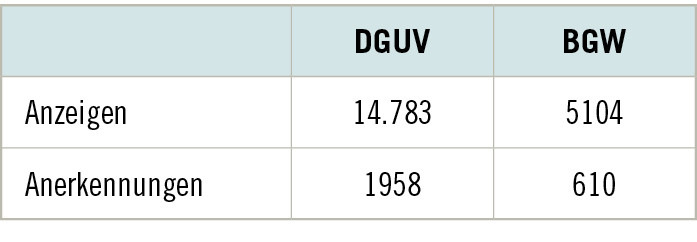
Die Berufsgenossenschaft für Gesundheitsdienst und Wohlfahrtspflege (BGW) verzeichnete im Jahr 2018 6652 Verdachtsfälle berufsbedingter Hauterkrankungen bei Beschäftigten im Gesundheitswesen (BGW 2019). Vor Beginn der SARS-CoV-2-Pandemie wird in Studien beispielsweise von einer Punktprävalenz des Handekzems von etwa 20 % bei Beschäftigten in der Altenpflege (Skudlik et al. 2009) oder von einer Ein-Jahres-Prävalenz von ebenfalls ca. 20 % bei Beschäftigten in der Krankenpflege berichtet (Brans u. Skudlik 2019; Hamnerius et al. 2018; Ibler et al. 2012). Aktuelle Studien zeigen eine pandemiebedingte Intensivierung der Hygienemaßnahmen im Gesundheitsbereich, wodurch das Auftreten berufsbedingter Hautveränderungen noch häufiger beobachtet wurde (Lan et al. 2020; Elston et al. 2020; Cavanagh et al. 2020; Greveling et al. 2020; Guertler et al. 2020). Mit 6327 Verdachtsfällen im Jahr 2020 zeigt sich dieser aufsteigende Trend bislang nicht in den gemeldeten Verdachtsfällen einer berufsbedingten Hautkrankheit bei Versicherten im Gesundheitswesen der BGW (gemäß persönliche Mitteilung von Sabine Kühn, BGW, Mai 2021); die Zahlen bleiben im Vergleich zu den Zahlen aus dem Jahr 2018 konstant (hoch).
Was führt zu diesen hohen Zahlen von Berufsdermatosen im Gesundheitswesen? Pflegerisches Fachpersonal verübt zu einem Großteil Arbeiten im feuchten Milieu. Unter der so genannten Feuchtarbeit werden „Tätigkeiten [gefasst], bei denen die Beschäftigten einen erheblichen Teil ihrer Arbeitszeit, das heißt regelmäßig mehr als 2 Stunden mit ihren Händen Arbeiten im feuchten Milieu ausführen oder häufig beziehungsweise intensiv ihre Hände reinigen müssen oder einen entsprechenden Zeitraum feuchtigkeitsdichte Schutzhandschuhe mit Okklusionseffekt (Wärme- und Flüssigkeitsstau) tragen“ (Abs. 3.3.4 (2) TRGS 401). Zudem ist neben den Händen auch zunehmend der Gesichtsbereich unter dem Mund-Nasen-Schutz von Hautveränderungen betroffen. Neben mechanischen Druckstellen und Unverträglichkeitsreaktionen auf das Material spielen auch hier okklusive Effekte, die durch die feuchte Atemluft verstärkt werden, eine entscheidende Rolle (Singh et al. 2020; Del Castillo Pardo de Vera et al. 2020; Zhou et al. 2020; Smart et al. 2020).
Möglichkeiten des Hautschutzes – das integrative Hautschutzmodell
Wie können die Beschäftigten ihre Haut auch unter diesen intensivierten Hygienemaßnahmen schützen? Welche Regeln sollten beachtet werden?
Studien deuten darauf hin, dass die Haut bestmöglich geschützt wird, wenn vor und während der Arbeit „Hautschutz“ im engeren Sinne angewendet wird. Darunter wird das konsequente Tragen von Schutzhandschuhen und gegebenenfalls das Auftragen einer Hautschutzcreme verstanden. Zusätzlich sollten die Hände gereinigt und/oder desinfiziert werden, um Schmutz und Pathogene zu entfernen, und nach der Arbeit soll eine aufgetragene Hautpflegecreme die Hautregeneration unterstützen. Dieses Drei-Säulen-Modell (Schutz, Pflege, Reinigung) ist reduzierten Modellen mit beispielsweise nur zwei Säulen (z. B. Hautschutz und Reinigung/Desinfektion) überlegen (Winkler et al. 2009; Kütting et al. 2010). Im Folgenden werden die einzelnen Komponenten des integrativen Hautschutzmodells näher betrachtet.
Hautschutz – Auswahl und Anwendung von Schutzhandschuhen
Wie kann der richtige Schutzhandschuh gefunden werden? Hierfür bieten deutsche Normen (DIN), europäische Normen (EN) und internationale Normen (ISO) zur Handschuhzertifizierung eine erste Orientierung: Schutzhandschuhe, die dem Schutz der Patientinnen und Patienten dienen, sind mit der DIN EN 455 als medizinische Schutzhandschuhe zum einmaligen Gebrauch zertifiziert. Im Gesundheitsbereich sollten Handschuhe, die direkt am Menschen angewendet werden, folglich dieser Norm entsprechen. Schutzhandschuhe, die die anwendende Person schützen, gelten als Teil der persönlichen Schutzausrüstung und sind, wenn sie zum Beispiel vor Flüssigkeiten, chemischen Gefahren (z. B. Flächendesinfektionsmittel) und Mikroorganismen schützen, mit der DIN EN ISO 374 gekennzeichnet. Darüber hinaus gilt für alle Schutzhandschuhe die Handschuhgrundnorm
DIN EN ISO 21420:2020-06. Die Auswahl der Schutzhandschuhe richtet sich sowohl nach Art und Dauer der Exposition (z. B. Art der Chemikalie, Kurzkontakt vs. Dauerkontakt) als auch nach den Bedarfen der anwendenden Person (z. B. Größe, Haptik, Schwitzempfinden, Typ-IV-Sensibilisierungen) sowie beispielsweise nach berufsspezifischen Vorschriften oder – in Zeiten der SARS-CoV-2-Pandemie – nach Verfügbarkeit. So hat die Pandemie zu einer deutlichen Materialverknappung auf dem Markt medizinischer Schutzhandschuhe geführt.
Handschuhe zum Schutz der Patientinnen und Patienten
Nach DIN EN 455 zertifizierte Handschuhe müssen im Penetrationstest1, in dem standardisiert die Dichtigkeit eines Handschuhs gegenüber Wasser gemessen wird, eine annehmbare Qualitätsgrenzlage (Accepted Quality Level; AQL) von ≤ 1,5 erreichen; hiermit gilt der Standard als medizinischer Einmalhandschuh als erfüllt (TRBA 250 2015). Ein AQL von 1,5 bedeutet, dass max. 1,5 % der Handschuhe einer Charge Fehlstellen (z. B. mikroskopisch kleine Löcher) aufweisen dürfen und damit bereits vor dem ersten Tragen defekt sind. Für die Praxis bedeutet dies, dass pro Paket mit einer Stückzahl von 100 ein bis zwei Handschuhe Löcher haben können, wenn ein AQL von 1,5 angegeben wird. Das Verfahren zur Bestimmung des AQL entspricht der Wasser-Leck-Prüfung zur Testung der Penetration gemäß DIN EN ISO 3742-2 (Schutzhandschuhe gegen Chemikalien und Mikroorganismen; Teil 2: Bestimmung des Widerstandes gegen Penetration). Mit dieser Methode wird ein Schutz vor Bakterien und Pilzsporen ausgelobt (vgl. DIN EN ISO 374-1: Schutzhandschuhe gegen Chemikalien und Mikroorganismen. Teil 1: Terminologie und Leistungsanforderungen). Eine nachgewiesene Virenbeständigkeit ist nicht Voraussetzung zur Zulassung eines medizinischen Einweghandschuhs. Zwischenzeitlich wurde mit der DIN EN ISO 374, Teil 5, ein Penetrationstest mit einem Modellbakteriophagen im Normungskatalog ergänzt, mit dem bereits einige Hersteller von medizinischen Einweghandschuhen (freiwillig) ihre Handschuhe prüfen. Handschuhe, die gegenüber Viren getestet wurden, erhalten unter dem Piktogramm für bakteriologische Kontamination zusätzlich das Wort VIRUS in Großbuchstaben.
Handschuhe als Persönliche Schutzausrüstung für zum Beispiel Reinigungs- und Flächendesinfektionsarbeiten
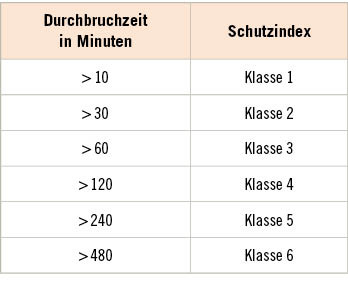
Für den Kontakt zu wässrigen Reinigungs- und Flächendesinfektionsmitteln (oder auch zu bestimmten Therapeutika wie Zytostatika) sollten Chemikalienschutzhandschuhe verwendet werden, die einen nachgewiesenen Schutz vor Durchdringung (Permeation) dieser Arbeitsstoffe aufweisen (Arbeitskreis „Krankenhaus und Praxishygiene“ der AWMF 2017; Weber 2013). Dies sind Schutzhandschuhe, die gemäß DIN EN ISO 16523-1 (zuvor DIN EN ISO 374-3) hinsichtlich der Permeation bestimmter (Prüf-)Chemikalien geprüft wurden. Permeation bezeichnet dabei die Diffusion auf molekularer Ebene von 1 µg/(cm² x min) der Prüfchemikalie bei 23° ± 1 °C. Es gibt 18 Prüfchemikalien3, wobei der Handschuh nicht gegenüber jeder beständig sein muss. Je nach Durchbruchszeit werden verschiedene Schutzlevel ausgewiesen (➥ Tabelle 1). Eine Prüfung der Permeationszeit über 480 min hinaus ist im Prüfverfahren nicht vorgesehen. Daher können keine Aussagen zum Schutz eines Handschuhs darüber hinaus getätigt werden.
Eine Kennzeichnung gemäß DIN EN ISO 16523-1 (Piktogramm Erlenmeyerkolben) als Chemikalienschutzhandschuh erhält ein Handschuh durch ein ausgewiesenes Prüfinstitut. Handschuhe werden abhängig von den ermittelten Durchbruchszeiten dem Typ A, B oder C zugeordnet:
- Typ C: Permeationszeit mindestens 10 min (entspricht Schutzlevel 1) gegenüber einer Prüfchemikalie,
- Typ B: Permeationszeit von mindestens 30 min (entspricht Schutzlevel 2) gegenüber 3 Prüfchemikalien,
- Typ A: Permeationszeit von mindestens 30 min (entspricht Schutzlevel 2) gegenüber 6 Prüfchemikalien).
Die Buchstaben unter dem Piktogramm geben Auskunft über die positiv getesteten Prüfchemikalien; damit wird auch deutlich, dass es keinen universellen Chemikalienschutz geben kann.
In der Regel sollten dickwandige Chemikalienschutzhandschuhe für Reinigungs- und Desinfektionsarbeiten, und keine medizinischen Einmalhandschuhe, verwendet werden (Arbeitskreis „Krankenhaus und Praxishygiene“ der AWMF 2017; TRBA 250 2015). Je nach Hygienevorschrift und/oder chemikalienabhängigen Permeationszeiten ist allerdings auch ein „Mehrweghandschuh“ nach einmaligem Gebrauch zu verwerfen.
Aufgrund hoher Arbeitszeitdichte und hoher arbeitspraktischer Relevanz stellt sich Frage, inwiefern auch medizinische Einweghandschuhe für kurzzeitige Flächendesinfektionen nutzbar sind. Im Rahmen einer 2015 durchgeführten Befragung bei zwölf Herstellern von medizinischen Einweghandschuhen wurden die Permeationszeiten von insgesamt 50 handelsüblichen Flächendesinfektionsmitteln und deren Gebrauchslösungen erfragt. Lediglich vier der Hersteller übermittelten konkrete, produktspezifische Angaben, die restlichen Hersteller machten Aussagen zu Reinsubstanzen oder antworteten nicht beziehungsweise konnten keine Aussage treffen. Konkrete Permeationszeiten lagen folglich nur von einzelnen Herstellern vor. Diese könnten als Hinweis für eine mögliche Eignung medizinischer Einweghandschuhe für eine kurzzeitige Flächendesinfektion unter bestimmten Bedingungen interpretiert werden. Anhand der ermittelten (und vielen fehlenden) Angaben lassen sich allerdings keine allgemeingültigen Aussagen, zum Beispiel zur Verwendung des Desinfektionsmittels (Konzentrat oder Gebrauchslösung), des Handschuhmaterials und/oder die Schichtstärke ableiten, so dass bei der Handschuhauswahl weiterhin Herstelleranfragen notwendig bleiben (Hansen et al. 2015). Für ausgewiesene Tätigkeiten in einem zeitlichen Umfang von unter einer Minute im Umgang mit chemischen Produkten, „bei denen es sich nicht um krebserzeugende, keimzellmutagene, reproduktionstoxische (CMR-)Substanzen (z. B. kein Formaldehyd) handelt und die die Handschuhe nachweislich nicht auflösen oder erkennbar aufquellen lassen“, können gemäß der kürzlich erschienenen DGUV Information 213-032 „Gefahrstoffe im Gesundheitsdienst“ für bestimmte ausgewiesene Tätigkeiten medizinische Nitrileinmalhandschuhe verwendet werden (DGUV 2021, S. 21). Dies ist allerdings je nach pflegerischem Kontext nicht ausnahmslos zu empfehlen, da mit zunehmender Tragedauer das Perforationsrisiko steigt (Kramer et al. 2016) und damit eine Schutzleistung sowohl gegenüber Pathogenen als auch Chemikalien nicht mehr gegeben ist.
Neben medizinischen Einweghandschuhen gibt es auch Einweghandschuhe, die gemäß der DIN EN ISO 374-3/DIN EN ISO 16523-1 zertifiziert sind und gegenüber ausgewiesenen Chemikalien für eine bestimmte Zeit schützen können. Diese können eine sinnvolle Alternative für die Durchführung von Flächendesinfektionsarbeiten sein, da dies die Gefahr einer zu langen Verwendung (wie z. B. bei einem „Mehrweghandschuh“) reduziert und gegebenenfalls kontextabhängige Hygieneregeln kostengünstiger eingehalten werden können.
Probleme bei und Lösungen für Kontaktallergien gegenüber Handschuhinhaltsstoffen
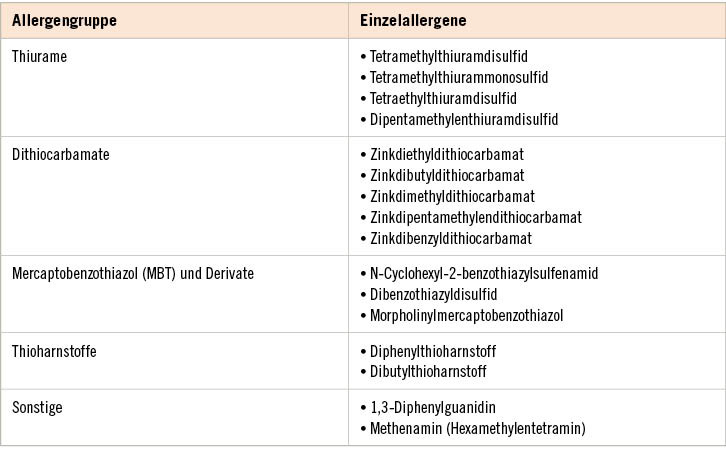
Manchmal werden Schutzhandschuhe selbst zum Problem, wenn zum Beispiel die Person, die die Handschuhe anwendet, eine Typ-IV-Sensibilisierung gegenüber einem darin enthaltenen Inhaltsstoff aufweist. Dabei handelt es sich in der Regel um während der Produktion eingesetzte Stoffe, die der Vernetzung von natürlichem (Latex) oder synthetischem Kautschuk (Nitril, Chloropren/Neopren, Fluor, Butyl) dienen, den so genannten Vulkanisationsbeschleunigern oder Akzeleratoren (➥ Tabelle 2).
Ob und welche Vulkanisatoren in einem Schutzhandschuh verwendet werden, ist materialabhängig und herstellerspezifisch, so dass eine Herstelleranfrage in der Regel sinnvoll und notwendig ist (Rose et al. 2009). Bereits technische Datenblätter zu Schutzhandschuhen können Informationen zu verwendeten Beschleunigern beinhalten. Bei einem Verdacht auf ein durch eine Typ-IV-
Sensibilisierung ausgelöstes allergisches Kontaktekzem sollte dies dem Unfallversicherungsträger gemeldet werden (Skudlik u. Elsner 2021) und eine Abklärung mittels Epikutantest durch die Hautärztin oder den Hautarzt erfolgen. Sollte sich der Verdacht bestätigen, gibt es im Bereich der Einweghandschuhe einen wachsenden Sektor an Handschuhen, die herstellerseits als „akzeleratorenfrei“ ausgelobt werden (Crepy et al. 2018).
Zwischen Thiuramen und Dithiocarbamaten sind „Kreuzreaktionen“ beschrieben worden. Daher sollte bei einer bekannter Sensibilisierung gegenüber einem der beiden Stoffe beide Allergengruppen gemieden werden (Hansson et al. 2014; Diepgen et al. 2008; Crepy et al. 2016).
Richtige Anwendung von Schutzhandschuhen und Hautschutzcremes
Hinweise zur Anwendung von Handschutzcreme unter Schutzhandschuhen finden sich in dem Artikel von Fartasch (2021) dieser Ausgabe.
Chemikalienschutzhandschuhe schützen die anwendende Person für eine definierte Zeit, die nicht der bereits vorgestellten, im Labor ermittelten Permeationszeit entsprechen muss, da unter Praxisbedingungen die Durchbruchzeit bis auf ein Drittel der unter DIN EN 374-3/DIN EN ISO 16523-1 ermittelten Permeationszeit sinken kann. Dies begründet sich zum Beispiel mit höheren Temperaturen und/oder einer zusätzlichen mechanischen Beanspruchung (TRGS 401). Entsprechend ist der Handschuh unter arbeitspraktischen Bedingungen deutlich früher als die Permeationszeit gemäß Herstellerangabe erwarten ließe zu entsorgen.
(Medizinische) Einweghandschuhe sollten nur einmal verwendet werden. Gemäß der Kommission für Krankenhaushygiene und Infektionsprävention (KRINKO) beim Robert Koch-Institut (Kramer et al. 2016) und dem Arbeitskreis „Krankenhaus- und Praxishygiene“ der AWMF (2017) bedeutet dies, dass medizinische Einmalhandschuhe nach jedem Patientenkontakt und im Intensivbereich sowie bei nicht sterilen und gleichzeitig mechanisch belastenden Tätigkeiten spätestens nach 15 min gewechselt werden sollten, da mit zunehmender Tragedauer das Risiko für Materialschäden an den Fingerspitzen steigt. Mit steigender Tragedauer steigt zusätzlich auch das Risiko für handschuhbedingte Okklusionseffekte. Wie eingangs erwähnt, zählt das Tragen okklusiver Schutzhandschuhe durch die sich unter dem Handschuh sammelnde Flüssigkeit zur Feuchtarbeit. Die Feuchtigkeit lässt die Haut mazerieren, wodurch sie vorübergehend während und nach Beendigung der Okklusion durchlässiger für Fremdstoffe und reizbarer wird (Fartasch et al. 2012). Daher sollten Schutzhandschuhe ausschließlich auf sauberer und trockener Haut angewendet werden (Arbeitskreis „Krankenhaus- und Praxishygiene der AWMF 2017; Ramsing u. Agner 1996).
Um einer Feuchtansammlung unter okklusiven Schutzhandschuhen zu begegnen, sollten flüssigkeitsdichte Schutzhandschuhe möglichst kurzzeitig getragen werden. Wenn sich längere durchgängige Handschuhtragezeiten nicht verhindern lassen, können Unterziehhandschuhe aus hygroskopischem Material wie Baumwolle verwendet werden. Diese nehmen bis zur Materialsättigung die Feuchtigkeit auf und leiten sie so von der Hautoberfläche weg. Für den bestmöglichen Effekt sollten die Baumwollunterziehhandschuhe mit beginnender Durchfeuchtung gewechselt werden (Sonsmann et al. 2015). Die Zeit bis zum erforderlichen Wechsel ist je nach Schwitzneigung und äußeren Bedingungen individuell sehr verschieden. Zum Erhalt der Taktilität an den Fingerspitzen gibt es Baumwollhandschuhe auch finger- oder fingerspitzenlos. Spätestens mit dem Wechsel des Überziehhandschuhs sollten die Baumwollhandschuhe gewechselt werden. Im medizinischen Bereich ist eine Mehrfachverwendung aus hygienischen Gründen unmöglich. Allerdings können die Handschuhe mit der Klinik- oder Hauswäsche wieder aufbereitet und somit erneut verwendet werden (Hübner et al. 2016).
Einige Hersteller von Hautschutzcremes loben ihre Produkte mit dem Zusatz aus: „unter Schutzhandschuhen geeignet/anwendbar“ oder „Hautschutzcreme schützt die Haut vor wässrigen oder wassergemischten Arbeitsstoffen und bei Feuchtarbeit. Auch beim Tragen von Handschuhen“. Hautschutzcremes unterliegen der Kosmetikverordnung. Gemäß § 11(2)d hat der Hersteller eine Nachweispflicht für die von ihm getätigten Produktauslobungen. Für den Nachweis der Eignung einer Schutzcreme unter Schutzhandschuhen gibt es bislang keinen verbindlichen Standard zur Objektivierung. Auf Nachfrage wird die Eignung getestet, indem ein Test auf Degradation des Handschuhs oder auf Wasserdurchlässigkeit (bislang häufig bei Latexeinmalhandschuhen) mit und ohne vorherige Cremeapplikation durchgeführt wird. Der Test auf Degradation (DIN EN ISO 374-4) beinhaltet den Test auf Durchstichfestigkeit und/oder auf Gewichtsveränderungen. Damit werden mögliche Auswirkungen auf die physikalische Integrität eines Handschuhs (Verdichtung vs. Materiallockerung) gemessen. Laut Arbeitskreis „Krankenhaus- und Praxishygiene“ der AWMF (2017) verändere sich die Reißfestigkeit eines Latexeinmalhandschuhs nach Auftragen einer fetthaltigen Creme kaum. Bei dem Test auf Wasserdichtigkeit wird ein möglicher Einfluss auf die Penetration gemäß DIN EN ISO 374-2 oder DIN EN ISO 455-2 erfasst. Beide Verfahren erfassen nicht mögliche Interaktionseffekte zwischen Creme und Handschuh in Richtung Auswirkung auf Permeationseigenschaften oder eine mögliche Begünstigung der Freisetzung von Handschuhinhaltsstoffen (siehe Handschuhallergene). Das heißt, zur Eignung von Hautschutzcreme unter Schutzhandschuhen können, bezogen auf die Material- und Schutzbeständigkeit eines Schutzhandschuhs, keine abschließenden Aussagen getroffen werden. Sofern eine Hautschutzcreme unter Handschuhen angewendet werden soll, sollte sie vollständig eingezogen und entsprechend der Auslobung für die Verwendung unter Schutzhandschuhen geeignet sein.
Nach dem Tragen von Schutzhandschuhen sollten die Hände desinfiziert werden, da medizinische Einweghandschuhe häufig nur mit Übung ohne Kontakt mit der gegebenenfalls kontaminierten Handschuhoberfläche beziehungsweise -außenseite ausgezogen werden können (Oreskov et al. 2015). Zudem kann bei Modellen mit einem ausgewiesenen AQL von 1,5 aufgrund der bereits vor dem Tragen eventuell vorhandenen Fehlstellen eine Kontamination der Hände trotz Tragen von Schutzhandschuhen nicht gänzlich ausgeschlossen werden.
Vor dem Anlegen neuer Schutzhandschuhe sollte das Händedesinfektionsmittel vollständig verdunstet sein, da andernfalls ein Herauslösen von gegebenenfalls allergenen Handschuhinhaltsstoffen begünstigt sein könnte. Zumindest für den Vulkanisationsbeschleuniger 1,3-Diphenylguanidin konnte eine mit alkoholischen Handdesinfektionsmittel bedingte verstärkte Freisetzung dokumentiert werden, obwohl das Mittel ordnungsgemäß verwendet wurde und vollständig verdunstet war (Hamnerius et al. 2019).
Foto: Pornpak Khunatorn / Getty Images
Hände hautschonend reinigen und desinfizieren
Gemäß Hygienevorschriften im medizinischen Bereich sind die Hände, Handgelenke und bei Bedarf Unterarme regelmäßig und konsequent zu reinigen und zu desinfizieren. Schon lange gilt im Gesundheitsbereich das Motto „besser desinfizieren als waschen“, zumindest sofern diesem Vorgehen Hygieneanforderungen indikationsabhängig nicht widersprechen. Durch die Händewaschung mit Wasser wird die Integrität der Hautbarriere geschädigt, da unter anderem Hautlipide herausgelöst werden (Hübner et al. 2015; Batalla et al. 2012; Kampf et al. 2009) und das Stratum corneum quillt und mazeriert. Die Quellung findet Ausdruck in einer bis zu 8- bis 10-minütigen Hyperhydratation, die durch Verdünnungseffekte eine eventuell anschließende Händedesinfektion in ihrer Wirksamkeit abschwächen kann (Hübner et al. 2015). Händewaschungen mit Wasser sollten daher nur in Ausnahmefällen gemäß Vorgaben durchgeführt werden, zum Beispiel bei sichtbaren Verschmutzungen und zum Entfernen von Proteinen und Sporen (Clostridium difficile) (Kampf et al. 2009; RKI 2000; WHO 2020).
Die hygienische Händedesinfektion erfolgt in der Regel mit Desinfektionsmitteln auf Alkoholbasis. Alkohole sind vergleichsweise gut hautverträglich und haben ein geringes Sensibilisierungspotenzial, wohingegen die den Desinfektionsmitteln zugesetzten Rückfetter, Hilfs-, Duft-, Konservierungs- und Farbstoffe durchaus ein allergenes Potenzial bergen können (Hübner et al. 2015; Batalla et al. 2012). Alkohole haben analog zu den Tensiden ebenfalls hohe fettlösende Eigenschaften. Während einer Händedesinfektion werden daher auch Hautlipide herausgelöst und in Lösung gebracht, verdunsten allerdings nicht gemeinsam mit dem Händedesinfektionsmittel, sondern verbleiben auf der Haut. Damit begründet sich unter anderem die bessere Hautverträglichkeit der Händedesinfektion gegenüber der Händewaschung (Hübner et al. 2015). Auch ein 2021 veröffentlichtes Review bestätigt erneut die im Vergleich zur Händewaschung bessere Hautverträglichkeit der Händedesinfektion (Tasar et al. 2021). Allerdings ergeben sich hieraus auch Hinweise zur richtigen oder falschen Anwendung. Sollten Überschüsse von Händedesinfektionsmitteln beispielsweise mit einem Papiertuch oder am Kittel abgewischt werden, werden die Hautfette ebenfalls mit entfernt und der im Gegensatz zur Händewaschung hautschonende Effekt geht verloren.
Da Alkohole an Hautläsionen zu brennenden und schmerzenden Missempfindungen führen, glauben die anwendenden Personen vielfach, die Händedesinfektion sei „aggressiver“ beziehungsweise hautschädigender als die Händewaschung und waschen daher häufiger die Hände, anstatt sie zu desinfizieren (Hübner et al. 2015; Batalla et al. 2012, Stutz et al. 2009). Dadurch kann ein Teufelskreis entstehen, da die Händewaschung unter anderem durch den Entzug der epidermalen Lipide die ohnehin schon vorgeschädigte Hautbarrierefunktion weiter beeinträchtigt (Sonsmann et al. 2017).
Gemäß Positionspapier der „EADV Task Force on Contact Dermatitis“ sollen sich Beschäftigte in Gesundheitsfachberufen vor und nach jeder Tätigkeit die Hände reinigen und dabei Hautreinigungsmittel ohne Duft- und Konservierungsstoffe verwenden beziehungsweise besser – sofern hygienisch möglich – die Hände desinfizieren und dabei ein alkoholisches Händedesinfektionsmittel mit Glycerin als Rückfetter verwenden. Nach möglichst jeder Händewaschung sollte zudem eine duftstofffreie Hautschutzcreme aufgetragen werden (Balato et al. 2020). Da die desinfizierende Wirkung der Händedesinfektion nur unmaßgeblich von einer zuvor erfolgten Applikation einer Hautschutzcreme abzuhängen scheint (Paula et al. 2017), könnte auch vor der Händedesinfektion bei Bedarf eine Hautschutzcreme benutzt werden.
Hautpflege
Die Hautpflege rundet den Hautschutz ab. Hautpflegecremes sind – sofern sie von Hautschutzcremes unterschieden werden – „reichhaltiger“, das heißt fetthaltiger in der Formulierung, ziehen in der Regel langsamer ein und können bisweilen Harnstoff enthalten, was die Haut weicher und durchlässiger werden lässt. Hautpflegecremes sollten daher erst nach der Arbeit, im privaten Kontext beziehungsweise allgemein in Zeiten ohne Hautbelastung aufgetragen werden.
Hautschonender Einsatz von Mund-Nasen-Schutzmasken und Schutzbrillen
Zur persönlichen Schutzausrüstung zum Schutz vor SARS-CoV-2 gehört ebenfalls das konsequente Tragen von Mund-Nasen-Schutzmasken und auf Covid-19-Stationen das zusätzliche Tragen von Schutzbrillen, Visieren und zusätzlicher Schutzbekleidung (Schutzoverall, Kopf- und Schuhabdeckung und „double gloving“ [zwei Paar medizinische Einweghandschuhe]). Für den Mund-Nasen-Schutz gibt es unterschiedliche Masken. Dazu zählen zum Beispiel FFP2-Masken, medizinischer Mund-Nasen-Schutz und OP-Masken (Li et al. 2021).
Für einen effektiven Schutz müssen Mund-Nasen-Schutzmasken und Schutzbrillen fest anliegen und die Haut abdichten. Daher führen sie bei vielen Anwenderinnen und Anwendern zu mechanischer Reibung und zu Druckstellen vorwiegend auf dem Nasenrücken, am Kinn, an der Stirn, im Wangenbereich und an den Ohren (Singh et al. 2020; Del Castillo Pardo de Vera et al. 2020; Zhou et al. 2020; Smart et al. 2020). Zur Prävention dieser Druck- und Reibestellen wird empfohlen – sofern möglich –, Tragepausen einzulegen und verschiedene Modelle abwechselnd zu verwenden. Unterschiedliche Modelle haben häufig einen anderen Sitz und damit andere Druck- und Reibepunkte. Des Weiteren gibt es verschiedene Publikationen, in denen eine Abdeckung mechanisch betroffener Hautareale mit Hydrokolloid-Pflastern (Del Castillo Pardo de Vera et al. 2020), Hydrogel-Augen-Pflastern (Zhou et al. 2020) oder Silikon-Pflastern (Smart et al. 2020) beschrieben wurde, die die Dichtigkeit der Maske nicht reduzieren und den Tragekomfort steigern sollen.
Neben den Druckstellen begünstigt die Wärme- und Feuchtigkeitsansammlung unter den Mund-Nasen-Schutzmasken (Okklusionseffekt durch die feuchte Atemluft und der Ansammlung von Schweiß) Hautveränderungen wie die irritative Kontaktdermatitis, die allergische Kontaktdermatitis, Dermatitis aufgrund von Schwitzen, Akne und die Lippenleckendermatitis (Singh et al. 2020). Auch eine Rosazea kann begünstigt werden, und trockene, juckende, gerötete Haut, Bläschenbildung und Ulzerationen im Maskenbereich werden beschrieben. Da öl- und fetthaltige Gesichtscremes sowie Make-up okklusive Effekte unter der Maske begünstigen, sollte während langer Tragezeiten von Masken auf diese Externa möglichst verzichtet werden. Zur Prävention sollten die Masken gewechselt werden, sobald sie feucht werden. Feuchte Masken schützen nicht mehr zuverlässig und können die Haut reizen. Sofern möglich sollten Pausenzeiten eingehalten und nach dem Tragen von Masken die Haut mit Wasser und einem milden Hautreinigungsmittel gereinigt werden. Gegen den Okklusionseffekt unter Masken wurde das Einlegen und regelmäßige Wechseln eines Papiertuchs beschrieben und publiziert (Yu et al. 2020). Bei auftretenden Hautbeschwerden können andere Masken ausprobiert werden. Die Masken unterscheiden sich nicht nur im Sitz, sondern auch in der Verarbeitung.
Bei persistierenden Beschwerden sollte dermatologischer oder betriebsärztlicher Rat eingeholt werden. Entsprechende Fachärztinnen und -ärzte können die Hautveränderungen diagnostizieren und behandeln und gegebenenfalls dem Unfallversicherungsträger melden (Skudlik u. Elsner 2021). So kann auch eine mögliche Typ-IV-Sensibilisierung gegenüber Inhaltsstoffen aus der jeweiligen Maske ausgeschlossen beziehungsweise identifiziert werden. Modellabhängig sind zum Beispiel Nickel in der formgebenden Nasenfixierung, Formaldehyd oder Latex im Gummiband neben eventuell weiteren Allergenen nicht auszuschließen (Yu et al. 2021).
Fazit
Beschäftigte in pflegerischen Berufen üben in hohem Maße Arbeiten im feuchten Milieu aus, wodurch das Risiko für die Entstehung berufsbedingter Hauterkrankungen steigt. Bedingt durch die SARS-CoV-2-Pandemie hat sich das Risiko weiter erhöht, da die Hände häufiger gereinigt und/oder desinfiziert werden, länger Schutzhandschuhe getragen werden und zusätzliche, persönliche Schutzausrüstung (PSA) wie Mund-Nasen-Schutz und Schutzbrillen benötigt wird. Dadurch können neben den Händen auch der Gesichts- und Kopfbereich von Hautveränderungen betroffen sein.
Der Zunahme der hautbelastenden Arbeitsbedingungen sollte mit einer Intensivierung von Hautschutzmaßnahmen begegnet werden. Dafür sind eine Schulung aller pflegerisch Beschäftigten, die Bereitstellung ausreichender und verschiedener PSA sowie ausreichend Personal, um Pausenzeiten einzuhalten, notwendig. Während ein besserer Personalschlüssel häufig nicht direkt beeinflussbar ist, kann im Rahmen der Verhaltensprävention jede einzelne Person vieles im Kontext Hautschutz richtig, aber auch falsch machen. Demzufolge bleiben die Implementierung von Hautschutzmaßnahmen sowie die Begleitung, Beratung und Therapie von pflegerisch beschäftigten Patientinnen und Patienten weiterhin herausfordernde, aber auch lohnende Bereiche betriebsärztlichen und dermatologischen Wirkens.
Interessenkonflikt: Als Mitarbeitende des iDerm sind die Autorinnen und der Autor in die Behandlung und Beratung von Patientinnen und Patienten mit berufsbedingten Hautkrankheiten involviert. Interessenkonflikte liegen nicht vor.
Literatur
Balato A et al.: European Task Force on Contact Dermatitis statement on coronavirus disease‐19 (COVID‐19) outbreak and the risk of adverse cutaneous reactions. J Eur Acad Dermatol Venereol 2020; 34: e353–e354.
Batalla A et al.: Products for hand hygiene and antisepsis: use by health professionals and relationship with hand eczema. Actas Dermosifiliogr 2012; 103: 192–197.
Berufsgenossenschaft für Gesundheitsdienst und Wohlfahrtspflege (Hrsg.): Jahresbericht 2018. 2019. Abrufbar unter: https://www.bgw-online.de/SharedDocs/Downloads/DE/Medientypen/BGW%20Grundlagen/BGW55-80-180_Jahresbericht-2018_Download.pdf?__blob=publicationFile (letzter Zugriff: 27.06.2021).
Brans R, Skudlik C: Prävention des Handekzems. Hautarzt 2019; 70: 797–803.
Bundesanstalt für Arbeitsschutz und Arbeitsmedizin (BAuA): Technische Regel für Gefahrstoffe – Gefährdung durch Hautkontakt – Ermittlung, Beurteilung, Maßnahmen. TRGS 401. Juni 2008 zuletzt berichtigt GMBl 2011 S. 175 [Nr. 9]. Abrufbar unter: https://www.baua.de/DE/Angebote/Regelwerk/TRGS/pdf/TRGS-401.pdf?__blob=publicationFile&v=2 (letzter Zugriff: 27.06.2021).
Bundesanstalt für Arbeitsschutz und Arbeitsmedizin (BAuA): Technische Regeln für Biologische Arbeitsstoffe. Biologische Arbeitsstoffe im Gesundheitswesen und in der Wohlfahrtspflege. TRBA 250. 2014, GMBl 2014, Nr. 10/11 vom 27.03.2014, Änderung vom 22.05.2014, GMBl Nr. 25, Änderung vom 21.07.2015, GMBl Nr. 29. Abrufbar unter: http://www.baua.de/de/Themen-von-A-Z/Biologische-Arbeitsstoffe/TRBA/pdf… (letzter Zugriff: 27.06.2021).
Cavanagh G, Wambier CG: Rational hand hygiene during the coronavirus 2019 (COVID-19) pandemic. J Am Acad Dermatol 2020; 82: e211.
Crepy MN et al.: Accelerator-free gloves as alternatives in cases of glove allergy in healthcareworkers. Contact Dermatitis 2018; 78: 28–32.
Crepy MN: Rubber: new allergens and preventive measures. Eur J Dermatol 2016; 26: 523–530.
Del Castillo Pardo de Vera JL et al.: The preventive effect of hydrocolloid dressing to prevent facial pressure and facial marks during use of medical protective equipment in COVID-19 pandemic. Br J Oral Maxillofac Surg 2020; 58: 723–725.
Deutsche Gesetzliche Unfallversicherung (DGUV) (2021): DGUV Information 213-032 „Gefahrstoffe im Gesundheitsdienst“. 2021. Abrufbar unter: https://publikationen.dguv.de/widgets/pdf/download/article/844 (letzter Zugriff: 27.06.2021).
Diepgen TL et al.: Beurteilung der Auswirkung von Allergien bei der Minderung der Erwerbsfähigkeit im Rahmen der BK 5101: Thiurame, Mercaptobenzothiazole, Dithiocarbamate, N-Isopropyl-N’-phenyl-p-phenylendiamin. Dermatologie in Beruf und Umwelt 2008; 56: 11–24.
Elston DM: Occupational skin disease among health care workers during the coronavirus (COVID-19) epidemic. J Am Acad Dermatol 2020; 82: 1085–1086.
Fartasch M et al.: Evidence of increased skin irritation after wet work: impact of water exposure and occlusion. Contact Dermatitis 2012; 67: 217–228.
Greveling K, Kunkeler ACM: Hand eczema pandemic caused by SARS-CoV-2 hygiene measures: the setup of a hand eczema helpline for hospital personnel. J Eur Acad Dermatol Venereol 2020; 34: e556–e557.
Guertler A et al.: Onset of occupational hand eczema among healthcare workers during the SARS-CoV-2 pandemic – comparing a single surgical site with a COVID-19 intensive care unit. Contact Dermatitis 2020; 83: 108–114.
Haamann F, Pohrt U, DGUV (Hrsg.): Achtung Allergiegefahr. BGI/GUV-I 8584. 2012. Abrufbar unter: https://www.gesundheitsdienstportal.de/files/GUV-I-8584-Allergiegefahr-durch-Latex-.pdf (letzter Zugriff: 27.06.2021).
Hamnerius N et al.: Skin exposure to the rubber accelerator diphenylguanidine in medical gloves-An experimental study. Contact Dermatitis 2019; 81: 9–16.
Hamnerius N et al.: Wet work exposure and hand eczema among healthcare workers: a cross-sectional study. Br J Dermatol 2018; 178: 452–461.
Hansen A et al.: Auswahl von Schutzhandschuhen zum Schutz vor Flächendesinfektionsmitteln in Pflegeberufen: Ergebnisse einer Herstellerbefragung. Dermatologie in Beruf und Umwelt 2015; 63: 126–127.
Hansson C et al.: Reaction profile in patch testing with allergens formed during vulcanization of rubber. Contact Dermatitis 2014; 70: 300–308.
Hübner NO et al.: Einsatz wiederaufbereitbarer textiler Unterziehhandschuhe für medizinische Tätigkeiten: eine Machbarkeitsstudie. Zentralblatt für Chirurgie 2016; 141: 62–67
Hübner NO et al.: Aspekte der Hautverträglichkeit, des Hautschutzes und der Hautpflege. Ein Beitrag zum Internationalen Tag der Händehygiene. Epidemiologisches Bulletin des Robert Koch-Institutes 2015; 18: 149–152.
Ibler KS et al.: Hand eczema: prevalence and risk factors of hand eczema in a population of 2274 healthcare workers. Contact Dermatitis 2012; 67: 200–207.
Kampf G, Löffler H, Gastmeier P: Hand hygiene for the prevention of nosocomial infections. Dtsch Arztebl Int 2009; 106: 649–655.
Kramer A et al.: Händehygiene in Einrichtungen des Gesundheitswesens Empfehlung der Kommission für Krankenhaushygiene und Infektionsprävention (KRINKO) beim Robert Koch-Institut (RKI). Bundesgesundheitsblatt 2016; 59: 1189–1220.
Kütting B et al.: Effectiveness of skin protection measures in prevention of occupational hand eczema: results of a prospective randomized controlled trial over a follow-up period of 1 year. Br J Dermatol 2010; 162: 362–370.
Lan J et al.: Skin damage among health care workers managing coronavirus disease-2019. J Am Acad Dermatol 2020; 82: 1215–1216.
Li DTS et al.: Facial protection in the era of COVID-19: A narrative review. Oral Dis 2021; 27 (Suppl 3): 665–673.
Oreskov KW et al.: Glove use among hairdressers: difficulties in the correct use of gloves among hairdressers and the effect of education. Contact Dermatitis 2015; 72: 362–366.
Paula H et al.: Effect of hand lotion on the effectiveness of hygienic hand antisepsis: Implications for practicing hand hygiene. Am J Infect Control 2017; 45: 835–838.
Ramsing DW, Agner T: Effect of glove occlusion on human skin (II). Long-term experimental exposure. Contact Dermatitis 1996; 34: 258–262.
Robert Koch-Institut: Händehygiene. Mitteilung der Kommission für Krankenhaushygiene und Infektionsprävention am Robert Koch-Institut. Bundesgesundheitsblatt – Gesundheitsforschung – Gesundheitsschutz 2000, 43: 230–233.
Singh M et al.: Personal protective equipment induced facial dermatoses in healthcare workers managing Coronavirus disease 2019. J Eur Acad Dermatol Venereol 2020; 34: e378–e380.
Skudlik C, Elsner P: Arbeitsbedingte Hautkrankheiten und Gesetzesänderung im Berufskrankheitenrecht zum 01.01.2021. Konsequenzen für das Vorgehen in der betriebsärztlichen Praxis. ASU Arbeitsmed Sozialmed Umweltmed 2021; 56: 186–189.
Skudlik C et al.: Hand eczema in geriatric nurses in Germany--prevalence and risk factors. Contact Dermatitis 2009, 60 (3): 136-43.
Smart H et al.: Preventing facial pressure injury for health care providers adhering to COVID-19 personal protective equipment requirements. Adv Skin Wound Care 2020; 33: 418–427.
Sonsmann FK et al.: „Ich kann mit Handschuhen nicht arbeiten!“ – oder doch? Herausforderungen und Lösungen bei der Auswahl eines adäquaten Handschuhschutzes. Aktuelle Dermatologie 2015; 41: 25–30.
Sonsmann FK, John SM, Wilke A: Hautschutz bei Beschäftigten in Gesundheitsfachberufen. Hautschutz überzeugend erklären und erfahren. In: Hofmann F, Reschauer G, Stößel U (Hrsg.): Arbeitsmedizin im Gesundheitsdienst, Band 30, edition FFAS. Freiburg im Breisgau: druckwerkstatt im grün, 2017, S. 183–195.
Stutz et al.: Nurses’ perceptions of the benefits and adverse effects of hand disinfection: alcohol-based hand rubs vs. hygienic handwashing: a multicentre questionnaire study with additional patch testing by the German Contact Dermatitis. Br J Dermatol 2009; 160: 565–572.
Tasar R, Wiegand C, Elsner P: How irritant are n‐propanol and isopropanol? – A systematic review. Contact Dermatitis 2021; 84: 1–14.
Weber LC: Reinigungsdienste und Hygiene in Krankenhäusern und Pflegeeinrichtungen. Leitfaden für Hygieneverantwortliche. Berlin, Heidelberg: Springer, 2013.
Wilke A, Skudlik C, Sonsmann FK: Individualprävention beruflicher Kontaktekzeme: Schutzhandschuhe und Hautschutzempfehlungen im berufsgenossenschaftlichen Heilverfahren. Hautarzt 2018; 69: 449–461.
Winkler R et al.: Effectiveness of skin protection creams in the prevention of occupational dermatitis: results of a randomized, controlled trial. Int Arch Occup Environ Health 2009; 82: 653–662.
World Health Organization: Infection prevention and control during health care when COVID-19 is suspected. 2020. Abrufbar unter: https://www.who.int/publications/i/item/10665-331495 (letzter Zugriff: 27.06.2021).
Yu J et al.: Occupational dermatitis to facial personal protective equipment in health care workers: A systematic review. J Am Acad Dermatol 2021; 84: 486–494.
Yu N et al.: One more paper towel, longer protection. J Am Acad Dermatol 2020; 82: e189–e190.
Zhou NY et al.: Prevention and treatment of skin damage caused by personal protective equipment: experience of the first-line clinicians treating SARS-CoV-2 Infection. Int J Dermatol Venereol 2020; 3: 70–75.
Fußnoten
Weitere Infos
Arbeitskreis der Krankenhaus- und Praxishygiene der AWMF: Leitlinien zur Hygiene in Klinik und Praxis. S1-Leitlinie Krankenhaushygiene: Anforderungen an Handschuhe zur Infektionsprophylaxe im Gesundheitswesen. 2017
https://www.awmf.org/uploads/tx_szleitlinien/029-021l_S1_Anforderungen-…
Berufsgenossenschaft der Bauwirtschaft: Allergenliste nach Hersteller
https://www.bgbau.de/themen/sicherheit-und-gesundheit/gefahrstoffe/gisb…
Kernaussagen
- Beschäftigte in Pflegeberufen haben ein hohes Risiko an einem berufsbedingten Handekzem zu erkranken, da sie häufig Arbeiten im feuchten Milieu verrichten.
- Es gibt Möglichkeiten, unter Einhaltung der Hygienevorschriften die Haut effektiv zu schützen, indem zum Beispiel kontextabhängig die Hände eher desinfiziert als gewaschen und konsequent Schutzhandschuhe getragen werden.
- Wenn Hautschutzmaßnahmen fehlerhaft angewendet werden, können sie die Haut schädigen (z. B. ungeeignete Schutzhandschuhe, Abtragen von noch flüssigem Händedesinfektionsmittel mit Papiertüchern oder am Kittel).
- Um Mund-Nasen-Schutz-bedingten Hautveränderungen im Kopfbereich vorzubeugen, sollten verschiedene MNS-Modelle abwechselnd getragen werden und auf die Anwendung von fettigen beziehungsweise öligen Externa im Gesicht verzichtet werden.
- Treten Hauterscheinungen auf, sollte eine haut- und/oder betriebsärztliche Versorgung und Beratung unter Einbeziehung des zuständigen Unfallversicherungsträgers erfolgen.
Checkliste
Pflegerisch Beschäftigte sollten, um ihre Haut bestmöglich zu schützen, idealerweise
- Pausenzeiten einhalten,
- möglichst häufig – spätestens bei beginnender Durchfeuchtung – Schutzhandschuhe und den Mund-Nasen-Schutz wechseln,
- bei längeren, ununterbrochenen Handschuhtragezeiten Baumwollunterziehhandschuhe verwenden,
- zur Infektionsprophylaxe bei längeren Handschuhtragezeiten gegebenenfalls zwei Paar medizinische Einweghandschuhe verwenden („double gloving“),
- medizinische Schutzhandschuhe nach Möglichkeit nur einmal verwenden,
- der Tätigkeit angepasste Schutzhandschuhe verwenden (z. B. für die Durchführung von Flächendesinfektionen dafür zertifizierte Schutzhandschuhe verwenden, für Arbeiten an Patientinnen und Patienten medizinische Einmalhandschuhe verwenden),
- nach jedem Handschuhtragen die Hände desinfizieren,
- Handschuhe nur auf sauberer und trockener Haut anlegen (das Händedesinfektionsmittel sollte vollständig verdunstet sein, Hautschutzcreme sollte vollständig eingezogen sein),
- ihre Hände vor und nach jeder Tätigkeit reinigen und dabei Hautreinigungsmittel ohne Duft- und Konservierungsstoffe verwenden,
- besser mit wässrigen alkoholischen Desinfektionsmitteln (mit Glycerin als Rückfetter) die Hände desinfizieren als mit Tensiden waschen,
- Händedesinfektionsmittel „ordnungsgemäß“ verwenden, das heißt dieses vollständig verdunsten lassen und nicht voreilig entfernen,
- regelmäßig duftstofffreie Hautschutzcreme verwenden (z. B. nach jeder Händewaschung; vor dem Tragen von Schutzhandschuhen sollte die Creme vollständig eingezogen sein),
- gegebenenfalls vor dem Auftragen von Händedesinfektionsmitteln die Hände mit Hautschutzcreme eincremen (vor der Desinfektion sollte die Creme vollständig eingezogen sein),
- bei der Verwendung von Hautschutzcreme auf die Auslobung und auf den Kontext achten (z. B. zum Schutz vor Wasser, unter Schutzhandschuhen geeignet),
- regelmäßig lipidreiche, duftstofffreie Hautpflegecreme auftragen (z. B. vor dem Schlafengehen),
- verschiedene Modelle von Mund-Nasen-Schutzmasken verwenden, um mechanische Druck- und Reibestellen zu wechseln und somit zu entlasten,
- gegebenenfalls Druck- und Reibestellen unter Masken zusätzlich „abpflastern“ (z. B. mit Hydrokolloidpflastern),
- gegebenenfalls ein Papiertuch zur Feuchtigkeitsaufnahme unter die FFP2-Maske legen,
- auf fett- und ölhaltige Hautpflegecremes und Make-up unter dem Mund-Nasen-Schutz verzichten,
- bei Hautveränderungen die Haut- oder Betriebsärztin bzw. den Haut- oder Betriebsarzt konsultieren.
Koautorenschaft
An der Erstellung des Beitrags beteiligt waren neben der Erstautorin Prof. Dr. med. Christoph Skudlik und Dr. rer. medic. Annika Wilke, alle Institut für interdisziplinäre Dermatologische Prävention und Rehabilitation (iDerm) an der Universität Osnabrück sowie Institut für Gesundheitsforschung und Bildung (IGB), Abteilung Dermatologie, Umweltmedizin und Gesundheitstheorie, Universität Osnabrück.