1 Ziel
Die Leitlinie richtet sich an Ärztinnen und Ärzte, die Patientinnen und Patienten mit Quarzstaublungenerkrankung und solche mit einem Verdacht darauf begutachten. Sie soll auf der Basis des aktuellen medizinisch-wissenschaftlichen und klinischen Erkenntnisstandes Empfehlungen zur Begutachtung der Berufskrankheit nach Nr. 4101 der Berufskrankheitenverordnung [1] geben.
Wesentlicher Anlass für die Erstellung der Erstfassung der Leitlinie im Jahr 2008 war, dass die seinerzeit bei geringgradig gestreuten Silikosen vielfach angewandte, auf der so genannten Moerser Konvention beruhende Begutachtachtungspraxis sich im Widerspruch zur weiterentwickelten medizinisch-wissenschaftlichen Datenlage befand.
Die Leitlinie verdeutlichte, dass zwischen dem Beschwerdebild – einschließlich Einschränkungen in der kardiopulmonalen Funktion und des Gasaustausches sowie dem radiologischen Bild – insbesondere den einzelnen Streuungskategorien nach der ILO-Klassifikation [2] anhand der Röntgen-Thoraxübersichtsaufnahme keine strenge Korrelation besteht.
Das Update der Leitlinie berücksichtigt die seit deren Erstfassung publizierte wissenschaftliche Literatur und die aus dem praktischen Umgang mit der Leitlinie gewonnenen Erfahrungen.
2 Bestandsaufnahme
Die Silikose ist seit 1929 Bestandteil der Berufskrankheitenverordnung [1]. Bis 1952 wurde die Erkrankung in der Verordnung als „schwere Staublungenerkrankung (Silikose)“, ab 1952 als „Staublungenerkrankung (Silikose)“ bzw. „Quarzstaublungenerkrankung (Silikose)“ geführt. Zunächst konnte nur die „schwere Silikose“ als Berufskrankheit entschädigt werden.
In den 1970er Jahren wurde die Absprache („Moerser Konvention“) getroffen, dass nur „relevant“ gestreute Silikosen eine Anerkennung als Berufskrankheit begründeten. Die auf Beschäftigte im Steinkohlenbergbau und weiteren Industriezweigen mit Staubexpositionen aus kristallinen Kieselsäuren angewandte „Moerser Konvention“ besagte, dass nur Silikosen mit einem Streuungsgrad von mindestens 2/3 p/q – bei Pinhead-Silikosen mindestens 2/2 p/p – oder Schwielensilikosen entschädigt wurden. So genannte niedrig gestreute Silikosen, also Silikosen, die die vorgenannten Merkmale nicht erfüllten, wurden nicht als Berufskrankheit anerkannt.
Seit 1990 wird infolge einer Entscheidung des Bundessozialgerichts aus dem Jahr 1989 zwischen dem Versicherungs- und dem Leistungsfall differenziert. Seitdem werden Silikosen mit einem niedrigen Streuungsgrad (Streuungskategorie 1/1-2/2) als Versicherungsfall anerkannt.
Von den 1335 im Jahr 2006 als BK Nr. 4101 neu angezeigten Fällen stammten 57 % aus dem Bergbau und 43 % aus anderen Gewerbezweigen; bei den im gleichen Zeitraum anerkannten 828 Fällen handelte es sich bei fast 2/3 um solche mit niedrigen bis mittleren radiologischen Streuungskategorien von 1/1 bis 2/1 oder 2/2 nach ILO 2000 [2] und bei mehr als 1/3 um solche mit Streuungskategorie 3 und/oder Schwielenbildungen.
Für das Jahr 2013 wurden 1497 Anzeigen einer BK-Nr. 4101 dokumentiert, ebenso 768 Anerkennungen, darunter 490 neue BK-Renten und 324 BK-bedingte Todesfälle. Der Großteil (563 Anzeigen) entfiel auf erkrankte Personen aus Mineralgewinnungs-/Bauberufen, gefolgt von Metallarbeitern/Mechanikern und verwandten Berufen (84 Anzeigen; vgl. BK-DOK; DGUV [3]).
3 Vorbemerkungen
3.1 Rechtliche Grundlagen zur Feststellung einer BK Nr. 4101
Nach §§ 1 und 9 Abs. 1 SGB VII in Verbindung mit Nr. 4101 der Anlage 1 zur Berufskrankheitenverordnung [1] haben die Träger der gesetzlichen Unfallversicherung die Quarzstaublungenerkrankung (Silikose) bei Vorliegen der gesetzlichen Voraussetzungen als Berufskrankheit anzuerkennen, gegebenenfalls Heilbehandlung zu gewähren und eventuell die durch die Berufskrankheit entstandene Minderung der Erwerbsfähigkeit (MdE) durch Geldleistungen zu entschädigen.
Aufgabe der medizinischen Begutachtung ist es dabei insbesondere, die Berufskrankheit zu diagnostizieren, die von ihr bedingten Funktionseinschränkungen zu ermitteln und Vorschläge zur Minderung der Erwerbsfähigkeit (MdE) sowie ggf. zur Heilbehandlung zu machen.
Die rechtliche Definition der Berufskrankheit nach Nr. 4101 und deren Auslegung, u.a. definiert durch das Merkblatt für die ärztliche Untersuchung (Bekanntmachung des BMAS, zuletzt vom 05.02.1998; BArbBl 1998 H. 4 S. 61 [4]) sowie durch die Rechtsprechung, bestimmt den sozialrechtlichen Umfang des Schutzbereichs der gesetzlichen Unfallversicherung und so der anerkennungsfähigen unmittelbaren und mittelbaren Erkrankungsfolgen in Abgrenzung zu nicht arbeitsbedingten Erkrankungen. Dabei sind die aktuellen Erkenntnisse der medizinischen Wissenschaft ebenso zu beachten wie die Abgrenzung und die Wechselwirkungen zu anderen Berufskrankheiten der Berufskrankheitenliste (z. B. BK Nrn. 4102, 4111, 4112).
Der in dieser Leitlinie verwendete Begriff „Quarzstaublungenerkrankung“ inkludiert neben der klassischen Silikose auch die sog. Kohlenbergarbeiterlunge („coal worker’s pneumoconiosis“) und die Quarzstaublungenerkrankungen durch andere silikogene Stäube wie Cristobalit und Tridymit.
Die Aktualisierung dieser Leitlinie erfolgt unter Berücksichtigung der seit der initialen Fassung von 2008 publizierten klinisch-wissenschaftlichen Arbeiten zur Diagnostik und Begutachtung der Quarzstaublungenerkrankung.
3.2 Versicherte Einwirkung (typische Exposition)
Aus dem Begriff „Quarzstaublungenerkrankung“ ergibt sich, dass als BK-Nr. 4101 nur solche Krankheitserscheinungen als Berufskrankheit anzuerkennen sind, die durch die inhalative Einwirkung von Staubgemischen mit unterschiedlich hohen Anteilen von alveolengängigen Quarz-, Cristobalit- oder Tridymitstaubpartikeln bedingt sind. Dabei ist das Risiko der Erkrankung abhängig von der Staubkonzentration in der Atemluft, dem Anteil der alveolengängigen Staubfraktion, dem Gehalt an freier kristalliner Kieselsäure (SiO 2 ), der Art der Begleitstäube, der Expositionsdauer, der individuellen Suszeptibilität auf die freie kristalline Kieselsäure und der Reinigungsfähigkeit der Lunge.
Bei der Prüfung, ob die medizinischen Voraussetzungen der BK Nr. 4101 bejaht werden können, sind dann die unmittelbaren oder mittelbaren Wirkungen dieses Anteils kristalliner Kieselsäure festzustellen und zu bewerten, seien sie für diese nun allein ursächlich oder wesentlich teilursächlich. Bei der Abgrenzung ist auch die Art der anderen Staubanteile, z. B. des Steinkohlenstaubs, zu beachten.
Art, Umfang und Dauer der Staubexposition und die Arbeitsplatzverhältnisse sind im Feststellungsverfahren durch die Unfallversicherungsträger sowie durch eine qualifiziert erhobene Arbeitsanamnese des ärztlichen Sachverständigen bestmöglich zu rekonstruieren und bei Prüfung der kausalen Zuordnung der festgestellten Krankheitserscheinungen zur BK-Nr. 4101 zu berücksichtigen.
Neben Beschäftigungen im Steinkohlen- und dem Erzbergbau sind u. a. auch sehr unterschiedlich gefährdende Beschäftigungen im Bereich der Steinbruch-, keramischen und Glasindustrie, in der Stahl- und Eisenindustrie, in Gießereien und im Tunnelbau, bei der Steinbearbeitung, bei der Bearbeitung von quarzhaltigen Werkstoffen, z. B. in Dentallaboren, und in der chemischen Industrie zu beachten. Dabei können sich die Expositionen in Art und Umfang erheblich unterscheiden.
Bei multifaktoriellen Einwirkungen und Ursachen berufskrankheitenrechtlich versicherter und unversicherter Art ist mit dem Grad hinreichender Wahrscheinlichkeit festzustellen, inwieweit die versicherte Einwirkung zumindest rechtlich wesentlich an den Erkrankungsfolgen mitgewirkt hat (siehe 3.3.2).
3.3 Rechtliche Definitionen und Tatbestandsmerkmale
3.3.1 Tatbestandsmerkmale der BK Nr. 4101
Die Anerkennung eines Versicherungsfalls der BK Nr. 4101 kann nur dann empfohlen werden, wenn alle Tatbestandsmerkmale der Berufskrankheit erfüllt sind.
Die Feststellungen, ob der Erkrankte versicherte Person ist, eine versicherte Tätigkeit ausgeübt hat und infolge dieser silikogenen (quarzhaltigen) Stäuben ausgesetzt war, sind als Vorfragen der Begutachtung durch den beauftragenden Unfallversicherungsträger zu klären. Wenn die arbeitstechnischen Voraussetzungen bejaht werden, ist im nächsten Schritt das Vorliegen der medizinischen Voraussetzungen zu prüfen.
Die in der BK-Liste bezeichnete Erkrankung, die Quarzstaublungenerkrankung, die im Klammerzusatz als „Silikose“ bezeichnet wird, muss gegeben sein.
Ist aus ärztlicher Sicht der Versicherungsfall einer BK Nr. 4101 zu bejahen, ist umfassend festzustellen, ob durch die schädigende Einwirkung der quarzhaltigen Stäube Gesundheitsstörungen verursacht worden sind. Ist dies der Fall, kommen, abhängig vom Ausmaß der Störungen, Leistungen aus der gesetzlichen Unfallversicherung wie Heilbehandlung und Rente in Betracht (sog. Leistungsfall).
3.3.2 Kausalitätsgrundsätze
Durch die nachfolgend dargestellten Kausalitätsgrundsätze wird der rechtliche Schutzbereich der gesetzlichen Unfallversicherung definiert. Das Kausalitätsprinzip ist tragendes Element des Sondersystems der gesetzlichen Unfallversicherung, das sich als System der Unternehmerhaftung wesentlich von der gesetzlichen Krankenversicherung unterscheidet.
Anzuerkennen und zu entschädigen sind nur solche Gesundheitsstörungen, die wesentlich ursächlich oder mitursächlich durch die schädigende Einwirkung (§ 9 Abs. 1 S. 1 SGB VII „infolge“) verursacht worden sind.
Dabei kann unfallversicherungsrechtlich nie kausal sein, was nicht auch im Sinne der naturwissenschaftlichen Kausalität ursächlich ist. Kommen mehrere Ursachen naturwissenschaftlich in Betracht, so sind nur die Ursachen als rechtserheblich anzusehen, die wegen ihrer besonderen Beziehung zum Erfolg zu dessen Eintritt wesentlich beigetragen haben. Haben mehrere Ursachen zu einem Erfolg (Schaden) beigetragen, so kann es mehrere rechtlich wesentliche Mitursachen geben. Es wird dann von einer sog. konkurrierenden Kausalität gesprochen. Diese setzt jedoch nicht voraus, dass die Bedingungen „gleichwertig“ oder „annähernd gleichwertig“ sind. Auch eine nicht annähernd gleichwertige, sondern rechnerisch verhältnismäßig niedriger zu bewertende Ursache kann für den Erfolg rechtlich wesentlich sein, solange die andere(n) Ursache(n) keine überragende Bedeutung haben. Ist jedoch eine der Bedingungen oder sind mehrere Bedingungen gemeinsam gegenüber einer anderen von überragender Bedeutung, so ist oder sind nur die erstgenannte(n) Bedingung(en) „wesentlich“ und damit Ursache(n) im Sinne des Sozialrechts (BSGE 12, 242, 245 ff. [5]). Die andere (naturwissenschaftliche) Ursache, die nicht als „wesentlich“ anzusehen ist und damit als Ursache nach der Theorie der wesentlichen Bedingung und im Sinne des Sozialrechts ausscheidet, wird meist als sog. „Gelegenheitsursache“ oder Auslöser bezeichnet [6]. Insoweit ist eine wertende Gegenüberstellung der ursächlichen Faktoren erforderlich (vgl. beispielhaft Landessozialgericht Baden-Württemberg v. 13.12.2007, L 6 U 2016/03, m. w. N.).
Wirken danach mehrere Ursachen wesentlich gemeinsam, so ist zu prüfen, ob eine dieser Ursachen dem versicherten Bereich zuzurechnen ist. Diese ist dann zumindest Teilursache im Rechtssinn und führt zur Bejahung der unfallversicherungsrechtlichen Kausalität. Stehen eine oder mehrere Ursachen aus dem unversicherten Bereich (z. B. Begleiterkrankungen, andere, unversicherte, schädigende Einwirkungen) ganz im Vordergrund (in der Terminologie des BSG: haben sie überragende Bedeutung) und ist der versicherte Bereich nicht rechtlich wesentlich (s. o.), verdrängen die unversicherten Einwirkungen die versicherte Einwirkung rechtlich als Ursache, die unversicherten Einwirkungen sind dann die allein wesentlichen Ursachen. Ein Versicherungsfall/Leistungsfall kann dann mangels Kausalität nicht vorliegen.
Angesichts des röntgenmorphologisch weitgehend charakteristischen Erscheinungsbildes der Silikose ist die kausale Zuordnung fibrosierender Veränderungen auf die Einwirkung quarzhaltiger Stäube einfacher als die kausale Zuordnung sonstiger Störungen der Atmung. Diese sind bei der Beurteilung im o.a. Sinne im Einzelnen sorgfältig wertend zu beachten.
3.3.3 Beweisgrundsätze
Die Tatbestandsmerkmale „versicherte Person“, „versicherte Tätigkeit“, „schädigende Einwirkung“, „Erkrankung“ bzw. „Gesundheitsschaden“ müssen im sog. Vollbeweis (mit an Sicherheit grenzender Wahrscheinlichkeit) nachgewiesen sein: Es darf also kein vernünftiger Zweifel darüber bestehen, dass die Tatsachen vorliegen.
Dies ist insbesondere für die Diagnostik des Gesundheitsschadens von Bedeutung. Liegt nur ein Verdacht auf einen Schaden vor, muss dieser durch weitere Untersuchungen erhärtet werden; ansonsten ist er außer Betracht zu lassen. Liegen schwankende und/oder grenzwertige Befunde vor, müssen die Untersuchungen – evtl. auch in zeitlichem Abstand – wiederholt werden.
Für die Bewertung der Ursachenzusammenhänge, insbesondere den Zusammenhang zwischen schädigender Einwirkung und Gesundheitsschaden, ist hinreichende Wahrscheinlichkeit erforderlich. Hinreichende Wahrscheinlichkeit bedeutet im rechtlichen Sinne, dass bei Abwägung aller Umstände den für die Bejahung des Zusammenhangs sprechenden Umständen ein deutliches Übergewicht zukommt, auf das die Überzeugung gegründet werden kann. Ein Kausalzusammenhang ist insbesondere nicht schon dann wahrscheinlich, wenn er lediglich nicht auszuschließen oder nur möglich ist. Die Tatsachen, auf denen die ärztliche Überzeugung gründet, sind zu benennen.
Bleibt ein Tatbestandsmerkmal beweislos oder ist ein Ursachenzusammenhang nicht hinreichend wahrscheinlich zu machen, geht dies nach dem auch im Sozialrecht geltenden Grundsatz der materiellen Beweislast zu Lasten der versicherten Person, die sich zur Begründung ihres Entschädigungsanspruchs auf diese Tatsachen und Zusammenhänge stützt. Ein Grundsatz „Im Zweifel für den Versicherten“ besteht nicht.
3.4 Verwaltungsverfahren und Begutachtung
Der Unfallversicherungsträger ist als Auftraggeber verpflichtet, eine sachgerechte Begutachtung zu gewährleisten. Der Auftrag muss klar formuliert sein. Dem Gutachter sind die notwendigen Vorinformationen zur Verfügung zu stellen. Dazu gehören insbesondere Unterlagen zur Krankheitsvorgeschichte und zu Erkrankungen, die in einer Beziehung zu der zu begutachtenden Krankheit stehen könnten, die Befunde der arbeitsmedizinischen Vorsorgeuntersuchungen sowie vollständige problemorientierte Ermittlungen zur Arbeitsvorgeschichte mit Angaben zur Dauer und Intensität relevanter Einwirkungen (siehe 6.1.)
Hinsichtlich allgemeiner Grundlagen der Begutachtung von Berufskrankheiten – einschließlich Maßnahmen der Qualitätssicherung und sonstiger Voraussetzungen – wird auf die Empfehlungen der Unfallversicherungsträger zur Begutachtung bei Berufskrankheiten verwiesen [7], die in Zusammenarbeit mit der Bundesärztekammer und zahlreichen wissenschaftlichen Fachgesellschaften entwickelt wurden. Dies gilt wegen der hohen Qualitätsstandards insbesondere für die „Checkliste Expositionsermittlungen“ und die Ermittlungen zur „Qualitätssicherung Arbeitsplatzstellungnahme“.
4 Klinischer und wissenschaftlicher Kenntnisstand zu den Fragen der Begutachtung der BK Nr. 4101
4.1 Medizinische Definition des Krankheitsbildes
Morphologische Veränderungen der Lungen durch die Inhalation anorganischer Mischstäube werden als Pneumokoniosen bezeichnet [8]. Je nach Zusammensetzung des Staubes sind Pneumokoniosen gekennzeichnet durch a) diffuse oder knotige Bindegewebsbildung, b) entzündliche Prozesse und c) Ablagerung des Staubes [8].
Man unterscheidet zwischen der Quarzstaubsilikose, die durch Einatmen von nahezu reinem Quarzstaub entsteht und den Mischstaubsilikosen, die durch Inhalation von Staubgemischen entstehen, die neben Quarz noch andere Bestandteile enthalten.
Die häufigste Mischstaubsilikose ist die Anthrakosilikose des Bergmanns vor Kohle. Der sog. Kohlengrubenstaub stellt ein hochkomplexes Gemisch verschiedener Mineralien und Zuschlagstoffe (Baustoffe etc.) dar. Er enthält den wegen seiner Zelltoxizität besonders gefährlichen Quarzstaub in unterschiedlichen Prozentanteilen. Je nach mineralogischer Beschaffenheit der Deckgebirge, des Inkohlungsgrades, der verwendeten Gewinnungsverfahren und des Einsatzes anhydrit- und zementhaltiger Dämmbaustoffe befinden sich im Kohlengrubenfeinstaub darüber hinaus variable Anteile nichtkohlenstoffhaltiger Staubfraktionen. So besteht etwa der (nichtkohlenstoffhaltige) nicht-veraschbare Staubanteil der Kohle im Ruhr- und Saarkarbon im Wesentlichen aus Tonmineralien, Sulfiden, Karbonaten und Quarz (siehe 4.2).
International wird der Begriff „Silikose“ nur für Pneumokoniosen, die durch kristalline hoch kieselsäurehaltige Staubarten hervorgerufen werden, verwendet, während die Pneumokoniose der Kohlenbergarbeiter als Mischstaub-Pneumokoniose bzw. „coal workers’ pneumoconiosis“ bezeichnet wird [9]. Im Folgenden wird dem deutschen Berufskrankheitenrecht entsprechend sowohl die „reine“ Silikose als auch die Pneumokoniose des Kohlenbergarbeiters unter dem Begriff Silikose subsummiert.
Die Silikose wird meist primär durch das Röntgenbild der Lungen erkannt. Charakteristisch sind disseminierte, mehr oder minder rundliche Verschattungen unterschiedlicher Größe und Dichte, evtl. mit zusätzlichen größeren sog. Schwielenbildungen, vorwiegend lokalisiert in den Ober- und Mittelfeldern, evtl. konfluierend und/oder zerfallend. Die Befundung der Thoraxübersichtsaufnahme ist nach der Staublungenklassifikation der ILO [2] standardisiert [10].
Eine Silikose kann auch primär durch einen computertomographischen oder semiquantitativen makroskopischen und histologischen Befund definiert werden [11]. Die diagnostischen Kriterien für die einzelnen Verfahren werden im Abschnitt 6.2 dargestellt.
Wird zur Befundung nur die Thoraxübersichtsaufnahme herangezogen, bleiben wichtige Aspekte außer Acht:
- die geringe Sensitivität und Spezifität des konventionellen Röntgenbildes für kleine rundlichen Verschattungen. Insbesondere bei niedrigen Streuungskategorien wird anhand der Thoraxübersichtsaufnahme in bis zu 30 % der Fälle ein falsch-positiver wie auch falsch-negativer Befund erhoben (siehe 4.4 [12, 13, 14, 11]).
- die Vernachlässigung weiterer morphologischer Veränderungen der Lungen bei Silikose, insbesondere des Lungenemphysems; dieses kann insbesondere in frühen Stadien nicht mit ausreichender Sensitivität durch das konventionelle Röntgenbild diagnostiziert werden.
- die mangelhafte Korrelation zwischen röntgenmorphologischen Befunden und pulmokardialen Funktionsausfällen.
Diese Gesichtspunkte sollten im Rahmen der Diagnostik und Begutachtung der Silikose unbedingt beachtet werden.
Bei der Quarzstaublungenerkrankung sind häufig auch die Hiluslymphknoten, gelegentlich auch die Mediastinallymphknoten mit betroffen, wobei keine enge Korrelation zur Schwere des Lungenbefalls besteht. Ausgedehntere konglomerierende und indurierende Lymphknotenprozesse können zu Dislokationen der Hili mit Rückwirkungen auf die großen Bronchien und Gefäßstämme führen. Durch Wandeinbrüche können Stenosen, in den Gefäßen auch örtliche Thrombosen entstehen. Poststenotisches Emphysem oder Bronchiektasen, ggf. auch trophische Störungen im Lungengewebe durch Einmauerung von Nerven kommen als Folgen vor. Vorwiegend randständige schalenförmige Lymphknotenverkalkungen kennzeichnen röntgenologisch den „Eierschalenhilus“ [15].
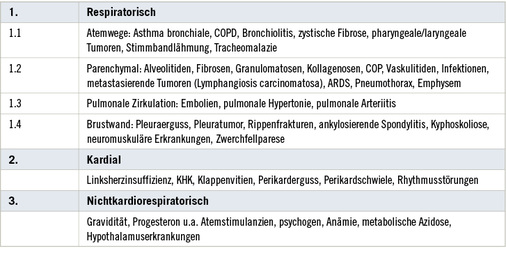
Fortgeschrittene Quarzstaublungenerkrankungen gehen mit einer respiratorischen Insuffizienz einher, in deren Folge eine pulmonale Hypertonie und ein Cor pulmonale mit Zeichen der Rechtsherzinsuffizienz auftreten können [8, 16, 17].
Selten ist die Quarzstaublunge mit rheumatischen Affektionen (Caplan-Syndrom) und anderen kollagenen Erkrankungen (u. a. Sklerodermie) vergesellschaftet. Beim Caplan-Syndrom treten neben einer rheumatoiden Arthritis auch sog. Rheumaknoten, rundliche Verschattungen in der Lunge, auf. Der zugrunde liegende Pathomechanismus der vorgenannten koinzidierenden Erkrankungen konnte bislang nicht geklärt werden. McCormic und Mitarbeiter [18] konnten in ihrer Metaanalyse zum Risiko einer Quarzexposition für die Sklerodermie 16 Studien einschließen, davon 3 Kohortenstudien und 9 Fall-Kontrollstudien. Es zeigte sich eine hohe Heterogenität (I 2 von 97 %!), d. h. die Ergebnisse der einzelnen Studien waren sehr unterschiedlich. Das Ausmaß der Korrelation von Quarzexposition und Auftreten einer Sklerodermie, das für Männer mit 3,2 [95 % Konfidenzintervall: 1,24–7,35] über alle Studien berechnet wurde, kann demzufolge nicht als abschließend gesichert gelten. McCormick et al. heben hervor, dass bei Berücksichtigung nur der Fall-Kontoll-Studien die Risikoerhöhung mit 2,24 [95 % KI 1,65–3,31] ohne signifikante Heterogenität und bei Berücksichtigung nur der Kohortenstudien mit 15,49 [95 % KI 4,54–52,78] mit signifikanter Heterogenität berechnet wurde.
In ihrer Schlussfolgerung äußern sich McCormick et al. entsprechend: Die Ergebnisse legen nahe („suggest“), dass Quarzexposition ein relevanter Risikofaktor für die Entwicklung einer Sklerodermie vor allem bei Männern ist. Sie schreiben aber abschließend auch: Es braucht weitere Beobachtungsstudien, die die Rolle der beruflichen Siliciumdioxid-Exposition im Kontext anderer Risikofaktoren untersuchen (s. auch Diskussion der Arbeit).
Für die anderen angeführten Erkrankungen liegen aktuell keine umfangreichen, einen kausalen Zusammenhang stützenden Untersuchungen vor.
Die Quarzstaublungenerkrankung geht mit einem erhöhten Lungenkrebsrisiko einher (s. hierzu BK Nummer 4112) [19].
Wenn bei einem Versicherten mit einer BK 4101 eine Lungenkrebserkrankung auftritt, ist ein begründeter Verdacht auf eine BK 4112 zu äußern und eine Berufskrankheitenverdachtsanzeige zu stellen.
Für die Entwicklung eines primären Lungenkarzinoms aus einer quarzbedingten hyalinen Narbe oder einer Mischstaubschwiele, einem so genannten silikotischen Narbenkarzinom, gibt es keine morphologischen Belege. Zu überprüfen ist aber im Einzelfall, ob indirekte kausale Beziehungen zwischen der Lungenkrebserkrankung und (anthrako-)silikotischen Schwielen derart bestehen, dass ggf. die Pneumokoniose zur zeitlichen Verzögerung der Lungenkrebsdiagnose und/oder -therapie geführt hat oder ob die vorbestehende Pneumokoniose eine Operation, den Krankheitsverlauf und/ oder die Durchführung einer intensiven Tumortherapie negativ beeinflusst hat [20].
4.2 Pathologische Anatomie der Silikose
Ätiopathologisch handelt es sich bei der Silikose um eine durch Inhalation quarzhaltiger, alveolengängiger Mischstäube induzierte Pneumokoniose, wobei Quarz und seine Hochtemperatur-Modifikationen (Cristobalit und Tridymit) eine fibrogene Wirkung aufweisen [21, 22].
Als ursächlich werden u.a. bestimmte Oberflächeneigenschaften der SiO 2 -Kristalle diskutiert: Durch die Halbleitereigenschaften soll ein Elektronentransfer zwischen Kristalloberfläche und Phagolysosomenmembran stattfinden, was zu einer Freisetzung lytischer Enzyme, zur Zytotoxizität und zum Zelltod führt. Andere Autoren stellen die pathogene Wirkung der Siliziumkristalle mit Eiweißabsorption und Denaturierung an der Kristalloberfläche in den Vordergrund [23–25].
Die silikogenen Staubpartikel gelangen in den Alveolarbereich und werden dort von Makrophagen phagozytiert. Sie penetrieren zum Teil in das Lungeninterstitium und werden u. a. in die Lymphknoten weitertransportiert. Initialstadium ist eine makrophagozytäre Entzündungsreaktion mit sekundärer interstitieller Fibrosierung. Das klassische Silikosegranulom besteht aus einem mehr oder weniger konzentrisch geschichteten Zentrum aus zwiebelschalenartig gelagerten Kollagenfasern, umgeben von einem lockeren Staubzellsaum, welcher durch die o. g. Mechanismen über einen Recyclingprozess freigesetzter Kristalle die „Wachstumszone“ des Granuloms darstellt [26, 27]. Dieser Aspekt erklärt das Fortschreiten der Silikose auch nach Ende der Exposition, z. B. nach Abkehr von der Untertagetätigkeit.
Histologisch lässt sich in Granulomen kristalline Kieselsäure (Quarzpartikel) nachweisen. Die einzelnen Granulome können zu größeren Schwielen konfluieren.
Die Ausprägung der silikotischen Veränderungen wird pathologisch-anatomisch meist in drei [8] oder vier verschiedene Schweregrade eingeteilt [13]; (vgl. auch Beispiel in Tabelle 10). Hierzu wird das expandierte formalinfixierte Lungengewebe in max. 10 mm dicke Scheiben transversal lamelliert, palpatorisch die Anzahl von Silikose- (verdächtigen) Knötchen ermittelt und anhand von mindestens 6 Paraffineinbettungen (Paraffinblöcken) histopathologisch untersucht [13, 11]. Dieses Vorgehen empfiehlt sich auch zum Silikose-Grading von Lungenresektaten. Die Schwielen können zentral durch ischämische Nekrosen erweichen [8].
Wenn Verkalkungen von Lymphknoten auftreten und/oder in Folge des lymphogenen Transportes hiläre und mediastinale Lymphknoten verkalken, wird von einer „Eierschalensilikose“ gesprochen [16].
Gegenüber der „reinen“ Silikose bei sehr hohem Quarzanteil des alveolargängigen Staubes, z. B. bei Sandstrahlern, werden die Veränderungen des Lungenparenchyms bei Mischstaub-Pneumokoniosen wesentlich durch die Begleitstäube mitgeprägt. Bei den weitaus meisten der in unseren Breiten beobachteten „Silikosen“ handelt es sich tatsächlich um Mischstaub-Pneumokoniosen, d. h. dass der inhalierte Staub neben kristalliner Kieselsäure in qualitativ und quantitativ unterschiedlichem Ausmaß mineralogisch weitere Bestandteile enthält.
Das Nebengestein der Steinkohle des westdeutschen Oberkarbons setzt sich vorwiegend aus den Gesteinsarten Schieferton, Sandschieferton und Sandstein sowie untergeordnet aus Konglomerat, Toneisenstein, Tonstein und Quarzit zusammen [28, 29]. Im Steinkohlenbergbau des Ruhrgebiets beträgt der Quarzanteil bis zu 7 %, im Saarland bis zu 16 %, während Stäube in der Stein- und Bauindustrie 30–80 % Quarz enthalten.
Quarzhaltige Stäube werden u.a. inhaliert bei Exposition gegenüber Granit, Sandstein, Erzgesteinen, Kohlengesteinen, Bauxit, Schamottsteinen, Porzellanstäuben, Schlackeprodukten, Glasschmelzen, Gießereistäuben etc. (siehe Merkblatt zur BK Nr. 4101 und [28]).
Diese unterschiedliche Staubzusammensetzung findet ihren Niederschlag in der pathologischen Anatomie dergestalt, dass sich in der Begutachtung auch ohne Kenntnisse der arbeitstechnischen Daten oftmals allein aufgrund der Morphologie der pneumokoniotischen Herde bereits Rückschlüsse auf die zugrunde liegende Noxe ableiten lassen und pathologisch-anatomisch oftmals berufsspezifische Befunde aufgezeigt werden können [30]. So zeigen z. B. die Granulome der Erzbergbauarbeiter aufgrund des Anteils an Eisenoxid eine braunrote Farbe. Erwähnt sei ferner die sog. Ockerstaublunge, deren gelbliche Färbung vom Anteil inhalierten Eisenoxidhydrates herrührt.
Derartige berufsgruppenbezogene Besonderheiten zeigen sich auch bei der sog. „coal worker’s pneumoconiosis“, der eigentlichen Mischstaubpneumokoniose der Bergarbeiter im Steinkohlenbergbau unter Tage. Stellen sich bei nahezu reiner oder überwiegender Quarzstaubbelastung die Herde silbrig bis schieferfarben dar, so entwickeln sich mit abnehmendem Quarz- und zunehmendem Kohlenstaubanteil zunehmend matt- bis tiefschwarze Knötchen oder Granulome, wie dies bei den Bergleuten im Ruhrkohlenbergbau unter Tage in klassischer Weise der Fall ist.
Das radiologische Bild lässt demgegenüber keine zuverlässigen Rückschlüsse auf die Zusammensetzung des inkorporierten Staubes zu.
Funktionelle Auswirkungen der Silikose beruhen vor allem auf sekundären Prozessen wie beispielsweise unterschiedlichen Formen des Emphysems [8, 31, 32]. Klassisches Beispiel ist das perinoduläre Traktionsemphysem oder fokale Narbenemphysem, dessen morphologisches Korrelat ein zentrales Granulom mit zentripetal darauf zulaufenden Resten alveolären Parenchyms ist, was zu dem viel zitierten Vergleich mit der „Spinne im Netz“ führte. Zu einer weiteren funktionellen Auswirkung kann es ferner durch Induktion oder Verschlimmerung einer chronischen (obstruktiven) Bronchitis oder von Bronchiektasen kommen.
Gelegentlich lassen sich im Rahmen der Begutachtung nur pathologisch-anatomisch diagnostizierbare Silikose-/Mischstaubpneumokoniose-induzierte pulmonale Läsionen beobachten. Ein Beispiel hierfür ist die sog. „Schwarze Löcherlunge“, deren morphologisches Korrelat ein massives Staubemphysem mit z. T. diffuser kleinknotiger Anthrakose und Anthrakofibrose in Kombination mit einer zumeist disseminierten Ablagerung anthrakotischen Pigmentes in den Alveolarsepten darstellt. Bei diesem Krankheitsbild handelt es sich um eine Besonderheit nach Inhalation von stark kohlenhaltigen Stäuben mit nur geringem Quarzanteil sowie daraus resultierender nahezu fehlender Granulombildung.
Eine weitere zum Teil nur mikroskopisch zu klärende Sonderform stellt die interstitielle disseminierte feinherdige Silikose (pinhead/Körnertyp) dar, welche klinisch zumeist als unspezifische interstitielle Lungenfibrose imponiert. Feingeweblich lassen sich jedoch im Bereich der fibrotisch verbreiterten Septen in wechselndem Ausmaß, teils frei im Interstitium, teils in Makrophagen gebunden, Staubablagerungen belegen, wobei die Beurteilung im polarisierten Licht eine zuverlässige semiquantitative Bewertung der inkorporierten polarisationsoptisch doppelbrechenden Quarzkristalle erlaubt.
4.3 Studienlage zu Lungenfunktionseinschränkungen
4.3.1 Einschränkungen in Abhängigkeit von der kumulativen Belastung gegenüber silikogenen Stäuben
In vielen Studien werden allgemein die Zusammenhänge zwischen Expositionen gegenüber quarzstaubhaltigen Stäuben und bestimmten Gesundheitsstörungen und Lungenfunktionseinschränkungen untersucht, ohne zu unterscheiden, ob eine Quarzstaublungenerkrankung im Sinn der BK Nr. 4101 (vgl. 4.1, 4.2) radiologisch objektiviert wurde. Da die Studien Probanden mit und ohne radiologisch belegte Quarzstaublungenerkrankung umfassen, können ihre Ergebnisse nur bedingt auf die BK-Nr. 4101 bezogen werden. Sie enthalten Aussagen zu den Gesundheitsstörungen, die allgemein bei Probanden mit Quarzstaubexposition beobachtet werden, wobei berücksichtigt werden muss, dass wie unter 4.4 näher ausgeführt, der Großteil der langjährig gegenüber quarzhaltigen Stäuben Exponierten pathologisch-anatomisch silikotische Veränderungen aufweist und in tabula die Voraussetzungen der BK Nr. 4101 erfüllt.
Es besteht in diesen zusammengefassten Untersuchungen trotz Healthy-worker-Effekten konsistent eine positive Assoziation zwischen der kumulativen Belastung gegenüber silikogenen Stäuben einerseits und der Häufigkeit einer COPD sowie obstruktiven und restriktiven Lungenfunktionseinschränkungen andererseits (Übersichten bei [33–37]. Dies betrifft sowohl den Steinkohlenbergbau [38–55] als auch andere Arbeitsbereiche mit wesentlicher Exposition gegenüber silikogenen Stäuben [56–64]. Dieser Zusammenhang ist ohne Berücksichtigung des Befundes der Thoraxübersichtsaufnahme v. a. in den umfassenden Studien von Marine et al. [41] und der DFG [28, 65, 29, 66] sowie von Collins et al. [42], Rogan et al. [67], Seixas et al. [38, 68] und Hnizdo [56 ] wiedergegeben. Nach Seixas et al. [38] beträgt der FEV 1 -Verlust bei Feinstaubbelastung im US-amerikanischen Steinkohlenbergbau pro mg/m 3 und Jahr – 5,5 mL, nach Attfield [141] – 2,5 mL (ähnlich auch nach Collins et al. [42]; s. unten).
Ein großer Teil der vorgenannten Studien berücksichtigt das Zigarettenrauchen und weist sowohl unter Rauchern als auch Nichtrauchern negative Auswirkungen der Belastung gegenüber silikogenen Stäuben mit signifikanten Lungenfunktionseinschränkungen nach (siehe diesbezüglich auch Übersichten von Oxman et al. [37] und Gamble et al. [69].
Eine Risikoverdopplung der COPD des Nierauchers ergibt sich im Steinkohlenbergbau bei einer kumulativen Belastung von etwa 100 Feinstaubjahren [70]. Für den Raucher liegt die entsprechende Kohlengrubenfeinstaubdosis um 20 bis 60 % höher. Auf die entsprechenden Befunde von Marine et al. [41], Lange und Ulm [71], Lange und Pache [72], Attfield u. Hodous [54] sowie Collins et al. [42] stützt sich die Wissenschaftliche Begründung der BK Nr. 4111 [70]. Collins et al. [42] beobachten einen FEV 1 -Abfall von 0,156 L (0,164 L (Raucher) bzw. 0,118 L (Nichtraucher) sowie einen VC-Verlust von 0,151 L pro 100 gh/m 3 (entsprechend 57 Feinstaubjahren). Legt man eine durchschnittliche Kohlengrubenfeinstaubkonzentration von 4 mg/ m³ zu Grunde, ergibt sich für den Nieraucher ein dadurch bedingter jährlicher FEV 1 - und VC-Verlust von je ca. 10 mL pro Jahr. Sircar et al. [73] geben den FEV 1 -Abfall des Rauchers mit 0,052 L/ Jahr und des Nierauchers mit 0,038 L/Jahr an, wobei ab einem Abfall von 60 mL/Jahr eine erhöhte Mortalität festzustellen war. Letzterem entsprechend beschreiben Kuempel et al. [74] und Attfield et al. [75] nach Raucherjustierung eine positive Korrelation der COPD-Mortalität mit der kumulativen Staubexposition unter US-amerikanischen Kohlengrubenarbeitern.
In Goldminen wurden, bezogen auf die Lungenfunktionsänderung, unter Rauchern und Nierauchern gleichartige Effekte infolge der quarzreichen Staubexposition beobachtet. Allerdings waren die Lungenfunktionsveränderungen 3fach höher als unter Steinkohlenbergleuten [37]. Eine kumulative Dosis des quarzreichen Staubs von 14,6 gh/m³ (Produkt aus mittlerer Konzentration in g/m 3 und Expositionsdauer in h) verursachte hier FEV 1 - und FVC-Verluste in Höhe von 236 bzw. 217 mL unter Nierauchern und von 552 bzw. 335 mL unter Rauchern. Bei 30 Packyears ließen sich 30 % der Funktionseinbußen auf die Staubbelastung, 70 % bzw. 64 % auf das Zigarettenrauchen zurückführen [56].
4.3.2 Einschränkungen bei Vorliegen einer Silikose
Baur [76] und Baur et al. [35] haben die wichtigsten Studien zur Lungenfunktion bei unterschiedlichen Formen der Quarz- bzw. Mischstaubexposition zusammengestellt. In beiden Übersichten wurde die Schlussfolgerung gezogen, dass bei langjähriger Einwirkung von Mischstäuben, die freie kristalline Kieselsäure enthalten, ein erhöhtes Risiko für die Verursachung einer chronischen Bronchitis, eines Lungenemphysems und silikotischer Läsionen mit unterschiedlichen Störungen der Lungenfunktion besteht.
In dieser Leitlinie wird spezifisch darauf eingegangen, welche konkreten Gesundheitsstörungen und Einschränkungen auf das Krankheitsbild der Quarzstaublungenerkrankung im Sinne der BK Nr. 4101 (siehe 4.1, 4.2) zurückzuführen sind.
Im Folgenden wird das Ergebnis einer Literaturrecherche dargestellt, in der nur die für die Fragestellung relevanten Arbeiten mit Klassifikation der radiologischen Befunde und Lungenfunktionsprüfung sowie einer Mindestfallzahl von n = 50 eingeschlossen wurden.
Methodik
Die Datenbank „PubMed“ wurde nach den Begriffen „silicosis“, „pneumoconiosis“, „coal“ oder „foundry“, in Kombination mit „lung function“ durchsucht. Darüber hinaus wurde die ältere Literatur aufgrund eigener Literaturrecherchen erarbeitet. Es wurden insgesamt 314 Arbeiten erfasst.
Die Klassifikation der Pneumokoniosen erfolgt nach der den meisten Studien zugrunde liegenden ILO 1980; bei Verwendung älterer Klassifikationen (1930, 1958/1968/1971) wurden die Daten nach der ILO 1980 neu bewertet, soweit dies möglich ist ( Tabelle 1 ) [31]. Nicht in allen Studien wurden die Lungenfunktionsdaten für alle Streuungskategorien detailliert dargestellt, sondern teilweise – und in unterschiedlicher Weise – zusammengefasst. Bei der Auswertung der neueren Literatur für diese aktualisierte Übersicht wurde auf eine möglichst genaue Zuordnung zu der Klassifikation nach ILO 1980 bzw. ILO 2000 [2], ILO 2000D und ICOERD geachtet.
Qualität der Studien
Einige der hier berücksichtigten Publikationen sind älteren Datums und haben gewisse Schwächen. Dies betrifft die mangelhafte Definition der untersuchten Kollektive ebenso wie die fehlende Publikation der Streuung der Daten. Auch sind die funktionellen Befunde nicht einheitlich auf die (gleichen) Lungenfunktionssollwerte bezogen worden. Statistische Angaben fehlen oft. Da die Ergebnisse der Studien trotz ihrer methodischen Schwächen weitgehend widerspruchsfrei sind, erschien eine Einbeziehung dennoch gerechtfertigt.
Resultate
In den Tabellen 2–9 werden die in dieser Übersicht erfassten Studien mit Angaben zu Lungenfunktion und Röntgenbefund zusammenfasst. Es liegen weitere Studien zur Thematik vor, die zum Teil im Text erwähnt werden. Diese wurden in die detaillierte Auswertung nicht mit einbezogen, da ihre methodischen Schwächen über die der anderen Studien hinausgehen. Von Bedeutung ist, dass diese nicht berücksichtigten Studien im Ergebnis zu keinen anderen Schlüssen führen würden.
Steinkohlenbergbau: Nachfolgend werden 13 Untersuchungen bei Kohlenbergarbeitern in der Reihenfolge ihrer Publikation vorgestellt (s. Tabelle 2).
Carstens et al. [55] stellten – wie auch Hnizdo [56] und andere Untersucher – einen Healthy-worker-Effekt schon zu Beschäftigungsbeginn der Bergleute fest (diese wiesen überdurchschnittlich gute Lungenfunktionswerte auf). Im Laufe des Arbeitslebens zeigten Steinkohlenbergleute erhebliche Lungenfunktionsstörungen, die nicht an die Diagnosen Silikose und Emphysembronchitis gebunden waren. So zeigen ältere Bergleute einen etwa 3fach stärkeren Abfall der Vitalkapazität als Kontrollen.
Muysers et al. [77] untersuchten bei 443 Bergleuten des Ruhrkohlenbergbaus und im Vergleich bei 31 nichtstaubexponierten Arbeitern die Blutgase. Bei Bergleuten ohne und mit Silikose I–III lagen die Sauerstoffpartialdrucke in Ruhe niedriger als in der Kontrollgruppe. Zwischen den Silikosegraden gab es nur geringe Unterschiede. Ferner wurde festgestellt, dass Bergleute mit den Zeichen einer Bronchitis und/oder eines Emphysems in den Silikosegraden I und II niedrigere Sauerstoffpartialdrucke aufwiesen als Bergleute ohne Bronchitis und/oder Emphysem. Worth et al. [78] fanden in einer Erweiterung der Untersuchungen von Muysers [77] eine höhere alveoloarterielle Sauerstoffdruckdifferenz in Ruhe bei allen Silikosegraden als bei Kontrollen, ein weiterer Hinweis auf die Störungen des Gasaustausches bei Bergleuten, auch solchen mit geringen Streuungskategorien.
Worth berichtete 1961 auf einem internationalen Symposium [78] über Studien bei 750 Steinkohlenbergarbeitern und 240 Arbeitern aus anderen Industrien ohne Staubexposition, dass bei Staubexponierten unter Tage das Residualvolumen und die funktionelle Residualkapazität erhöht, die FEV 1 aber erniedrigt waren. Wesentliche Unterschiede zwischen Bergarbeitern ohne silikotische Einlagerungen und mit unterschiedlichen Silikosegraden fanden Worth et al. weder für den Abfall der FEV 1 noch für das Residualvolumen. Die Funktionsstörungen nahmen mit zunehmender Dauer der Exposition zu. Worth et al. nahmen an, dass die Unterschiede bei Staubbelastung in jüngeren Jahren auf einer verstärkten Bronchitis (Hypersekretion durch Staubbelastung) und im Alter von über 50 Jahren vorwiegend auf einem Verlust der Lungenelastizität beruhten.
Ulmer et al. [79] untersuchten 632 unter Tage tätige Bergleute des Ruhrkohlenbergbaus und 200 Bergleute (Gutachtenfälle) mit leichtgradiger Silikose, darüber hinaus 560 Kontrollen, von denen 80 % Arbeiter der eisenerzeugenden und -verarbeitenden Industrie waren, in 20 % handelte es sich um Angestellte. Es fand sich in allen exponierten Gruppen, unabhängig vom Silikosegrad, eine signifikante Erniedrigung des Sauerstoffpartialdrucks im Vergleich zu den Kontrollen. Ulmer et al. [80] führten eine weitere Untersuchung bei 952 Männern (vorwiegend Stahlarbeitern), 626 Bergleuten ohne Silikose im Röntgenbild, 376 Bergleuten mit einer gering gestreuten Silikose einschließlich kleiner (A-)Schwielen (mnpA) und 304 Bergleuten mit einer Silikose mit größeren Schwielen (BC) durch. Die Ergebnisse dieser Untersuchung waren unter anderem eine Lungenblähung und erniedrigte Sauerstoffpartialdrucke bei Bergleuten beider Gruppen vs. Kontrollen. Aufgrund erst bei einer BC-Klassifikation erhöhter Atemwegswiderstände wurde erst bei der Schwielensilikose eine kausale Beziehung mit der gefährdenden Tätigkeit gesehen.
Von Reichel [31, 81] wurden später ergänzende Daten dieser Untersuchungen mitgeteilt inkl. spirometrischer Parameter, die belegten, dass auch bei gering gestreuter Silikose bereits Funktionsstörungen im Mittel vorliegen. Reichel gab in diesen Arbeiten an, er zitiere ältere Daten von Ulmer et al. [79]. Die spirometrischen Daten und die Angaben zur CO-Diffusionskapazität finden sich aber an angegebener Stelle nicht und bezüglich der Atemwiderstände bestehen nicht nachvollziehbare Diskrepanzen.
Rogan et al. [67] untersuchten die Abhängigkeit des FEV 1 von 3581 britischen Kohlenbergarbeitern von der Staubbelastung, dem Rauchen und dem Schweregrad der Bronchitis. Sie fanden eine übermäßige Einschränkung des FEV 1 -Abfalls in 10 Jahren bei höhergradiger Bronchitis, während eine Pneumokoniose keine Ursache eines rascheren Abfalls der FEV 1 war. Die FEV 1 -Werte (andere Lungenfunktionsparameter werden in dieser Arbeit nicht dargestellt) der Silikosegrade I–III waren deutlich niedriger als die des Grades 0, dies ließ sich aber attributabel auf die kumulative Kohlengrubenstaubbelastung zurückführen.
Worth und Smidt [82] führten bei 711 Bergleuten mit in der Thoraxübersichtsaufnahme objektivierter Silikose weitere umfassende Lungenfunktionsprüfungen durch. Sie fanden in allen Altersgruppen Einschränkungen der Lungenfunktion in den Silikosekategorien I–III, bei Zunahme der Ausfallerscheinungen mit dem Alter, nicht aber dem radiologischen Schweregrad der Silikose. Die Autoren stellten heraus, dass das Röntgenbild zwar ein Indikator für die fibrogenen Wirkungen des Mischstaubes, jedoch kein geeigneter Messparameter für die funktionellen Störungen sei.
Smidt [40] veröffentlichte Daten von 1195 Bergleuten ohne Silikose, 874 mit Silikose I, 925 mit Silikose II, 532 mit Silikose III und 126 mit „Pinhead“-Silikose. Es wurden 570 Kontrollen ohne Staubexposition aus dem Bau- und Transportgewerbe eingeschlossen, Funktionelle Veränderungen wurden auch ohne Zeichen einer Silikose anhand der Thoraxübersichtsaufnahme in allen Altersstufen festgestellt. Es fand sich bei allen Streuungskategorien im Mittel eine Verringerung spirometrischer Daten, eine Zunahme der Blähungsparameter und eine Abnahme der Lungendehnbarkeit gegenüber Kontrollen. Es bestand nur eine geringe Tendenz zu einer Zunahme der Funktionsausfälle mit zunehmendem Streuungsgrad der Silikose in der Übersichtsaufnahme, u .a. für FEV 1 und RV%TLC; die Funktionsstörungen waren bei der dichtgestreuten „Pinhead“-Silikose am ausgeprägtesten.
Collins et al. [42] untersuchten 895 britische Bergleute ohne und mit rundlichen bzw. irregulären Verschattungen. In letzterer Gruppe mit Silikose lag die FEV 1 niedriger als in jener ohne Silikose.
Gevenois et al. [52] untersuchten 83 Personen, davon 48 Kohlenbergarbeiter in Belgien und 35 Quarzstaubexponierte anderer Berufe (Sandstrahlarbeiter, Former etc.). Darüber hinaus wurde eine Kontrollgruppe aus 40 Probanden mit Emphysemzeichen eingeschlossen. Es wurden ein Standardröntgenbild, ein Computertomogramm (HR, konventionell) und eine Lungenfunktionsprüfung durchgeführt. FVC, FEV 1 , D L,CO und RV wichen von den Normwerten ab, unterschieden sich aber nicht zwischen Bergleuten mit und ohne CT-Nachweis rundlicher Verschattungen. Bei den Bergleuten und den nichtexponierten Personen mit Emphysem unterschieden sich die Befunde nicht. Es bestand auch kein Unterschied zwischen den Expositionsarten. Die Autoren folgerten, dass die radiologisch nachweisbare Pneumokoniose keinen Einfluss auf die Lungenfunktion besitze.
Wang et al. [44] untersuchten 493 südwestchinesische Bergleute, 289 ohne Nachweis einer Silikose in der Thoraxübersicht, 205 mit Silikose ohne Schwielenbildung, davon 132 mit Silikose 1–2 und 73 mit Silikose 2–3. Bergleute mit Silikose 1–2 und 2–3 hatten signifikant schlechtere Lungenfunktionswerte (Spirometrie, D L,CO ) als Bergleute ohne Silikose.
Bauer et al. [90] wiesen bei 66 Bergleuten aus dem Ruhrbergbau mit Atemwegsobstruktion (FEV 1
Bauer et al. [89] untersuchten 87 Bergleute aus dem Ruhrbergbau mit allen Streuungskategorien nach ILO. Es bestand keine Korrelation zwischen ILO-Klassifikation und Dyspnoe oder FEV 1 . Der CT-Emphysemscore war eng korreliert mit der D L,CO und der FEV 1 /VC max bei univariater Analyse, jedoch nicht mit dem Dyspnoescore. In der multivariaten Analyse war der CT-Emphysemscore assoziiert mit der FEV 1 , nicht aber die ILO-Klassifikation. Die Dyspnoe wurde am besten eingeschätzt mit der D L,CO . Die Autoren folgerten, dass die ILO-Klassifikation des Röntgenbildes zwar möglicherweise ein Marker der Exposition ist, aber wenig Information über den Grad der Funktionsstörungen gibt. Aus den Daten folgt, dass die derzeit durch ärztliche Sachverständige vorgenommene übliche Beurteilung von Steinkohlenbergarbeitern mit der Standard-Lungenfunktionstestung den Grad der Einschränkung durch die Folgen der Silikose nur unzureichend erfasst und dass zumindest eine Bestimmung der D L,CO erfolgen sollte.
Eine Literaturauswertung ergibt, dass eine Silikose mit der Streuungskategorie von > 1/1 (vorwiegend rundliche Fleckschatten) mit einem Verdopplungsrisiko für die Entstehung einer COPD nach einer 15-jährigen Untertagetätigkeit im Steinkohlenbergbau verbunden ist [70].
Andere quarzstaubexponierte Berufsgruppen: Für die Folgen einer Quarzstaubexposition außerhalb des Steinkohlenbergbaus werden acht Arbeiten zitiert, eine weitere Arbeit wurde bereits oben dargestellt [52]. Verwiesen wird auf die Übersicht von Gamble et al. [69], in der die gesamte Literatur mit den überwiegend Raucher-adjustierten Studien berücksichtigt wurde, so dass hier nur die wichtigsten Daten dargestellt werden.
Irwig und Rocks [83] untersuchten 1830 südafrikanische Goldminenarbeiter, davon 122 mit Röntgenzeichen der Silikose, darunter 66 mit Silikose I, 39 mit Silikose II und 11 mit Silikose III, 6 mit großen Schwielen, und 1708 ohne Silikose. FVC, FEV 1 und FEF 25–75 lagen bei Silikose II und III niedriger als bei Silikose 0 und I. Die Unterschiede von FEV 1 bzw. FEF 25–75 zwischen Fällen mit und ohne Silikose waren statistisch signifikant.
Koskinen [64] fand bei 144 finnischen Silikose-Gutachtenfällen eine Einschränkung von FVC und D L,CO bei 46 bzw. 47 % der Untersuchten, mit zunehmender Einschränkung der CO-Diffusionskapazität bei höheren Silikosegraden (3 vs. 2 und 1). Eine Subanalyse von 28 Arbeitern ergab, dass FVC, FEV 1 und D L,CO niedriger lagen als bei geeigneten Kontrollfällen ohne radiologische Zeichen der Silikose. Dyspnoe war das häufigste Symptom in 87 % der Fälle, auch ohne Lungenfunktionseinschränkung. Die D L,CO war der sensitivste Funktionsparameter. Die Arbeit weist nach, dass bereits bei Silikosen mit geringer Streuungskategorie erhebliche Lungenfunktionsstörungen vorliegen können.
Bégin et al. [84] analysierten funktionelle und radiologische (Röntgen, CT) Befunde von 94 kanadischen Arbeitern aus Granitwerken oder Goldminen. Sie unterteilten die Arbeiter in: 1. ohne Nachweis einer Silikose im Röntgenbild oder im CT (Kategorie 0), n = 21; 2. Kategorie 1 im Röntgenbild und im CT, n = 28; 3. Kategorie 1 im Röntgenbild, aber Schwielen anhand des CT, n = 18; 4. Kategorie 1 im Röntgenbild und Schwielen sowohl im Röntgenbild als auch im CT, n = 27. VC und der Unterschied der alveoloarteriellen Sauerstoffdruckdifferenz in Ruhe und unter Belastung waren in den Gruppe 3 und 4 signifikant eingeschränkt. FEV 1 war in den Gruppen 3 und 4, FEF25–75 und FEF 50 waren in den Gruppen 2–4 signifikant vermindert. Über die Spirometrie hinaus wurden unter anderem die Diffusionskapazität und die Lungencompliance untersucht. Die Lungencompliance lag in allen Gruppen mit radiologisch nachweisbarer Silikose niedriger als bei unauffälligem Röntgenbefund, mit signifikanter Verringerung bei schwieliger Silikose. Die CO-Diffusionskapazität war in allen Silikosegruppen vermindert, signifikant bei Schwielenbildung. Auch diese Daten zeigen, dass bei Quarzstaubexposition außerhalb des Steinkohlenbergbaus die Funktionsstörungen mit dem Grad der radiologischen Veränderungen zwar zunehmen, jedoch auch schon in leichteren Fällen vorliegen.
Cowie und Mabena [85] untersuchten 1197 südafrikanische Goldminenarbeiter, davon 340 ohne und 857 mit Silikose, mit den Schweregraden 1 (n = 432), 2 (n = 376) und 3 (n = 49). Die Silikose aller Schweregrade war mit Einschränkungen der Lungenfunktion (Spirometrie, D L,CO ) verbunden, die mit der Schwere der Silikose zunahmen. Die Unterschiede für FVC, FEV 1 , FEF 22–75 und D L,CO zwischen den Kategorien 0/0 und 2/2 waren sämtlich signifikant (p
Cowie [86] stellte in einer Nachuntersuchung von 242 der 1197 Goldminenarbeiter fest, dass bei allen Silikosegraden der jährliche Verlust an FEV 1 , FVC und D L,CO signifikant größer war als bei Arbeitern ohne Silikose, mit Zunahme der Verluste in Abhängigkeit vom Grad der Silikose.
Ng und Chan [87] fanden bei 206 aktiven und 132 ehemaligen chinesischen Steinbrucharbeitern mit Granitstaubexposition eine Korrelation zwischen dem röntgenologischen Silikosegrad und Lungenfunktionsstörungen (FVC, FEV 1 ), insbesondere in den Kategorien 2 und 3. Signifikante Unterschiede von FVC und FEV 1 bestanden zwischen Arbeitern mit rundlichen Verschattungen der Kategorien 2/1–3/4, n = 10, bzw. Schwielen A, B, C (n = 10) und ohne Silikose 0/0 (n = 171).
Bégin et al. [88] untersuchten 207 kanadische Arbeiter mit Asbest- und Quarzstaubexposition. Die 111 Quarzstaubexponierten waren Arbeiter aus Steinbrüchen bzw. steinverarbeitenden Betrieben, darunter 60 mit und 45 ohne Silikose. Hauptergebnis der Studie war, dass im HRCT ein Emphysem auch bei lebenslangen Nichtrauchern häufig war (8/11 mit, 1/20 ohne Pneumokoniose). Das Emphysem korrelierte mit den Einschränkungen von FEV 1 /VC, FEF 22–75 und D L,CO und war die wesentliche Ursache für Funktionsstörungen der Silikosegrade 0 und 1.
Wang und Yano [63] zeigten bei 220 chinesischen Schamott-Arbeitern, dass pulmonale Einschränkungen durch das mit der Silikose verbundene Emphysem verursacht werden (D L,CO , FEV 1 , FEV 1 /FVC), mit signifikanter Zunahme der Funktionsstörungen mit dem Silikosegrad. Besonders die Blähung (Röntgenbefund) war für die Ausfallerscheinungen verantwortlich (Regressionsanalyse). Eine Lungenblähung wurde auch bei Probanden ohne Silikose festgestellt.
Tjoe-Nij et al. [89] erhoben bei 1335 niederländischen Bauarbeitern mit Quarzstaubexposition unterschiedlicher Art radiologische und funktionsanalytische Daten. Diese wurden verglichen mit einer Kontrollgruppe von 1350 Nichtexponierten. Die Lungenfunktion war bei Quarzstaubexponierten signifikant eingeschränkt, mit einer Risikoerhöhung bereits ab der Streuungskategorie 1/1.
Confounder
Problematisch ist die Abgrenzung der Funktionseinschränkungen von den Folgen des Zigarettenrauchens [9, 90]. In einer Reihe von Untersuchungen ist gezeigt worden, dass die Intensität oder Häufigkeit funktioneller Veränderungen unter rauchenden Probanden größer ist als unter Nichtrauchern [42, 83, 44] (siehe 4.1.3.1). Es ist jedoch ebenfalls durch diese Arbeiten belegt, dass silikotische Lungenveränderungen nicht nur bei Rauchern auftreten [42, 83, 44]. Das Rauchen kann bei nachgewiesener Quarzstaublungenerkrankung im Regelfall nicht als alleinige wesentliche (Teil-)Ursache der Funktionseinschränkungen abgegrenzt werden.
Update der Literatur
De Castro et al. [91] untersuchten im Rahmen einer größeren Studie auch 23 Nichtraucher mit „verschwielender“ Silikose mittels konventionellem Röntgen und CT, Lungenfunktion und Diffusionskapazität. Das Lungenvolumen wurde auch mittels CT quantifiziert.
Es wurden signifikante Korrelationen zwischen dem Emphysemvolumen und der forcierten Vitalkapazität und dem Residualvolumen festgestellt. Außerdem bestand eine Korrelation zwischen der Lungendichte und dem Residualvolumen. Es bestand keine Korrelation der Funktionsstörungen mit dem Volumen der großen Schatten. Die Ergebnisse deuten nach Ansicht der Autoren darauf hin, dass das Emphysemausmaß und weniger die Ausprägung der großen Schatten für die Lungenfunktionsbeeinträchtigung bei komplizierten Silikosen verantwortlich ist.
Auch wenn das Ergebnis der Studie pathophysiologisch plausibel erscheint, sind folgende Einschränkungen zu bedenken: Die Autoren machen unverständlicherweise keine Angaben zu den kleinen Schatten bei den untersuchten Patienten, obwohl eine ILO-Klassifikation durchgeführt wurde. Die technische Durchführung der CTs (sequentielle Technik mit 1,5 mm Schichtdicke und 10 mm Inkrement)) entspricht nicht den heutigen Standards. Insgesamt sind die Ergebnisse dieser Arbeit wegen methodischer Mängel schwer zu interpretieren.
Meijer et al. [92] berichten über eine Studie bei 79 Bauarbeitern, die mit Lungenfunktion, CO-Diffusionskapazität, konventionellem Röntgen und HRCT untersucht wurden. Die Röntgenbefunde wurden mittels ILO-Klassifikation, die HRCT-Befunde mit der ICOERD-Klassifikation kodiert. In der ILO-Kategorie 0/0 wurden bei 8 % rundliche, bei 22 % irreguläre Schatten und bei 41 % Emphysemzeichen festgestellt. Rundliche Schatten waren mit einer hohen kumulativen Quarzexposition assoziiert (OR 7,1; 95 % CI 1,3–37,8). Emphysemzeichen waren nicht mit der Exposition, jedoch mit den Rauchgewohnheiten (OR 10,1; 95 % CI 1,2–84,2) und einer Reduktion der Diffusionskapazität assoziiert. Rundliche Schatten im HRCT waren nicht mit der Lungenfunktion korreliert. Die aktuellen Rauchgewohnheiten waren negativ assoziiert mit FEV 1 /FVC und positiv mit RV/TLC und zeigten eine Reduktion in der Diffusionskapazität nach Adjustierung für HRCT-Veränderungen.
Die Autoren zeigen, dass eine gering gestreute Silikose nicht ausgeschlossen werden kann, wenn das konventionelle Röntgenbild normal ist. Emphysemveränderungen waren in dieser Studie expositionsunabhängig vorhanden und trugen neben den Rauchgewohnheiten maßgeblich zu den Funktionsstörungen bei. Rundliche Fleckschatten waren nicht mit Funktionsstörungen assoziiert.
Einschränkend ist in dieser Studie allerdings anzumerken, dass lediglich 4 Fälle eine Streuung 0/1 bzw. 1/0 gemäß ILO Klassifikation und nur 3 Fälle eine Streuung 1/1 aufwiesen.
Brüske et al [93] publizierten ein systematisches Review und eine Metaanalyse zum Zusammenhang zwischen Quarzstaubexposition und einer Obstruktion. Eine berufliche Quarzstaubexposition ist nach Ausschluss von Studien mit konventionell röntgenologischem Nachweis von Silikosen mit einem signifikanten Abfall von FEV 1 und FEV 1 /FVC assoziiert.
Blackley et al. [94] werteten die im Rahmen eines Health-Surveillance-Programmes 2005 bis 2012 erhobenen Spirometriebefunde und Röntgenthoraxaufnahmen von 3771 US-amerikanischen Kohlebergarbeitern aus. 6,5 % wiesen eine Pneumokoniose der Kategorien 1–3 (kleine rundliche Verschattungen) und 1,4 % Schwielenbildungen (PMF) auf. 14,6 % zeigten eine Einschränkung der Lungenfunktion (5,1 % obstruktiv, 7,9 % restriktiv, 1,6 % kombiniert). 30,5 % der Pneumokoniose-Probanden mit kleinen rundlichen Verschattungen, 41,5 % der Probanden mit Schwielenbildungen und 13,5 % der Bergleute ohne einen auffallenden Röntgenbefund hatten Lungenfunktionseinschränkungen. Offensichtlich aufgrund schlechterer arbeitshygienischer Bedingungen ergab sich für kleine Minen im Vergleich zu großen eine mehr als doppelt so hohe Prävalenz einer Pneumokoniose und der Kombination einer kleinherdigen Pneumokoniose mit Lungenfunktionseinschränkung. Die Autoren schlussfolgern, dass trotz der bestehenden Regularien zur Staubreduktion und Empfehlungen zum Arbeitsschutz, die Arbeitsbedingungen in US-amerikanischen Kohleminen keinen adäquaten Schutz vor adversen respiratorischen Effekten gewährleisten.
Forastiere et al. [95] untersuchten 642 weibliche Keramikarbeiterinnen, die an einem Vorsorgeprogramm zwischen 1974 und 1987 teilnahmen und bis 1991 weiter verfolgt wurden. Das Silikoserisiko war nicht mit den Rauchgewohnheiten assoziiert und zeigte eine Dosis-Wirkungs-Beziehung für die Expositionsdauer. Sowohl FVC als auch FEV 1 zeigten signifikante Assoziationen mit der Expositionsdauer und mit röntgenologischen Befunden.
Tse et al. [96] beschreiben eine historische Kohortenstudie mit 3202 Personen mit Silikose in Hongkong, die von 1981 bis 2005 verfolgt wurde. Es wurde die Interaktion zwischen Rauchgewohnheiten und Silikose analysiert. Es wurde eine signifikant erhöhte SMR für Atemwegserkrankungen (Lungenkrebs, chronische obstruktive Atemwegserkrankung, Silikose) und andere Lungenerkrankungen wie z. B. Tuberkulose gefunden. Die Interaktion zwischen Rauchgewohnheiten und Erkrankung differierte zwischen den einzelnen Diagnosen, wobei nach Aussagen der Autoren die Power der Studie limitiert sei.
Kreuzer et al. [97] haben bei einer Kohorte von Furanminenarbeitern mit 58 690 Beschäftigten die Todesursachen in einem Beobachtungszeitraum von 1946 bis 2008 von 2336 Todesfällen ausgewertet. Das Risiko an einer COPD oder an anderen nicht malignen Atemwegserkrankungen zu sterben in Abhängigkeit zur kumulativen Exposition zu Quarzstaub war nicht erhöht, außer in der Gruppe der Probanden mit Silikose oder anderer Pneumokoniose. Hier ergab sich ein starker nicht linearer Anstieg des Risikos. Die kumulative Radonexposition war nicht zu Todesfällen durch COPD und anderen nicht malignen Atemwegserkrankungen assoziiert.
Tamura et al. [98] untersuchten 46 Probanden mit Exposition gegenüber mineralischen Stäuben und 25 Kontrollprobanden mit der konventionellen Röntgentechnik und HRCT. Drei Experten kodierten die Röntgenbilder gemäß ILO-Klassifikation und die CT-Aufnahmen gemäß ICOERD Klassifikation. Die Spearman Rangsummenkorrelation zwischen ICOERD und ILO war 0,844 für rundliche Fleckschatten (p
Die Autoren widersprechen sich allerdings in ihrer Ergebnisdarstellung. Einerseits beschreiben sie, dass sich die Korrelation ausschließlich auf Probanden mit rundlichen Fleckschatten bezieht und damit auf ein Teilkollektiv, andererseits geben sie bei den Ergebnissen der Korrelation mit n = 74 die Summe der Exponierten und nichtexponierten Kontrollprobanden an, die aber nicht alle rundliche Fleckschatten hatten.
Diskussion und Schlussfolgerungen
Die verfügbaren Untersuchungen der Lungenfunktion in Abhängigkeit von den radiologisch nachweisbaren Folgen der Exposition gegenüber silikogenen Stäuben belegen, dass bei Personen mit allen röntgenologisch nachweisbaren Graden der Silikose wesentlich häufiger Lungenfunktionsstörungen als bei nicht quarzstaubexponierten Vergleichsgruppen auftreten. Ähnliches gilt für Korrelationen zwischen Pathologie-Befunden und der Lungenfunktion. Dies gilt sowohl für die Parameter VC, FEV 1 und D L,CO als auch für den Blählunge-Parameter RV und spiroergometrische Messgrößen (siehe Tabellen 3–9). Diese Ausfallserscheinungen stimmen mit den pathologisch-anatomischen Erkenntnissen überein, nach denen bei einer Silikose häufig ein Emphysem unterschiedlicher Art und Schwere nachzuweisen ist [99, 100, 88, 52, 77, 44, 63, 78]. Nicht der konventionell-röntgenologisch nachweisbare Befund einer Granulomatose und Fibrose, sondern die mit diesen Veränderungen verbundenen Folgen, d. h. Lungenemphysem und Elastizitätsminderung, sind vor allem für die Ausfallserscheinungen der Lungenfunktion und die Leistungseinschränkung des Erkrankten verantwortlich, eine keineswegs neue Erkenntnis [81, 17]
In der umfassenden Übersicht über die Veränderungen der Lungenfunktion bei Quarzstaubexponierten außerhalb des Steinkohlenbergbaus von Gamble et al. [69] wurden Rauchen und Staubexposition als die wesentlichen Einflussfaktoren für die Assoziation zwischen Silikose und Lungenfunktionseinschränkung identifiziert. Aus den dargestellten Studien ergibt sich kein wesentlicher Unterschied der FEV 1 bzw. D L,CO zwischen den Silikosen mit den ILO-Kategorien 0 und 1, während für die Kategorien 2 und 3 bzw. die schwielige Silikose zunehmende Funktionsausfälle festgestellt wurden. Dies gilt sowohl für Studien mit als auch ohne Raucheradjustierung. Dabei ist zu berücksichtigen, dass Exponierte mit Silikosekategorie 0 im Mittel bereits eingeschränkte Lungenfunktionswerte aufweisen. Diese Aussagen werden von einigen Fehlern (z. B. wird die dosisabhängige Lungenfunktionseinschränkung von Hnizdo [56] nicht korrekt wiedergegeben) nicht eingeschränkt.
Tjoe-Nij et al. [89], Cowie [86], Reichel [31], Koskinen [64] und Smidt [40], Meijer et al., [92] und Blackley et al. [94] haben dargelegt, dass ein erhöhtes Risiko für das Auftreten von Funktionsstörungen auch bei einem Silikosegrad 1/1 besteht.
Zusammenfassend besteht ein erhöhtes Risiko für Einschränkungen der Lungenfunktion auch bei niedrig gestreuten Silikosen. Darüber hinaus wird dargestellt, dass zwischen dem Dyspnoegrad und der Standardlungenfunktion keine enge Beziehung besteht. Die CO-Diffusionskapazität und die submaximale Spiroergometrie korrelieren besser mit dem Grad der Dyspnoe als die Parameter der Spirometrie und Ganzkörperplethysmografie.
Die kumulative Belastung durch silikogene Stäube spielt eine wesentliche Rolle bei der Entstehung von Lungenschäden, allerdings kann es bereits bei relativ geringer Exposition schon zu Beschwerden und Funktionsstörungen kommen [39].
Die Literatur belegt, dass die Spirometrie und Ganzkörperplethysmografie nur bedingt geeignet sind, die Dyspnoe zu erfassen. Nach Duvenkamp et al. [102] besteht bei Probanden mit gering gestreuten Silikosen keine Korrelation zwischen spiroergometrisch objektivierten Funktionseinschränkungen und ILO-Klassifikation. Im Mittel fanden sich signifikante Einschränkungen bereits bei niedrig gestreuten Silikosen im Vergleich zu nicht exponierten Kontrollen. Bauer et al. [99] fanden, dass der ergospirometrische Parameter V.E/ V.O 2 mit dem Dyspnoegrad signifikant besser als die Obstruktionsparameter korreliert.
Der HRCT-Grad des Lungenemphysems korreliert eng mit der CO-Diffusionskapazität, der FEV 1 und der FEV 1 in % der VC (sog. Tiffeneau-Index) [100]. Letztere Autoren folgern, dass die ILO-Klassifikation zwar möglicherweise ein guter Expositionsmarker ist, jedoch keine wesentliche Information über den Grad der Funktionsminderung liefert, und dass die Routinediagnostik zumindest die Bestimmung der Diffusionskapazität involvieren sollte.
Diese Untersuchungen belegen, dass für die korrekte Einschätzung der Belastbarkeit bzw. der Dyspnoe bei Quarzstaubexponierten neben den klassischen Parametern der Spirometrie und Ganzkörperplethysmografie auch die Parameter des Gasaustausches erfasst werden müssen. Hierfür eignen sich in erster Linie die CO-Diffusionskapazität und eine Spiroergometrie.
Im Ergebnis ist aus den Studien zu schließen, dass bei Quarz- und Mischstaubexponierten der Grad der funktionellen Schäden (vor allem Störungen der Atemmechanik mit obstruktiver und restriktiver Ventilationsstörung und des Gasaustausches) nicht gut mit dem Befund der konventionellen Thorax-Übersichtsaufnahmen korreliert.
4.3.3 Interaktion der Exposition durch silikogene Stäube und Zigarettenrauch
Die differenzialdiagnostisch bedeutsamen gesundheitsschädlichen Auswirkungen des Zigarettenrauchens, insbesondere auf die Lungenfunktion, sind in einer Reihe von Studien gut belegt (siehe diesbezügliche Dosis-Wirkungs-Beziehungen bei Fletcher et al. [103, 104] und Jaakkola et al. [105] (jährlicher FEV 1 -Verlust: – 8,4 mL/Packyear).
Hinsichtlich der synergistischen Interaktion von Belastungen durch silikogene Stäube und Zigarettenkonsum wird auf die unter 4.3.1 und 4.3.2 dargestellten Veröffentlichungen sowie auf die Übersichtsarbeiten von Coggon und Newman Taylor [33, 106]) und von Oxman et al. [37] verwiesen. Die Schätzungen der letztgenannten Autoren ergaben, dass 80 von 1000 Nieraucher-Bergleuten mit einer kumulativen Staubdosis von 122,5 gh/m 3 (entsprechend 35 Jahren Arbeit mit einer Feinstaubexposition von 2 mg/m 3 ), einen auf diese Staubdosis zurückzuführenden klinisch bedeutsamen FEV 1 -Verlust von mehr als 20 % aufweisen; für Raucher betrug der Anteil 66 von 1000 bei derselben Staubdosis.
In umfassenden Verlaufsuntersuchungen von 895 britischen Kohlenbergarbeitern objektivierten Collins et al. [42] lineare Dosis-Wirkungs-Beziehungen des quarzhaltigen alveolengängigen Kohlengrubenstaubs in Bezug auf die Einschränkung der Lungenfunktion (FEV 1 , FVC, FEV 1 /FVC) unter Berücksichtigung des Röntgenbefundes sowohl für Zigarettenraucher als auch für Nieraucher.
Ähnlich beschreiben Montes et al. [107] einen akzelerierten signifikanten FEV 1 -Verlust bei der überwiegenden Tätigkeit vor Stein in Kohlenbergwerken (p = 0,044) und Rauchen (p = 0,001). Der akzelerierte FEV 1 -Verlust betrug unter Rauchern 14,8 %, unter Exrauchern 10,9 % und unter Nierauchern 8,6 %; die Effekte der Staubbelastung und des Rauchens waren additiv.
Kuempel et al. [108] fanden mittels multivariater Analysen bei Autopsien von 616 US-amerikanischen Kohlenbergarbeitern einen stärkeren Einfluss der kumulativen Kohlengrubenstaubbelastung auf die Emphysemausprägung als des Rauchens.
Zusammenfassend lassen sich in der Gesamtschau der Literatur konsistent Assoziationen zwischen der Dosis silikogener Stäube einerseits und dem Auftreten von Dyspnoe, Lungenfunktionseinschränkungen unter Nierauchern und Rauchern andererseits darstellen. Auch sind die synergistischen (additiven) Wirkungen der alveolengängigen Staubbelastung und des Zigarettenkonsums mit Kollektiv- und Studiendesign-bedingten Streuungen gut belegt. Die differenzialdiagnostisch bedeutsamen Effekte des Zigarettenrauchens sind unter Berücksichtigung ihrer bekannten Dosis-Wirkungs-Beziehung in gut definierten Kollektiven abzuschätzen.
Hinsichtlich der Begutachtung des Einzelfall ist festzuhalten, dass bei einer gesicherten Quarzstaublungenerkrankung als Folge der versicherten Einwirkung von silikogenen Stäuben dieser Staubbelastung bei gleichzeitigem Zigarettenrauchen in der Regel ein rechtlich wesentlicher Anteil an der „Krankheitsentstehung“ und Lungenfunktionsminderung zukommt (vgl. 3.2 „Versicherte Einwirkung“, 3.3.2 „Kausalitätsgrundsätze“ und 4.3.2 „Einschränkungen bei Silikose“).
4.4 Studienlage zu Histologiebefunden versus Thoraxübersichtsaufnahmen
Pathologisch-anatomische Untersuchungen zeigen, dass mit der konventionellen Röntgen-Thoraxaufnahme in einem Großteil der Fälle die silikotischen Läsionen nicht entdeckt werden, so in 200 von 328 Fällen (61 %) in den Untersuchungen von Hnizdo und Mitarb. [13] und in über 30 % in den Untersuchungen von Vallyathan et al. [109]. Der ganz überwiegende Teil der langjährig unter Tage beschäftigten Steinkohlenbergleute weist in tabula silikotische Veränderungen auf [110–112] stellten bei 430 Autopsiefällen von Kohlenbergarbeitern eine Korrelation zwischen den Befunden der Thoraxübersichtsaufnahme zu Lebzeiten und mikro- und makronodulären pathologischen Befunden fest (R = 0,5), eine gute Übereinstimmung lag aber erst bei höhergradigen pathologischen Befunden bzw. einer ILO-Klassifikation von 0/1 vor. Laut Vallyathan et al. [112] sind in 96 % Maculae, in 70 % mikronodulär- und in 45 % makronodulär-silikotische Läsionen nachweisbar. Ein Drittel der anhand der Thoraxübersichtsaufnahme diagnostizierten Schwielen ließ sich pathologisch-anatomisch nicht bestätigen, 22 % der pathologisch-anatomisch festgestellten Schwielen waren im konventionellen Röntgenthoraxbild nicht entdeckt worden.
Hnizdo et al. [13] untersuchten bei 557 Goldminenarbeitern den Zusammenhang zwischen Röntgenbild des Thorax und autoptischen Befunden. Bei Verwendung des ILO-Kriteriums 1/1 lag die Sensitivität Befunder-abhängig zwischen 0,393 und 0,236 und die Spezifität zwischen 0,987 und 0,965. Dass bedeutet, dass zahlreiche leichtere Silikosefälle in Folge einer ILO-Klassifikation Tabelle 10).
Bauer et al. [14] verglichen bei 126 verstorbenen Kohlenbergarbeitern den pathologisch-anatomischen Befund mit der ILO-Klassifikation. Erst bei einer ILO-Klassifikation von 2/3 stimmte die anhand der Thoraxübersichtsaufnahme gestellte Diagnose mit dem pathologisch-anatomischen Befund hinreichend überein (Spezifität 74 %), die Sensitivität lag bei dieser Klassifikation nur bei 60 %. Eine gute Übereinstimmung fand sich nur für die Schwielenbildung (rs = 0,71; p
Die Studien belegen die Limitationen der Thoraxübersichtsaufnahme für die Erfassung silikotischer Läsionen der Lungen. Häufig sind dabei sowohl falsch-positive als auch falsch-negative Befunde sowie graduelle Über- und Unterschätzungen des Streuungsgrades.
5 Grundlagen der Begutachtung
5.1 Diagnosesicherung
Die Diagnose beruht auf der nachgewiesenen, versicherten Exposition gegenüber silikogenen Stäuben und dem Nachweis von für die Quarzstaublunge typischen Veränderungen im konventionellen Röntgenthoraxbild, in der Low Dose Volumen HRCT (Einzelheiten siehe Untersuchungsprotokolle in den Anlagen) und/oder in der pathologisch-anatomischen Untersuchung von Lungengewebe.
Differenzialdiagnostisch müssen v.a. andere granulomatöse Lungenveränderungen wie z. B. die Sarkoidose und tumorbedingte Veränderungen (s. Tabelle 11 ) berücksichtigt werden.
Als Anzeigekriterium für das Vorliegen einer Silikose hat sich in der langjährigen täglichen Praxis in Deutschland für die Thoraxübersichtsaufnahme der Streuungsgrad 1/1 nach ILO, bevorzugt in beiden Oberfeldern bzw. das Vorliegen eierschalenartig verkalkter Lymphknoten herauskristallisiert.
Als Anzeigekriterium für eine Silikose in der Computertomographie gilt ein Gesamtstreuungsgrad rundlicher Verdichtungen von 2 mit Beteiligung beider Oberfelder oder Lymphknotenverkalkungen.
5.2 Feststellung der Funktionseinschränkungen
Die Funktionseinschränkungen werden in erster Linie mit den Methoden der qualitätsgesicherten Lungenfunktionsprüfung objektiviert, die auf Basis der Empfehlung der wissenschaftlichen Fachgesellschaften durchzuführen ist. Im Einzelnen sind dies: Spirometrie mit Flussvolumenkurve, Ganzkörperplethysmografie, bei Obstruktion und/oder Lungenblähung ein Reversibilitätstest, Bestimmung der CO-Diffusionskapazität (Transferfaktor), Blutgasanalyse in Ruhe und nach submaximaler Belastung und wenn möglich Spiroergometrie.
Zur Basisuntersuchung gehört außerdem ein EKG, bei Hinweisen auf eine Druckerhöhung im kleinen Kreislauf auch die Doppler-Echokardiografie. Für Einzelheiten vgl. Kapitel 6.2. Für die Beurteilung der Lungenfunktionswerte sind der intraindividuelle Verlauf sowie aktuelle und valide Referenzwerte zu Grunde zu legen [113]. Im Spätstadium mit respiratorischer Insuffizienz kommt es typischerweise zur Druckerhöhung im kleinen Kreislauf, schließlich zum Cor pulmonale und zur Rechtsherzinsuffizienz (siehe 4.1).
5.3 Zusammenhang zwischen Quarzstaublungenerkrankung und Funktionseinschränkung
Der auf die Quarzstaublungenerkrankung zurückzuführende Funktionsverlust im Sinne obstruktiver und restriktiver Ventilationsstörungen sowie Gasaustauschstörungen ergibt sich aus den unter 4.3.2 dargestellten Studien.
6 Empfehlungen für die Erstellung eines Zusammenhangsgutachtens
Den Auftrag zur gutachterlichen Untersuchung erteilt der zuständige Unfallversicherungsträger nach Abschluss der Vorermittlungen. Der Auftrag soll eindeutig formuliert sein.
Als Hilfestellung für Gutachter und UV-Träger hat die DGUV [3] die Empfehlung für die Begutachtung von Quarzstaublungenerkrankungen (Silikosen) – Bochumer Empfehlung – veröffentlicht; die Empfehlung wird derzeit überarbeitet.
6.1 Vorermittlungen
Dem ärztlichen Sachverständigen sollen alle für die Begutachtung notwendigen Vorinformationen zur Verfügung gestellt werden. Dazu gehören insbesondere Unterlagen zur Krankheitsvorgeschichte und zu Erkrankungen, die in einer Beziehung zu der zu begutachtenden Krankheit stehen können, die Befunde der arbeitsmedizinischen Vorsorgeuntersuchungen sowie vollständige problemorientierte Ermittlungen zur Arbeitsvorgeschichte mit Angaben zur Dauer und Intensität relevanter Einwirkungen. Für die Zusammenhangsbeurteilung ist daher neben den medizinischen Befunden auch zu klären, ob und in welchem Umfang der zu Begutachtende gegenüber Stäuben exponiert war, die kristalline Kieselsäure enthalten haben. Auch die Exposition gegenüber allen silikogenen Modifikationen der freien Kieselsäure, also auch Tridymit und Cristobalit, ist zu ermitteln. Die Unfallversicherungsträger haben diese Ermittlungen so umfassend wie möglich vorzunehmen und vor dem Gutachtenauftrag abzuschließen.
Wenn keine Messergebnisse zur Staubbelastung oder zur Belastung mit Quarz vorliegen, die auf die individuelle Belastung schließen lassen, was eher die Regel ist, sind die Arbeitsplätze differenziert hinsichtlich der Länge der Belastung, der lüftungstechnischen Gegebenheiten und weiterer Faktoren zu beschreiben, die für die Abschätzung der Belastung bedeutsam sind. Für den Bergbau gehören dazu Angaben, ob und wie lang im Streckenvortrieb, im Schachtbau oder vor Kohle gearbeitet wurde und welche Staubminderungsmaßnahmen ergriffen worden sind. Für die Steinbearbeitung sind Angaben bedeutsam, ob trocken oder nass bearbeitet wurde und welche Stauberfassungsgeräte tatsächlich eingesetzt wurden. Weitere wichtige Hinweise zur Abschätzung der Belastung sind Daten zum Anteil von freier Kieselsäure im bearbeiteten Material. Sehr hilfreich können auch branchen- und tätigkeitsspezifische Daten zur Belastung sein, die dem ärztlichen Sachverständigen zur Verfügung zu stellen sind. Für den untertägigen Bergbau haben sich die Schichtbuchauszüge als wichtige Quelle für Expositionsabschätzungen bewährt. Ein Bericht des Präventionsdienstes, der die Ergebnisse der Ermittlungen zur qualitativen und kumulativen quantitativen Exposition zusammenfasst, sollte dem Begutachtungsauftrag beiliegen.
Fehlen ausreichende Daten zur Belastung oder sind die Ermittlungen zu den Arbeitsverhältnissen nicht durchgeführt worden, ist eine Zusammenhangsbeurteilung nicht möglich. Die medizinische Begutachtung kann nicht begonnen werden, bevor eine entsprechende Belastung mit silikogenen Stäuben mit an Sicherheit grenzender Wahrscheinlichkeit festgestellt worden ist. Wegen der erforderlichen medizinischen Diagnostik (Strahlenexposition) sind die Ermittlungen zu den Belastungen am Arbeitsplatz immer vor der medizinischen Begutachtung abzuschließen.
Neben den vorgenannten Ermittlungen sind die für die Beurteilung erforderlichen medizinischen Befunde, die noch verfügbar sind, zu ermitteln und dem ärztlichen Sachverständigen zur Verfügung zu stellen. Dies gilt insbesondere für radiologische Untersuchungen des Thorax. Entsprechendes gilt für andere Arztberichte und Untersuchungsbefunde, soweit sie sich auf das Atmungsorgan sowie Herz und Kreislauf beziehen und/oder sonst für die Fragestellung relevant sind.
Die Unfallversicherungsträger haben das Recht, im Rahmen der Ermittlungen zur Feststellung einer Berufskrankheit auf die medizinischen Daten zuzugreifen, nicht nur Fragen bei den (auch früher) behandelnden Ärzten, sondern auch bei der Krankenkassen und den Rentenkassen sowie auch beim Versorgungsamt sind dazu zulässig.
Erforderlich ist auch immer eine Nachfrage bei den Betriebsärzten des Beschäftigungsbetriebs nach entsprechenden medizinischen Befunden, denn Personen, die im Rahmen ihrer versicherten Arbeit gegenüber Staub mit kristalliner Kieselsäure exponiert sind, muss arbeitsmedizinische Vorsorge gemäß ArbMedVV angeboten werden. Insbesondere diese Vorbefunde müssen vollständig eingeholt und in der Zusammenhangsbeurteilung berücksichtigt werden. Für die Befunde aus diesen Untersuchungen gelten gesonderte längere Aufbewahrungsfristen (AMR 6.1).
6.2 Diagnostik
6.2.1 Anamnese
Eine gute Qualität des medizinischen Gutachtens setzt qualifizierte arbeitsmedizinische und pneumologische Feststellungen voraus. Die vom ärztlichen Sachverständigen erhobene eingehende Anamnese soll unter Berücksichtigung der Befunde der Vorermittlungen die gesundheitliche und berufliche Vorgeschichte des Versicherten sowie seine gesundheitlichen Beschwerden, insbesondere Husten, Auswurf, Dyspnoe, klären. Zur besseren Standardisierung steht heute der COPD-Assessment-Test (CAT) zur Verfügung [114, 115]. Eine Online-Version steht zur Verfügung unter: www.catestonline.org/english/index_German.htm .
Es ist eine vollständige Anamnese über das gesamte Arbeitsleben einschließlich der Expositionsbedingungen zu erheben und das Ergebnis mit den aktenkundigen Ermittlungsergebnissen zu vergleichen. Auch müssen außerberufliche gesundheitliche Gefährdungen erfasst werden, insbesondere die Rauchgewohnheiten. Diese Angaben werden in das Gutachten aufgenommen. Auf für die Beurteilung bedeutsame Abweichungen zur Aktenlage hat der ärztliche Sachverständige hinzuweisen und gegebenenfalls eine Alternativbeurteilung vorzunehmen.
6.2.2 Diagnosesicherung
Die wesentlichen diagnostischen Schritte sind im Algorithmus „Diagnostikschema“ dargestellt ( Abb. 1 ).
Die Verdachtsdiagnose wird in der Regel zunächst anhand der konventionellen Röntgenaufnahmen des Thorax in einer Ebene unter Berücksichtigung der radiologischen Vorbefunde geäußert. Sofern Voruntersuchungen vorliegen, ist eine Verlaufsbeurteilung unverzichtbar. Anamnese und Expositionsermittlung sind zu berücksichtigen. Zur Röntgendiagnostik und diesbezüglichen Qualitätssicherung siehe Ooi et al. [116] und Hering [117].
Die Anzeigekriterien für eine Silikose sind erfüllt, wenn kleine rundliche Schatten von Typ p, q oder r mit einer gewissen Reichlichkeit und gleichmäßigen Verteilung im Sinne eines Streuungsgrades nach ILO 2000 [2] von 1/1 oder höher im Röntgenthorax-Bild nachweisbar sind.
Differenzialdiagnostisch müssen v.a. andere granulomatöse Lungenveränderungen wie z. B. die Sarkoidose und tumorbedingte Lungenveränderungen (s. Tabelle 11) abgegrenzt werden.
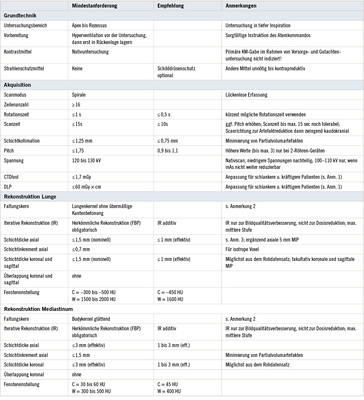
Wegen der häufig bestehenden Unsicherheit bei der Beurteilung der Röntgenaufnahmen des Thorax, insbesondere bei gering gestreuter Silikose, ist im Rahmen der Erstbegutachtung grundsätzlich eine qualifizierte Low Dose Volumen HRCT des Thorax erforderlich, um die Diagnose Silikose zu sichern oder auszuschließen und gegebenenfalls ein Emphysem morphologisch zu objektivieren [118].
Unter dem Gesichtspunkt der rechtfertigenden Indikation ist zu beachten, dass alle existierenden CT-Untersuchungen der Lunge, die aus anderer Ursache angefertigt wurden, vor der Indikationsstellung zu einer erneuten CT-Untersuchung herangezogen werden. Nur wenn die Befundung dieser Aufnahmen keine eindeutige Diagnose zulässt, wird die Anfertigung einer weiteren Computertomographie empfohlen, die standardisiert qualifiziert nach Protokoll (siehe Anlage) zu erfolgen hat.
Für die standardisierte Befundung der Low-Dose-Volumen-HRCT ist die Anwendung der CT-Klassifikation ICOERD (International Classification of Occupational and Environmental Respiratory Diseases) zwingend erforderlich. Um die Diagnose einer Silikose in der CT-Untersuchung zu stellen, ist der Nachweis scharf berandeter Verdichtungen in beiden Oberlappen, die in Lungenkern und Lungenmantel lokalisiert sein können, erforderlich. Beim Vergleich mit dem Referenzfilm muss mindestens die Streuungskategorie 1 im rechten wie auch im linken Oberfeld erreicht sein (Gesamtstreuung mindestens 2).
Grundsätzlich ist die HRCT-Untersuchung in Low-Dose-Technik durchzuführen. Aus Gründen der Reproduzierbarkeit und Vergleichbarkeit ist ein standardisiertes Untersuchungsprotokoll einzuhalten [119–121]. Genaue Angaben dazu finden sich im Anhang „Low-Dose-Volumen-HRCT des Thorax“.
Die pathologisch-anatomische Diagnose erfolgt nach den in 4.2 genannten Kriterien. Als insignifikant sind Befunde anzusehen, bei denen weniger als 5 Silikoseknötchen pro Lungenflügel palpatorisch erfasst (siehe 4.2) und histologisch bestätigt werden [122] und seltene nichtfibröse Formen der Silikose wie eine rein makuläre Silikose [123] ausgeschlossen werden kann. Es gibt unter Steinkohlenbergleuten auch Hinweise auf eine Kohlengrubenstaub-induzierte diffuse Fibrose, die sich klinisch von der idiopathischen Lungenfibrose nicht unterscheiden lässt [124].
Es besteht weder eine Indikation noch eine Mitwirkungspflicht hinsichtlich einer Biopsie, die allein der Diagnosesicherung im Rahmen des BK-Verfahrens dient. Stehen histopathologische Untersuchungsbefunde, die aus anderer Indikation gewonnen wurden, zur Verfügung, können diese jedoch einbezogen werden. Erfahrungsgemäß ist die Sensitivität und Spezifität der Diagnosestellung anhand von Gewebeproben sensitiver und spezifischer als die HRCT-Diagnostik, wenn ausreichend geeignetes und repräsentatives Gewebe vorliegt
Sofern Zweifel an der Diagnose bestehen, z. B. bei anamnestisch oder durch den radiologischen Befund begründeten Hinweisen auf differenzialdiagnostisch zu erwägende andere Ursachen pulmonaler Verschattungen (Tabelle 11), ist die weitere Abklärung Bestandteil der gutachterlichen Untersuchung bis zur Bestätigung oder bis zum Ausschluss einer BK-Nr. 4101. Sofern die CT-Untersuchung primär andere Erkrankungen wahrscheinlich macht und eine Silikose ausschließt, kann die gutachterliche Diagnostik an dieser Stelle beendet werden. Der versicherten Person sollte empfohlen werden, eine weitere Abklärung der Untersuchungsergebnisse vornehmen zu lassen, z. B. durch den Hausarzt. Die weiterbehandelnden Ärzte sollten gleichfalls informiert werden, sofern die versicherte Person damit einverstanden ist.
Stützt die (CT-)Untersuchung die Diagnose einer Silikose, wird die gutachterliche Untersuchung unter der Annahme eines Versicherungsfalls einer BK Nr. 4101 weitergeführt.
6.2.3 Funktionseinschränkungen
Durch weitere Diagnostik ist zu klären, welches Ausmaß die Folgen der BK Nr. 4101 aufweisen und ob auch der Leistungsfall einer BK Nr. 4101 aus gutachterlicher Sicht bejaht werden kann.
Durch die BK Nr. 4101 werden v. a. Beschwerden und Befunde im Sinne einer chronischen (obstruktiven) Bronchitis und/oder eines Lungenemphysems verursacht. Hauptsymptome sind Belastungsluftnot und/oder Husten und Auswurf. Insbesondere die Belastungsluftnot ist ein vieldeutiges Symptom, das unter Berücksichtigung der jeweils betroffenen Altersgruppe eine sorgfältige Differenzialdiagnostik erforderlich macht ( Tabelle 12 ). Daher sollte die weitergehende Diagnostik in erster Linie auf die Abklärung, Objektivierung und Quantifizierung der Dyspnoe bzw. der Belastungseinschränkung ausgerichtet sein.
Die Erfassung und Quantifizierung von Funktionseinschränkungen erfordert eine qualitätsgesicherte, vollständige Lungenfunktionsprüfung auf Basis der Empfehlungen der wissenschaftlichen Fachgesellschaften [125–130]. Durchgeführt und grafisch dokumentiert werden müssen Spirometrie mit Flussvolumenkurve, Ganzkörperplethysmografie (bei Obstruktion und/oder Blähung mit Reversibilitätstest, Bestimmung der CO-Diffusionskapazität (Transferfaktor), Blutgasanalyse in Ruhe und Ergometrie mit submaximaler Belastung im Steady State, möglichst Spiroergometrie mit Blutgasanalyse bei maximaler Belastung.
Falls weder eine Ergometrie noch eine Spiroergometrie durchführbar ist, soll ein 6-Minuten-Gehtest mit Pulsoxymetrie durchgeführt werden [131, 132]. Diese Belastungsuntersuchungen haben eine große Bedeutung bei der Erfassung der kardiopulmonalen Leistungsfähigkeit.
Weitere diagnostische Verfahren sind EKG sowie bei Hinweisen auf Druckerhöhung im kleinen Kreislauf und gegebenenfalls zur Beurteilung der linksventrikulären Funktion eine Dopplerechokardiografie. Werden echokardiographisch pulmonalarterielle Drücke über 30 mmHg systolisch ermittelt, kann eine pulmonale Hypertonie vorliegen (s. Leitlinie pulmonale Hypertonie). Echokardiographisch gilt eine pulmonale Druckerhöhung aber erst ab systolischen Werten > 50 mmHg als wahrscheinlich.
Im vorgenannten Grenzbereich kann eine Rechtsherzkatheter-Untersuchung im Rahmen einer Silikose-Begutachtung ausnahmsweise empfohlen werden, wenn die Echokardiographie Hinweise auf erhöhte Druckwerte ergibt. Sie kann gegebenenfalls helfen, die Diagnose einer pulmonal-arteriellen Hypertonie zu klären. Eine pulmonale Hypertonie ist bei der Beurteilung der MdE zu berücksichtigen und ist auch prognostisch relevant.
Auch bei der Differentialdiagnose zwischen rechts- und linkskardialer Insuffizienz kann die Rechtsherzkatheter-Untersuchung hilfreich sein.
Die Rechtsherzkatheter-Untersuchung ist nicht mitwirkungspflichtig. Die versicherte Person ist daher darüber zu informieren, dass ihr bei Ablehnung der Untersuchung keine Nachteile entstehen.
Für die Spirometriebeurteilung werden die neuen GLI-Referenzwerte zugrunde gelegt [113]. Bzgl. der Graduierung der Einschränkungen wird auf die Leitlinie Spirometrie der DGP [133] verwiesen. Eine Zusammenfassung ist im Folgenden dargestellt:
- Obstruktive Ventilationsstörung
Wenn FEV 1 /FVC
FEV 1 -Einschränkung
85% LLNleichtgradig
Restriktive Ventilationsstörung
Wenn TLC
FVC-Einschränkung
85% LLN leichtgradig
Aufgrund der unterschiedlichen Bezugsgrößen nach Einführung der neuen Sollwerte sollte immer auch der intraindividuelle Verlauf besonders gewürdigt werden.
Eine Blutgasanalyse mit Bestimmung des Säure-Basen-Haushaltes ist obligater Bestandteil jeder Begutachtung. Das Blut wird aus dem gut hyperämisierten Ohrläppchen entnommen. Wird eine kapilläre Blutgasanalyse unter Belastung durchgeführt, ist auf das Erreichen des sog. Steady State (s. oben) zu achten, d. h. die Abnahme darf erst am Ende der vierten Minute bei gleichbleibender Belastungsstufe erfolgen. In jedem Fall muss die Abnahme aber vor Abbruch der Belastung durchgeführt werden.
Ursachen für ein respiratorisches Versagen (Hypoxämie ohne Hyperkapnie) in Ruhe können sowohl eine Diffusionsstörung, ein intrapulmonaler Shunt als auch eine Ventilations-/Perfusionsinhomogenität (mismatch) sein. Die Pathophysiologie einer Ventilations-/Perfusionsinhomogenität ist typisch für obstruktive Atemwegserkrankungen. Bei schwerer Obstruktion kann auch eine Hypoventilation auftreten (ventilatorische Insuffizienz, Hypoxämie mit Hyperkapnie). Die Hypoxämie ist dann konsekutiv. Dies wird nur in fortgeschrittenen Stadien der Erkrankung beobachtet und ist Folge einer erschöpften Atemmuskulatur.
Ist eine Ventilations-/Perfusionsinhomogenität die Ursache der Hypoxämie, so kommt es unter Belastung zu einem Anstieg des Sauerstoffpartialdruckes. In einem solchen Fall ist die möglicherweise in Ruhe zu messende Hypoxämie (in der Regel nur leichtgradig) nicht relevant für die Einschätzung der MdE. In diesem Fall stützt das beobachtete Verhalten des Sauerstoffpartialdruckes unter Belastung nur die Diagnose einer obstruktiven Atemwegserkrankung, z. B. in Folge Silikose.
Kommt es unter Belastung zu einem Abfall des Sauerstoffpartialdruckes, so ist dies Ausdruck einer für Sauerstoff relevanten Diffusionsstörung, z. B. in Folge eines Lungenemphysems, einer Fibrose oder einer Alveolitis. Signifikant ist ein Abfall des Sauerstoffpartialdruckes nur bei einem Abfall von 5 mm g und unter den altersentsprechenden Sollgrenzwert (65–70 mmHg). Das Erreichen des Steady State ist für eine valide Aussage unbedingt erforderlich, ebenso das Erreichen einer submaximalen Belastung.
Sowohl in Ruhe als auch unter Belastung muss für die adäquate Einschätzung des P a,O2 die Ventilationsarbeit, d. h. der P a,CO2 berücksichtigt werden. Nicht selten findet sich bei Patienten mit Silikose eine leichte Hyperventilation bereits in Ruhe. Diese gibt es aber auch nicht selten bei Patienten ohne Silikose. Auch Gesunde (v. a. Raucher, Übergewichtige) können leichte Ventilations-Perfusions-Inhomogenitäten und damit eine irrelevante Hypoxämie aufweisen. Eine körperliche Belastung minimiert die Ventilations-Inhomogenitäten. Bleibt die Hypoxämie bestehen, kann unter Berücksichtigung der individuellen Pathophysiologie in den so genannten Standard-P a,O2 umgerechnet werden:
P a,O2 Standard = P a,O2 aktuell – 1,66 x (40 – P a,CO2 aktuell) [134].
Eine anhaltende Hypoxie und Hyperventilation unter Belastung weisen auf eine respiratorische Insuffizienz hin.
Mittels der kardiopulmonalen Funktionsdiagnostik lässt sich die Dyspnoe in der Regel pulmonalen und/oder kardialen Ursachen zuordnen. Der nachgewiesene Grad von Obstruktion, Blähung, Einschränkung von CO-Diffusionskapazität und Gasaustausch ist Grundlage der Bewertung der Leistungseinschränkung. Sofern eine Einschränkung der Funktionsbefunde nicht nachweisbar ist, liegen keine Leistungseinschränkungen im Sinne einer Minderung der Erwerbsfähigkeit vor (vgl. 6.4).
Die Plausibilität der Befunde muss durch den ärztlichen Sachverständigen überprüft werden. Dies gilt insbesondere für das Verhalten des Sauerstoffpartialdruckes in Ruhe und unter Belastung im Vergleich zu der CO-Diffusionskapazität. So ist z. B. ein Abfall des Sauerstoffpartialdruckes unter Belastung nicht plausibel als Folge einer Silikose zu erklären, wenn die CO-Diffusionskapazität als normal bestimmt wurde. Die Messung der CO-Diffusionskapazität muss als besonders sensitiv angesehen werden. Dies bedeutet, dass eine leichte Einschränkung der D L,CO nicht immer mit einer auch für Sauerstoff relevanten Diffusionsstörung einhergeht, insbesondere dann, wenn aus anderen Gründen keine Submaximalbelastung oder kein Steady State erreicht wird. Die klinische Relevanz einer Diffusionsstörung wird aber durch einen Abfall des Sauerstoffpartialdruckes unter Belastung besonders deutlich. Der Transferkoeffizient K CO (entspricht dem volumenkorrigierten Transferfaktor) korreliert besonders gut mit der emphysembedingten Reduktion des Gasaustausches. Wird auf eine Belastungsuntersuchung verzichtet, so muss dies vom ärztlichen Sachverständigen entsprechend begründet werden (z. B. schlechter Allgemeinzustand, Komorbiditäten wie kardiovaskuläre Erkrankungen).
Für die Beurteilung der Lungenfunktionswerte sind der intraindividuelle Verlauf sowie aktuelle und valide Referenzwerte zu Grunde zu legen; Letzteres gilt insbesondere für Grenzbefunde [130]. Die Lungenfunktionsreferenzwerte [113] sind mit Hilfe einer im Internet frei verfügbaren Software zu berechnen ( www.ers-education.org/guidelines/global-lung-function-initiative/tools.aspx ).
Bei Diskrepanzen zwischen dem Lungenfunktionsbefund und der klinischen Anamnese wie auch bei differenzialdiagnostischen Fragestellungen (z. B. kardial oder pulmonal bedingte Luftnot) muss ggf. die Diagnostik erweitert werden (z. B. D-Dimere, BNP, Spiroergometrie, Echokardiographie, Rechtsherzkatheter).
Hierzu können Befunde der Klinischen Chemie (z. B. Anämie, Entzündungsparameter) hilfreich sein. Auch müssen insbesondere pulmonal-vaskuläre Ursachen erwogen werden. Die Abklärung erfolgt nach dem diagnostischen Algorithmus für pulmonal-arterielle Hypertonie, der 2013 auf der Nizza-Konferenz festgelegt wurde [135]. Darin wird festgelegt, dass die pulmonale Hypertonie weiterhin anhand eines mittleren pulmonal-arteriellen Drucks 25 mmHg in Ruhe, gemessen während einer Rechtsherzkatheter-Untersuchung, definiert ist.
Wegen ihres häufigen Auftretens sind neben kardialen Ursachen der Dyspnoe auch Lungenembolien besonders zu berücksichtigen, und gegebenenfalls differenzialdiagnostisch abzugrenzen. Auch hierzu können Befunde der Klinischen Chemie (z. B. Anämie, Entzündungsparameter, BNP oder NT-proBNP) hilfreich sein. Sofern diese Untersuchungen andere Erkrankungen als die Silikose als Ursachen des Beschwerdebildes wahrscheinlich machen und eine Silikose sicher ausschließen, kann die gutachterliche Diagnostik an dieser Stelle beendet werden. Die versicherte Person sollte mit der Empfehlung zu einer weiterführenden Abklärung über das Ergebnis der Untersuchungen informiert werden. Der weiterbehandelnde Arzt sollte eine entsprechende Information erhalten, wenn die versicherte Person damit einverstanden ist.
Sofern auch nach den Befunden der erweiterten Diagnostik anderen als den beruflichen Ursachen keine überragende Bedeutung zukommt (vgl. 3.4) und relevante Einschränkungen der kardiopulmonalen Funktionen nachgewiesen wurden, ist der Leistungsfall einer BK Nr. 4101 zu bejahen. In diesem Fall ist das gesamte Ausmaß der Funktionseinschränkungen als BK-Folge zu bewerten und dementsprechend die Bewertung der MdE vorzunehmen.
6.3 Zusammenhangsbeurteilung
Der ärztliche Sachverständige kann das Vorliegen des Versicherungsfalles einer BK Nr. 4101 als hinreichend wahrscheinlich (bewiesen) ansehen, wenn die gefährdende Tätigkeit durch Vorermittlungen und Anamneseerhebung widerspruchsfrei belegt ist und sich aus dem Befund der Thoraxübersichtsaufnahme mit einer Streuungskategorie von mindestens 1/1 und/oder auch des qualifizierten Low-Dose-Volumen-CT sowie ggf. durch ergänzende Untersuchungsergebnisse (pathologisch-anatomische Befunde) keine Zweifel an dem Vorliegen einer Silikose begründen lassen.
Da mittlerweile die CT-Diagnostik als im Vergleich zur konventionellen Röntgendiagnostik sensitivere und spezifischere Methode zunehmend zum Einsatz gelangt, kann eine Silikose/Mischstaubpneumokoniose primär auch im CT im Kontext mit der Arbeitsanamnese und sicherheitstechnischen Expositionsermittlung gesichert und anhand der Vorgaben der Internationalen CT-Klassifikation semiquantitativ beschrieben werden [136, 118]. Nach computertomographischen Befunden ist eine Silikose als gesichert anzusehen, wenn in beiden Oberfeldern im Lungenkern und/oder im Lungenmantel scharf berandete rundliche Verschattungen nachweisbar sind, die im Vergleich mit dem Referenzfilm jeweils mindestens die Streuung 1 erreichen (Gesamtstreuung mindestens 2) [121].
Das pathologisch-anatomische Grading der (Anthrako-)Silikose sollte nach den Kriterien von Könn et al. [8] und Hnizdo et al. [122] erfolgen. Neben dem Grading sind sämtliche indirekten Folgen der (Anthrako-)Silikose, wie z. B. ein Lungenemphysem, eine chronische und/oder exazerbierte Bronchitis/Pneumonie (COPD?), morphologische Zeichen einer pulmonalen Hypertonie, Zeichen einer Rechtsherzhypertrophie/-belastung/-insuffizienz und deren Folgen, z. B. Mobilitätsverlust/Bettlägerigkeit, venöse Thromboseneigung/frischere oder abgelaufene Thrombembolien zu berücksichtigen.
6.4 Zuordnung der Funktionseinschränkungen zur Silikose
Bei Bejahung des Versicherungsfalls ist zu prüfen und zu begründen, ob und ggf. welche der objektivierten Funktionseinschränkungen auf die diagnostizierte Silikose (s. 6.2.2) mit Wahrscheinlichkeit (s. 3.3.3) zurückgeführt werden können. Soweit relevante Einschränkungen der kardiopulmonalen Funktionen nachgewiesen wurden und auf die Silikose zurückzuführen sind, handelt es sich um Folgen der BK, die der Ermittlung der MdE (s. 6.5) zugrunde zu legen sind. Beschwerden, die nach den Befunden der erweiterten Diagnostik (s. 6.2.) auf andersartigen Ursachen beruhen, kommen nicht als Folgen der BK in Betracht.
Die unter 6.1 (Vorermittlungen) aufgeführten Vorbefunde müssen vollständig eingeholt und in der Zusammenhangsbeurteilung berücksichtigt werden. Entsprechendes gilt für Arztberichte und Untersuchungsbefunde, soweit sie sich auf das Atmungsorgan beziehen und/oder für die Fragestellung relevant sind. Ebenso ist der Bericht des Präventionsdienstes des UV-Trägers zu berücksichtigen.
Radiologische und/oder pathologisch-anatomische Nachweise silikotischer Lungenveränderungen sind Voraussetzung für die Anerkennung der Berufskrankheit Nr. 4101. Aufgabe des ärztlichen Sachverständigen ist es, BK-bedingte Krankheitssymptome und Funktionseinschränkungen (Restriktion, Obstruktion, Gasaustauschstörung) zu objektivieren, zu quantifizieren und mit dem Beweismaß der Wahrscheinlichkeit als ursächlich zuzuordnen.
Neben der objektivierten arbeitsbedingten Belastung, der Arbeitsanamnese, dem Krankheitsverlauf, den ärztlichen Vorbefunden, dem konventionellen Röntgenthorax-Befund ergänzt durch das qualifizierte Low-Dose-Volumen-HRCT sowie ggf. weitergehenden Untersuchungsergebnissen, sind Confounder wie Inhalationsrauchen (Packyears), Atemwegsallergien, Systemerkrankungen und andere arbeitsbedingte und nicht arbeitsbedingte Erkrankungen zu berücksichtigen und soweit möglich bezüglich ihrer funktionellen Auswirkungen abzugrenzen. Der medizinische Sachverständige muss sich dabei an den Qualitätsstandards der medizinisch-wissenschaftlichen Fachgesellschaften orientieren und sich regelmäßig fortbilden.
Hinsichtlich des Zusammenhangs zwischen der Belastung gegenüber silikogenen alveolengängigen Stäuben und den dadurch bedingten Gesundheitsstörungen sind die unter 3. bis 5. dargestellten berufskrankheiten- und versicherungsrechtlichen Grundlagen sowie klinischen und medizinisch-wissenschaftlichen Kenntnisse von Bedeutung.
6.5 Minderung der Erwerbsfähigkeit (MdE)
Der ärztliche Sachverständige ermittelt die medizinisch-funktionellen Grundlagen der Minderung der Erwerbsfähigkeit und macht einen hierauf beschränkten Vorschlag zur Bemessung der MdE. Es wird auf Tabelle 13 verwiesen. Die MdE-Tabelle gibt eine Orientierung für die Abstufung der MdE-Prozentsätze, die – den individuellen Gegebenheiten entsprechend – Entscheidungsspielräume belässt. Es ist der medizinisch-funktionelle Anteil der MdE zu ermitteln und zu begründen, für den die Mehrheit der Einzelangaben und -messwerte spricht.
Im Gutachten ist die Ableitung der hierauf beschränkten MdE unter Nennung und Diskussion aller Teilbereiche der Tabelle konkret darzustellen. Besonders zu achten ist auf die Plausibilität der Beschwerdeangaben im Vergleich mit klinischen und funktionsdiagnostischen Befunden. Bei der Bewertung der spirometrischen Befunde werden die Referenzwerte von Quanjer et al. [113] zugrunde gelegt (s. auch Leitlinie Spirometrie [130]). Die Festsetzung des MdE-Grades ist Aufgabe des Unfallversicherungsträgers bzw. des Rentenausschusses; der MdE-Grad bemisst sich gem. § 56 Abs. 2 SGB VII danach, in welchem Umfang durch die Beeinträchtigung des körperlichen und geistigen Leistungsvermögens die Arbeitsmöglichkeiten auf dem gesamten Gebiet des Erwerbslebens vermindert sind. Weitergehende Aspekte sind der Bochumer Empfehlung [137] zu entnehmen.
7 Hinweise zu weiteren Heilbehandlungsmaßnahmen bei Vorliegen des Versicherungsfalls
Maßnahmen der Rehabilitation mit ihren inhaltlichen Schwerpunkten wie optimierte medikamentöse Therapie, Patientenschulung, Trainingstherapie, physikalische Therapie und Selbsthilfetechniken sind heute wissensbasiert und wesentlicher Anteil einer leitliniengerechten Therapie der Begleit-COPD bei Silikose. Die Entwicklung von Standards der stationären wie auch der ambulanten Rehabilitation bei Begleit-COPD bei Silikose stellt für beide Verfahrensweisen im Wesentlichen gleiche Inhalte dar (siehe BAR-Richtlinien [138]).
7.1 Ziele der Silikose-Rehabilitation (s. auch Bochumer Empfehlung)
Die häufigsten Symptome bei Versicherten mit Silikose sind Husten, Auswurf und Luftnot. Beginnend mit der Luftnot droht eine Abnahme der körperlichen Leistungsfähigkeit und damit der Lebensqualität ( Abb. 2 ).
Ziel der Rehabilitation ist, diese Dekonditionierungsspirale möglichst frühzeitig zu unterbrechen, d. h. die körperliche Belastbarkeit zu steigern, die Symptome (Husten, Atemnot, Ängste, Depressionen) zu lindern und damit die Lebensqualität der Versicherten zu verbessern. Maßnahmen der Rehabilitation mit ihren inhaltlichen Schwerpunkten wie optimierte medikamentöse Therapie, Patientenschulung, Trainingstherapie, physikalische Therapie und Selbsthilfetechniken sind heute wissensbasiert und dienen dazu, die Ziele der Rehabilitation zu erreichen. Exazerbationen bronchialer Infekte und anderen Komplikationen soll vorgebeugt und eine drohende Beeinträchtigung der Teilhabe am Leben in der Gesellschaft abgewendet werden.
Gerade für die Rehabilitation bei COPD sind nach GOLD (Global Strategy for the Diagnosis, Management and Prevention of Chronic obstructive pulmonary disease, up date [139]) gesicherte Effekte nachgewiesen für
Besserung der körperlichen Leistungsfähigkeit (Evidenz Grad A)
Besserung der krankheitsspezifischen Lebensqualität (Evidenz Grad A)
Reduktion der Anzahl und Dauer von Krankenhausaufenthalten (Evidenz Grad B).
7.2 Auswahlkriterien für stationäre/ambulante Rehabilitationsmaßnahmen
Bei anerkannten Berufskrankheiten nach Nrn. 4101 und 4102 der BKV sind bei Atembeschwerden und/oder Funktionseinschränkungen therapeutische Maßnahmen, ggfs. auch Heilverfahren angezeigt. Eine Silikose kann auch nach Beendigung der Exposition fortschreiten. Ist die Silikose mit einer COPD vergesellschaftet, ist die Indikation für Rehabilitationsmaßnahmen in Abhängigkeit vom Schweregrad der Erkrankung regelmäßig zu prüfen. Zur Verbesserung der Nachhaltigkeit der Effekte wird zudem eine Überleitung der Versicherten in heimatnahe Lungensportgruppen angestrebt. Die Entscheidung, ob eine Rehabilitation ambulant oder stationär in Betracht kommt, ist neben der Rehabilitationsfähigkeit (s. unten) abhängig von der medizinischen Überwachungsbedürftigkeit, den Begleiterkrankungen, vom sozialen Umfeld, den berechtigten Wünschen des Rehabilitanden und dem Vorhandensein einer den Qualitätskriterien entsprechenden Einrichtung (BAR-Richtlinien [138] zur ambulanten pneumologischen Rehabilitation).
Die Indikation zur Teilnahme an einer stationären Maßnahme ist bei Erkrankten mit gesicherter Silikose und therapeutisch angehbaren Funktionsstörungen zu bejahen, es sei denn die Rehabilitationsfähigkeit ist insbesondere unter folgenden Gesichtspunkten nicht gegeben:
dekompensierte Herzinsuffizienz,
instabile Angina pectoris,
kürzlich durchgemachter Myokardinfarkt,
offene Tuberkulose,
schwere Bewegungseinschränkungen (orthopädisch oder neurologisch),
geistige und psychische Unfähigkeit, am Schulungsprogramm teilzunehmen.
Neben den medizinischen Voraussetzungen muss der Rehabilitand für eine ambulante Rehabilitation
über die zur Inanspruchnahme der Rehabilitation erforderliche Mobilität und physische und psychische Belastbarkeit verfügen,
die ambulante Rehabilitationseinrichtung in einer zumutbaren Fahrzeit erreichen können,
über eine durchgängige Kooperations-, Handlungs- und Lernfähigkeit verfügen und
über eine ausreichende Compliance und Motivation/Motivierbarkeit verfügen.
Die häusliche Versorgung des Rehabilitanden sowie seine sonstige medizinische Versorgung müssen sichergestellt werden.
8 Kurzfassung
Die Literaturauswertung ergibt weitestgehend konsistent, dass zwischen dem anhand der Thoraxübersichtsaufnahme ermittelten Streuungsgrad der Silikose nach ILO [2] und der Schwere der Symptomatik und der Funktionsausfälle keine strengen Korrelationen bestehen. Bereits in niedrigen Streuungskategorien können Symptome und Funktionsausfälle auftreten. Ebenso wurde konsistent gefunden, dass die Funktionseinschränkungen eng mit dem Emphysem und nicht dem Streuungsgrad silikotischer Herdsetzungen assoziiert sind. Daraus ergibt sich, dass die Moerser Konvention mit ihrem Abschneidekriterium bei dem Streuungsgrad nach ILO [2] 2/2 wissenschaftlich nicht begründet ist.
Bei der gutachterlichen Prüfung des Versicherungsfalls ist zu beachten, dass die Thoraxübersichtsaufnahme eine geringe Sensitivität aufweist, auch ihre eingeschränkte Spezifität ist zu berücksichtigen. Bei gesicherter Exposition ist in der Erstbegutachtung daher ein qualifiziertes Low-Dose-Volumen-HRCT des Thorax obligatorisch.
Bei Vorliegen einer Silikose jeglicher, auch geringer, Streuungskategorien ist eine qualitätsgesicherte standardisierte Diagnostik (siehe Abb. 1, Diagnostikschema) indiziert. Dabei sind die radiologischen Befunde, insbesondere aber auch das Beschwerdebild, z. B. Verlauf und Ausmaß von Dyspnoe, zu erfassen und das Ausmaß der Funktionsstörung (u. a. Restriktion, Obstruktion, Gasaustauschstörung) zu objektivieren.
Die Begutachtung erfordert deshalb – nicht zuletzt auch aus differenzialdiagnostischen Gründen – eine umfassende Funktionsprüfung des kardiopulmonalen Systems einschließlich Bestimmung der CO-Diffusionskapazität, des Gasaustausches unter Belastung sowie nach Möglichkeit auch eine Spiroergometrie.
Für die Zusammenhangsbegutachtung gilt der Beweismaßstab der hinreichenden Wahrscheinlichkeit. Bei den Funktionsausfällen ist zu beurteilen, ob und in welchem Umfang sie Folge der festgestellten Silikose sind. Hierbei ist häufig zu prüfen, ob konkurrierende Faktoren ggf. überragende Bedeutung für die Verursachung der Funktionsausfälle haben. Dies gilt insbesondere für die Abgrenzung der Funktionseinschränkung durch andere Erkrankungen und – soweit möglich – des Zigarettenrauchens.
Der medizinisch-funktionelle Anteil der MdE ist integrativ aus dem Schweregrad des Beschwerdebildes und der einzelnen funktionellen Einschränkungen zu ermitteln und zu quantifizieren (s. Tabelle 13).
Verfahren zur Konsensbildung
Das Update der Leitlinie wurde im Auftrag der Deutschen Gesellschaft für Pneumologie und Beatmungsmedizin sowie der Deutschen Gesellschaft für Arbeitsmedizin und Umweltmedizin unter Beteiligung der Deutschen Gesellschaft für Pathologie und der Deutschen Röntgengesellschaft erstellt.
Es wurde in einem nominalen Gruppenprozess bei einem Treffen der Mitglieder der Leitliniengruppe (07.10.2014, Frankfurt/Main) sowie im schriftlichen Abstimmungsverfahren von den nachfolgend genannten Experten entsprechend den Empfehlungen der AWMF unter Moderation des unabhängigen Priv. Doz. Dr. H. Sitter erarbeitet. Die Koordination lag bei Herrn Prof. Dr. med. X. Baur. Protokollführerin war Frau Dr. med. Gertrud Michaely.
Beteiligte Experten:
Prof. Dr. med. Xaver Baur, Deutsche Gesellschaft für Pneumologie und Beatmungsmedizin
Prof. Dr. med. Rainer M. Bohle, Deutsche Gesellschaft für Pathologie
Dr. med. Michael Heger, Vereinigung Deutscher Staatlicher Gewerbeärzte
Bernhard Heise (Patientenvertretung)
Dr. med. Kurt Georg Hering, Deutsche Röntgengesellschaft e.V.
Priv.-Doz. Dr. med. Karina Hofmann-Preiss, Deutsche Röntgengesellschaft e.V.
Prof. Dr. med. Thomas Kraus, Deutsche Gesellschaft für Arbeitsmedizin und Umweltmedizin
Prof. Dr. med. Dennis Nowak, Deutsche Gesellschaft für Arbeitsmedizin und Umweltmedizin
Melanie Duell, Deutsche Gesetzliche Unfallversicherung
Stefanie Palfner, Deutsche Gesetzliche Unfallversicherung
Dr. med. Gertrud Michaely, Vereinigung Deutscher Staatlicher Gewerbeärzte
Dr. med. Irene Özbek, Vereinigung Deutscher Staatlicher Gewerbeärzte
Prof. Dr. med. Andrea Tannapfel, Deutsche Gesellschaft für Pathologie
Prof. Dr. med. Helmut Teschler, Deutsche Gesellschaft für Pneumologie und Beatmungsmedizin
Dr. med. Thomas Voshaar, Deutsche Gesellschaft für Pneumologie und Beatmungsmedizin
Danksagung: Prof. Dr. R. Merget und Frau Dr. N. Kotschy-Lang wird für großteils übernommene frühere Beiträge gedankt. Außerdem wird Frau Dr. G. Michaely und Dr. I. Özbek für die Protokollführung gedankt.
Erstelldatum der Erstfassung: 22.9.2008
Datum der Fertigstellung der Überarbeitung: August 2016
Überprüfung geplant: Oktober 2020
Für die Verfasser
Prof. Dr. med. Xaver Baur
Charité – Universitätsmedizin Berlin
Campus Benjamin Franklin
Thielallee 69
14195 Berlin
Zitierte und weiterführende Literatur
Berufskrankheitenverordnung (BKV) www.baua.de/de/Publikationen/Faltblaetter/F3.pdf?__blob=publicationFile
International Labour Office (ILO). Guidelines for the use of the ILO international classification of radiographs of pneumoconioses. 2000 edition. Geneva: International Labour Office, 2002 (Occupational Safety and Health Series No. 22 [Rev. 2000])
Deutsche gesetzliche Unfallversicherung (DGUV). Reichenhaller Empfehlung. Begutachtungsempfehlungen für die Berufskrankheiten der Nrn. 1315 (ohne Alveolitis), 4301 und 4302 der Anlage zur BKV. Meckenheim: DCM-Druck Center, 2012
Bundesministerium Arbeit und Soziales, BArbBl 1998; (4) S. 61
Bundessozialgericht Entscheidungen Bd. 12, S. 242–247, 2 RU 86/56 om 30.6.1960
Becker P. Gesetzliche Unfallversicherung. Arbeits- und Wegeunfälle, Berufskrankheiten. München: Deutscher Taschenbuchverlag; 2004: 35 (dtv Beck Rechtsberater 50628)
Hauptverband der gewerblichen Berufsgenossenschaften (HVBG). Empfehlungen der Unfallversicherungsträger zur Begutachtung bei Berufskrankheiten. Meckenheim: DCM-Druck Center, 2004
Könn G, Schejbal V, Oellig WP. Die pathologische Anatomie der Pneumokoniosen. In: Ulmer WT, Reichel G, Hrsg. Pneumokoniosen. Berlin, Heidelberg, New York: Springer, 1976: 101–135 (Schwiegk H, ed. Handbuch der inneren Medizin. 4. Bd, Teil 1: Erkrankungen der Atmungsorgane, 5. Aufl.)
Weill H, Jones RN, Parkes W. Silicosis and related diseases. In: Parkes WR, eds. Occupational lung disorders. 3. Aufl. Oxford: Butterworth-Heinemann, 1994: 285–339
Hering KG, Jacobsen M, Borsch-Galetke E et al. Die Weiterentwicklung der Internationalen Staublungenklassifikation – von der ILO 1980 zur ILO 2000 und zur ILO 2000/Version Bundesrepublik Deutschland. Pneumologie 2003; 57: 576-84
Hnizdo E, Murray J, Davison A. Correlation between autopsy findings for chronic obstructive lung disease and in-life disability in South African gold miners. Int Arch Occup Environ Health 2000; 73: 235-244
Remy-Jardin M, Degreef JM, Beuscart R et al. Coal Worker’s Pneumoconiosis: CT Assessment in Exposed Workers and Correlation with Radiographic Findings. Radiology 1990; 177: 363-371
Hnizdo E, Murray J, Sluis-Cremer GK, Thomas RG. Correlation between radiological and pathological diagnosis of silicosis: An autopsy population based study. Am J Ind Med 1993; 24; 427-445
Bauer TT, Merget R, Schmidt EW et al. Korrelation radiologischer und pathologisch-anatomischer Befunde bei Mischstaub-Pneumokoniosen ehemaliger Kohlebergarbeiter. Pneumologie 1997; 51: 1093-1097
Remmele et al. Pathologie Rechtsfragen der Pathologie, Einführung in die bioptische Diagnostik, Herz- und Gefäßsystem, Hämatologie, Atmungsorgane. (Bd. 1): Springer 1984
Reichel G. Pneumokoniosen durch anorganische Stäube. In: Ferlinz R, Hrsg. Pneumologie in Praxis und Klinik. Stuttgart, New York: Thieme, 1994: 581-608
Baur X. Durch berufliche Noxen ausgelöste Atemwegs- und Lungenkrankheiten. In: Matthys H, Seeger W, Hrsg. Klinische Pneumologie. 4. Aufl. Heidelberg, Springer 2008
McCormic, Khuder SS, Aryal BK et al. Occupational silica exposure as a risk factor for skleroderma: a meta-analysis. Int Arch Occup Environ Health 2010 Oct; 83 (7) 763–769)
Tioe Nij E, Heederik D. Risk assessment of silicosis and lung cancer among construction workers exposed to respirable quartz, Scand J Work Environ Health 2005; 31: 49-55 (Suppl. 2)
Müller KM, Wiethege T. Quarz und Lungentumoren – Daten und Fakten des Pathologen. Pneumologie 2000; 54: 24-31
Mossman BT, Churg A. Mechanism in the pathogenesis of asbestosis and silicosis. Am J Repir Crit Care Med 1998; 157: 1666–1680
Donaldson K, Borm PJ. The quartz hazard: A variable entity. Ann Occup Hyg 1998; 5: 287–294
Fubini B, Hubbard A. Reactive oxygen species (ROS) and reactive nitrogen species (RNS) generation by silica in inflammation fibrosis. Free Radic Biol Med 2003; 34: 1507–1516
Rimal B, Greenberg AK, Rom WN. Basis pathogenic mechanism in silicosis: current understanding. Curr Opin Pulm Med 2005; 11: 1169–1173
Hamilton RF, Thakur SA, Holian A. Silica binding and toxicity in alveolar macrophages. Free Radic Biol Med 2008; 44: 1246–1258
diBiasi W. Zur pathologischen Anatomie der Silikose. Verh Dtsch Ges Path 1949; 44: 371–377
Fujimura N. Pathology and pathophysiology of pneumoconiosis. Curr Opin Pulm Med 2000; 6: 140–144
Deutsche Forschungsgemeinschaft (DFG). Quarz-Feinstaub und Quarz-haltiger Feinstaub. In: Henschler D, Hrsg. Gesundheitsschädliche Arbeitsstoffe, Toxikologisch-Arbeitsmedizinische Begründung von MAK-Werten. Weinheim: Wiley-VCH, 1971: 1–21
Deutsche Forschungsgemeinschaft (DFG). Quarz-Feinstaub und Quarz-haltiger Feinstaub – Nachtrag. In: Henschler D, Hrsg. Gesundheitsschädliche Arbeitsstoffe, Toxikologisch-Arbeitsmedizinische Begründung von MAK-Werten. Weinheim: Wiley-VCH, 1984: 1-8
Worth G, Schiller E. Die Pneumokoniosen. Köln: Staufen Verlag, 1954
Reichel G. Die Silikose (Anthrakosilikose). .In: Ulmer WT, Reichel G, Hrsg. Pneumokoniosen. Berlin, Heidelberg, New York: Springer, 1976:159–320 (Schwiegk H, Hrsg. Handbuch der inneren Medizin. 4. Bd, Teil 1: Erkrankungen der Atmungsorgane, 5. Aufl).
Eibel R, Weber A, Stolpe S, Hellenbrand U, Bauer T. Zusammenhang zwischen Emphysemtyp und Schweregrad der Pneumokoniose bei Bergleuten: Korrelation von HR-CT-Befunden und ILO-Klassifikation. Fortschr Röntgenstr 2002; 174: 846–853
Coggon D, Newman Taylor A. Coal mining and chronic obstructive pulmonary disease: a review of the evidence. Thorax 1998; 53: 398–407
Baur X, Hillenbach C, Degens P. Literaturstudie „Chronische Bronchitis und Emphysem – eine Berufskrankheit der Bergleute?“ Bochum: Eigendruck BGFA, 1994
Baur X, Köhler D, Voshaar T. Positionspapier der Deutschen Gesellschaft für Pneumologie zur Begutachtung der Silikose. Pneumologie 2005; 59: 549–553
Morfeld P, Vautrin HJ, Kösters A et al. Components of coal mine dust exposure and the occurence of pre-stages of pneumoconiosis. J Appl Occup Environ Hyg 1997; 12: 973–979
Oxman AD, Muir DC, Shannon HS et al. Occupational dust exposure and chronic obstructive pulmonary disease. A systematic overview of the evidence. Am Rev Respir Dis 1993; 148 (1): 38–48
Seixas NS, Robins TG, Attfield MD et al. Exposure-response relationships for coal mine dust and obstructive lung disease following enactment of the Federal Coal Mine Health and Safety Act of 1969. Am J Ind Med 1992; 21 (5): 715–734
Carta R, Aru G, Barbieri MT et al. Dust, exposure, respiratory symptoms, and longitudinal decline of lung function in young coal miners. Occup Environ Med 1996; 53: 312–319
Smidt U. Distribution of inhaled air in coal workers with and without silicosis. Rev Inst Hyg Mines (Hasselt) 1974: 29: 72–84
Marine WM, Gurr D, Jacobsen M. Clinically important respiratory effects of dust exposure and smoking in British coal miners. Am Rev Respir Dis 1988; 137: 106–112
Collins HP, Dick JA, Bennett JG et al. Irregularly shaped small shadows on chest radiographs, dust exposure, and lung function in coalworkers‘ pneumoconiosis. Br J Ind Med 1988; 45: 43–55
Lewis S, Bennett J, Richard K et al. A cross sectional study of the independent effect of occupation on lung function in British coal miners. Occup Environ Med 1996; 53: 575–576
Wang X, Yu ITS, Wong TW et al. Respiratory symptoms and pulmonary function in coal miners: Looking into the effects of simple pneumoconiosis. Am J Indust Med 1999a; 35: 124–131
Soutar CA, Hurley JF. Relation between dust exposure and lung function in miners and ex-miners. Br J Ind Med 1986; 43: 307–20
Henneberger PK, Attfield MD. Coal mine dust exposure and spirometry in experienced miners. Am J Respir Crit Care Med 1996; 153: 1560–1566
Leung CC, Chang KC, Law WS et al. Determinants of spirometric abnormalities among silicotic patients in Hong Kong. Occup Med (Lond) 2005; 55: 490–493
Cockcroft A, Berry G, Cotes JE et al. Shape of small opacities and lung function in coalworkers. Thorax 1982; 37: 765–769
Lapp NL, Morgan WK. Cardio-respiratory function in United States coal workers. Bull Physiopath Respir (Nancy) 1975; 11: 527–559
Nemery B, Veriter C, Brasseur L et al. Impairment of ventilator function and pulmonary gas exchange in non-smoking coalminers. Lancet 1987; 2 (8573): 1427–1430
Gevenois PA, Sergent G, De Maertelaer V et al. Micronodules and emphysema in coalmine dust or silica exposure: relation with lung function. Eur Respir J 1998; 12: 1020–1024
Cowie HA, Miller BG, Rawborne RG et al. Dust related risks of clinically relevant lung functional deficits. Occup Environ Med 2006; 63: 320–325
Attfield MD, Hodous T. Pulmonary function of US coal miners related to dust exposure estimates. Am Rev Respir Dis 1992; 145: 605–609
Carstens M, Brinkmann O, Lange HJ et al. Beiträge zur Pathophysiologie der Staublungenkrankheit im Bergbau. III. Mitt. Arch Gewerbepath Gewerbehyg 1958; 16: 459–477
Hnizdo E. Loss of lung function associated with exposure to silica dust and with smoking and its relation to disability and mortality in South African gold miners. Br J Ind Med 1992; 49 (7): 472–479
Hnizdo E, Vallyathan V. Chronic obstructive pulmonary disease due to occupational exposure to silica dust: a review of epidemiological and pathological evidence. Occup Environ Med 2003; 60: 237–243
Neukirch F, Cooreman J, Korobaeff M et al. Silica exposure and chronic airflow limitation in pottery workers. Arch Environ Health 1994; 49: 459–464
Ulvestad B, Bakke B, Eduard W et al. Cumulative exposure to dust causes accelerated decline in lung function in tunnel workers. Occup Environ Med 2001; 58: 663–669
Green DA, McAlpine G, Semple S, Cowie H, Seaton A. Mineral dust exposure in young Indian adults: an effect on lung growth? Occup Environ Med 2008; 65(5):306–310
Neghab M, Choobineh A. Work-related respiratory symptoms and ventilator disorders among employees of a cemet industry in Shiraz, Iran. J Occup Health 2007; 49: 273–278
Ooi GC, Tsang KWT, Cheung TF et al. Silicosis in 76 men: Qualitative and quantitative CT evaluation – clinical-radiologic correlation study. Radiology 2003; 228: 816–825
Wang X, Yano E. Pulmonary dysfunction in silica-exposed workers: A relationship to radiographic signs of silicosis and emphysema. Am J Ind Med 1999b; 36: 299–306
Koskinen H. Symptoms and clinical findings in patients with silicosis. Scand J Work Environ Health 1985; 11: 101–106
Deutsche Forschungsgemeinschaft (DFG). Arbeitsmedizinische Querschnittsuntersuchungen zur Bedeutung chronischer inhalativer Belastungen für das bronchopulmonale System. Forschungsbericht chronische Bronchitis und Staubbelastung am Arbeitsplatz. Boppard: Harald Bolt Verlag, 1975
Deutsche Forschungsgemeinschaft (DFG). Steinkohlengrubenstaub. In: Greim H, Hrsg. Gesundheitsschädliche Arbeitsstoffe. Toxikologisch-arbeitsmedizinische Begründungen von MAK-Werten. Weinheim: Wiley-VCH, 1998: 1-51
Rogan JM, Attfield MD, Jacobsen M et al. Role of dust in the working environment in development of chronic bronchitis in British coal miners. Br J Ind Med 1973; 30: 217–226
Seixas NS, Robins TG, Attfield MD et al. Longitudinal and cross sectional analyses of exposure to coal mine dust and pulmonary function in new miners. Br J Ind Med 1993; 50 (10): 929–937
Gamble JF, Hessel PA, Nicolich MJ. Relationship between silicosis and lung function. Scand J Work Environ Health 2004; 30: 5–20
Bundesministerium für Arbeit und Soziales. Wissenschaftliche Begründung zur BK Nr. 4111: Chronische obstruktive Bronchitis oder Emphysem von Bergleuten unter Tage im Steinkohlenbergbau bei Nachweis der Einwirkung einer kumulativen Dosis von in der Regel 100 Feinstaubjahren [(mg/m³) Jahre]. BArbBl 1995; (10): 39–45
Lange HJ, Ulm K. Mathematische Modelle zur Frage eines allgemeinen Staubgrenzwertes. Weinheim: Verlag Chemie, 1983
Lange HJ, Pache L. Bericht über Auswertungen von Daten der Knappschaftlichen Rentenversicherung (KnRV), der Arbeiterrenten- (ArV) und der Angestelltenversicherung (AnV) zur Frage von Chronischer Bronchitis (CB) und/oder Emphysem (E) als arbeitsbedingte Erkrankungen der Bergleute. Arbeitsmed Sozialmed Präventivmed 1991, Sonderheft 17: 1-46
Sircar K, Hnizdo E, Petsonk E et al. Decline in lung function and mortality: implications for medical monitoring. Occup Environ Med 2007; 64: 461–466
Kuempel ED, Staynder LT, Attfield MD et al. Exposure-response analysis of mortality among coal miners in the United States. Am J Ind Med 1995; 28: 167–184
Attfield MD, Kuempel ED. Mortality among U.S. underground coal miners: a 23-year follow-up. Am J Indus Med 2008; 51: 231–245
Baur X. Auswirkungen der Belastungen unter Tage im Steinkohlenbergbau auf die Lunge. Pneumologie 2004; 58: 107–115
Muysers K, Siehoff F, Worth G et al. Neuere Ergebnisse atemphysiologischer Untersuchungen von Kohlenbergarbeitern unter Berücksichtigung von Silikose, Bronchitis und Emphysem. I. Mitteilung. Das Verhalten der Gase im arteriellen Blut. Arch Gewerbepath Gewerbehyg 1961;18: 353–369
Worth G, Gasthaus L, Muysers K et al. Neuere Ergebnisse atemphysiologischer Untersuchungen von Kohlenbergarbeitern unter Berücksichtigung von Silikose, Bronchitis und Emphysem. Arch Gewerbepath Gewerbehyg 1961; 18: 581–595
Ulmer WT, Reichel G, Roeske G et al. Klinische und funktionsanalytische Untersuchungen bei Bergleuten mit und ohne Silikose im Vergleich zu nichtstaubexponierten Arbeitern. Int Arch Gewerbepath Gewerbehyg 1967; 23: 32–48
Ulmer WT, Reichel G, Werner U. Die chronisch obstruktive Bronchitis des Bergmannes. Untersuchungen zur Häufigkeit bei der Normalbevölkerung und bei Bergleuten. Die Bedeutung der Staubbelastung und der Einfluß des Rauchens. Int Arch Gewerbepath Gewerbehyg 1968; 25: 75–98
Reichel G. Die Bedeutung der beruflichen Staubbelastung unter Tage für die Entwicklung der obstruktiven Atemwegserkrankungen. Atemwegs-Lungenkrkh 1989; 15: 471–475
Worth G, Smidt U. Lung function in coal workers in relation to age and to size and profusion of small pneumoconiotic opacities. Rev Hyg Mines 1974; 29: 144–147
Irwig LM, Rocks P. Lung function and respiratory symptoms in silicotic and nonsilicotic gold miners. Am Rev Respir Dis 1978; 177: 429–435.
Bégin R, Ostiguy G, Cantin A et al. Bergeron D. Lung function in silica-exposed workers. A relationship to disease severity assessed by CT scans. Chest 1988; 94: 539–545
Cowie RL, Mabena SK. Silicosis, chronic airflow limitation, and chronic bronchitis in South African gold miners. Am Rev Respir Dis 1991; 143: 80–84
Cowie RL. The influence of silicosis on deteriorating lung function in gold miners. Chest 1998; 113: 340–344
Ng T-P, Chan S-L. Lung function in relation to silicosis and silica exposure in granite workers. Eur Respir J 1992; 5: 986–991
Bégin R, Filion R, Ostiguy G. Emphysema in silica- and asbestos-exposed workers seeking compensation. Chest 1995; 108: 647–655
Tjoe-Nij E, de Meer G, Smit J et al. Lung function decreases in relation to pneumoconiosis and exposure to quartz-containing dust in construction workers. Am J Ind Med 2003; 43: 574–583
Kibelstis JA. Diffusing capacity in bituminous coal mine. Chest 1973; 63: 501–504
de Castro MC, Ferreira AS, Irion KL et al. CT quantification of large opacities and emphysema in silicosis: correlations among clinical, functional, and radiological parameters. Lung. 2014 Aug; 192(4) : 543-51
Meijer E, Tjoe Nij E, Kraus T et al. Pneumoconiosis and emphysema in construction workers: results of HRCT and lung function findings. Occup Environ Med. 2011 Jul; 68 (7): 542–546
Brüske I, Thiering E, Heinrich J et al. Respirable quartz dust exposure and airway obstruction: a systematic review and meta-analysis. Occup Environ Med. 2014 Aug; 71 (8) :583-9
Blackley DJ, Halldin CN, Wang ML et al. Small mine size is associated with lung function abnormality and pneumoconiosis among underground coal miners in Kentucky, Virginia and West Virginia. Occup Environ Med. 2014; 71(10): 690–694.
Forastiere F, Goldsmith DF, Sperati A et al. Silicosis and lung function decrements among female ceramic workers in Italy. Am J Epidemiol. 2002; 156 (9): 851–856.
Tse LA, Yu ITS, Qiu H et al. Joint Effects of Smoking and Silicosis on Diseases to the Lungs. PLoS ONE 9 (8): e104494. doi:10.1371/journal.pone.0104494
Kreuzer M, Sogl M, Brüske I et al. Silica dust, radon and death from non-malignant respiratory diseases in German uranium miners. Occup Environ Med. 2013;70 (12): 869–875.
Tamura T, Suganuma N, Hering KG et al. Relationships (I) of International Classification of Highresolution
Computed Tomography for Occupational and Environmental Respiratory Diseases with the ILO International Classification of Radiographs of Pneumoconioses for parenchymal abnormalities. Industrial Health 2015, 53, 260–270
Bauer TT, Schultze-Werninghaus G, Kollmeier J et al. Functional variables associated with the clinical grade of dyspnoea in coal miners with pneumoconiosis and mild bronchial obstruction. Occup Environ Med 2001; 58: 794–799
Bauer TT, Heyer CM, Duchna HW et al. Radiological findings, pulmonary function and dyspnea in underground coal miners. Respiration 2007; 74: 80–87
Worth G. Emphysema in coal workers. Editorial. Am J Ind Med 1984; 6: 401–403
Duvenkamp I, Bauer TT, Schmidt EW et al. Submaximale spiroergometrische Belastungsuntersuchung bei Patienten mit MischstaubPneumokoniosen. Pneumologie 1998; 52: 171–177
Fletcher CM, Peto R, Tinker CM et al. The natural history of chronic bronchitis and emphysema. An 8-year study of working men in London. Oxford: Oxford University Press, 1976
Fletcher C, Peto R. The natural history of chronic airflow obstruction. Br Med J 1977; 1: 1645–1648
Jaakkola MS, Ernst P, Jaakkola JJ, N’gan’ga LW, Becklake MR. Effect of the cigarette smoking on evolution of ventilatory lung function in young adults: an eight year longitudinal study. Thorax 1991; 46: 907–913
Coggon D, Newman Taylor A. Coal mining and COPD. Thorax 1999; 54: 187–188
Montes II, Fernández GR, Reguero J et al. Respiratory disease in a cohort of 2,579 coal miners followed up over a 20-year period. Chest 2004: 126: 622–629
Kuempel ED, Wheeler MW, Smith RJ et al. Contributions of dust exposure and cigarette smoking to emphysema serverity. 2009, Am J Respir Crit Care Med. 2009 Aug 1; 180(3):257-64
Vallyathan V, Green FHY, Brower P et al. The role of coal mine dust exposure in the development of pulmonary emphysema. Ann Occup Hyg 1997; 41:352–357
Ruckley VA, Fernie JM, Chapman JS et al. Comparison of radiographic appearances with associated pathology and lung dust content in a group of coal workers. Br J Ind Med 1984a; 41: 459–467
Attfield MD, Vallyathan V, Green FHY. Radiographic appearances of small opacities and their correlation with pathology grading of macules, nodules and dust burden in the lungs. Ann Occup Hyg 1994; 38 (Suppl. 1): 782–789
Vallyathan V, Brower PS, Green FHY et al. Radiographic and pathologic correlation of coal workers pneumoconiosis. Am J Respir Crit Care Med 1996; 154: 741–748
Quanjer PH, Stanojevic S, Cole TJ et al. ERS Global Lung Function Initiative. Multi-ethnic reference values for spirometry for the 3-95-yr age range: the global lung function 2012 equations. Eur Respir J. 2012; 40 (6):1324-1343. www.ncbi.nlm.nih.gov/pmc/articles/PMC3786581/
Jones PW, Harding G, Berry P, Wiklund I, Chen WH, Kline Leidy N. Development and first validation of the COPD Assessment Test. Eur Respir J. 2009; 34 (3): 648–654.
Jones PW, Tabberer M, Chen WH. Creating scenarios of the impact of COPD and their relationship to COPD Assessment Test (CAT™) scores. BMC Pulm Med. 2011: 11: 42
Ooi CG, Silva CI, Müller NL et al. Inhalational Diseases and Aspiration. In: Müller NL, Silva CIS, eds. Imaging of the Chest. Saunders: Philadelphia 2008; 2 (15): 1117–1197
Hering KG: Inhalationsschäden. In: Freyschmidt J, Hrsg. Handbuch diagnostische Radiologie, Galanski M, Hrsg. Band Thorax. Berlin: Springer; 2003: 355–394
Chong S, Lee KS, Chung Mj et al. Comparison of Imaging and Pathologic Findings. Radiographics 2006; 26: 59–77
Hering KG, Tuengerthal S, Kraus T: Standartisierte CT/HRCT-Klassifikation der Bundesrepublik Deutschland für arbeits- und umweltbedingte Thoraxerkrankungen. Radiologe 2004; 44: 500–511
Hering KG, Kraus T: Coding CT-Classification in Occupational and Environmental Respiratory Disease (OERD). In: Kusaka, Y, Hering,KG, Parker, JE: International Classifikation of HRCT for Occupational and Environmental Respiratory Diseases. Springer Verlag Tokyo; 2005: 15–23
Hering KG, Kraus T. Bildgebende Verfahren in der Diagnostik arbeits- und umweltbedingter Erkrankungen der Atemwege, der Lunge und der Pleura. In: Letzel S, Nowak D (Hrsg.) Handbuch der Arbeitsmedizin 2013; A III-3.4.2: 29–136
Hnizdo E, Singh T, Churchyard G. Chronic pulmonary function impairment caused by initial and recurrent pulmonary tuberculosis following treatment. Thorax 2000; 55: 32–38
Honma K, Abraham JL, Chiyotani K, De Vuyst P, Dumortier P, Gibbs AR, Green FH, Hosoda Y, Iwai K, Williams WJ, Kohyama N, Ostiguy G, Roggli VL, Shida H, Taguchi O, Vallyathan V. Proposed criteria for mixed-dust pneumoconiosis: definition, descriptions, and guidelines for pathologic diagnosis and clinical correlation. Hum Pathol. 2004; 35: 1515–1523
Petsonk EL, Rose C, Cohen R. Coal mine dust lung disease. New lessons from old exposure. Am J Respir Crit Care Med. 2013; 187: 1178–1185
Deutsche Gesellschaft für Arbeitsmedizin und Umweltmedizin. Leitlinien Lungenfunktionsprüfungen in der Arbeitsmedizin, DGAUM Arbeitsmed Sozialmed Umweltmed 2005; 40:358–367
MacIntyre N, Crapo RO, Viegi G et al. Standardisation of the single-breath determination of carbon monoxide uptake in the lung. Eur Respir J 2005; 26 (4): 720–735
Miller MR, Hankinson J, Brusasco V et al. Standardisation of spirometry. Eur Respir J 2005; 26: 319–338
Pellegrino R, Viegi G, Brusasco V et al. Interpretative strategies for lung function tests. Eur Respir J 2005; 26(5): 948-968 erj.ersjournals.com/cgi/reprint/26/5/948
Worth H, Buhl R, Cegla U et al. Leitlinie der Deutschen Atemwegsliga und der Deutschen Gesellschaft für Pneumologie zur Diagnostik und Therapie von Lungenemphysem (COPD). Pneumologie 2002; 56: 704-38
Criée CP, Baur X, Berdel D et al. [Standardization of spirometry: 2015 update. Published by German Atemwegsliga, German Respiratory Society and German Society of Occupational and Environmental Medicine]. Pneumologie. 2015 Mar; 69 (3): 147–164
Holland AE, Spruit MA, Troosters T et al. An official European Respiratory Society/American Thoracic Society technical standard: field walking tests in chronic respiratory disease. EurRespir J. 2014 ;44 (6): 1428–1446.
Singh SJ, Puhan MA, Andrianopoulos V et al. An official systematic review of the European Respiratory Society/American Thoracic Society: measurement properties of field walking tests in chronic respiratory disease. Eur Respir J. 2014; 44 (6):1447–1478.
Deutsche Gesellschaft für Pneumologie und Beatmungsmedizin, Deutsche Gesellschaft für Arbeitsmedizin und Umweltmedizin. Empfehlungen zur Überarbeitung des Reichenhaller Merkblatts 2008 (s. a. Preisser A, Baur X. Reichenhaller Merkblatt – Vorschläge zur Aktualisierung. In: Baur X, Hrsg., 48. Wissenschaftliche Jahrestagung der Deutschen Gesellschaft für Arbeits- und Umweltmedizin vom 12.–15.03.2008 in Hamburg, DGAUM 2008
Diekmann M, Smidt U. Berechnung eines Standard-P aO2 in Analogie zum Standard-Bikarbonat. Atemw-Lungenkrkh 1984; 10: 248–250
Hoeper MM, Bogaard HJ, Condliffe R. Definitions and diagnosis of pulmonary hypertension. J Am Coll Cardiol. 2013 Dec 24;62 (25 Suppl):D42–50
Kim JS, Lynch DA. Imaging of Nonmalignant Occupational Lung Disease. Journal of Thoracic Imaging 2002; 17: 238–260
Bochumer Empfehlungen, DGUV, 2011, 1–57
Bundesarbeitsgemeinschaft für Rehabilitation e.V. (BAR), 2009, ISSN 0933-8462, 1–31
GOLD www.who.int/respiratory/copd/GOLD_WR_06.pdf
Arakawa H, Gevenois PA, Saito Y et al. Expiratory Thin-Section CT Assessment of Airway Obstruction. Radiology 2005; 236: 1059–1066
Attfield MD. Longitudinal decline in FEV 1 in United States coalminers. Thorax 1985; 40: 132–137
Bakke P, Baste V, Hanoa R et al. Prevalence of obstructive lung disease in a general population: relation to occupational title and exposure to some airborne agents. Thorax 1991; 46: 863–870
Balmes J, Becklake M, Blanc P et al. American Thoracic Society Statement: Occupational contribution to the burden of airway disease. Am J Respir Crit Care Med 2003; 167: 787–797
BalmesJ, Nowak D. COPD caused by occupational exposure. In: Donner CF and Carone M, eds. Clinical challenges in COPD. Oxford: Clinical Publishing; 2007: 85–95
Bergin CJ, Müller NL, Vedal S et al. CT in silicosis: Correlation with plain films and pulmonary function tests. AJR Am J Roentgenol 1986;146:477–483
Blanc PD, Torén K. Occupation in chronic obstructive pulmonary disease and chronic bronchitis: an update. Int J Tuberc Lung Dis 2007; 11: 251–257
Carstens M, Brinkmann O, Lange HJ et al. Die Staubschädigungen der Bergleute. Arch Gewerbepath Gewerbehyg 1959; 17: 67–107
Hering KG, Hofmann-Preiß K, Kraus T. Update: Standardisierte CT-/HRCT-Klassifikation der Bundesrepublik Deutschland für arbeits- und umweltbedingte Thoraxerkrankungen. Radiologe 2014; 54: 363–384
Hnizdo E, Sulivan PA, Bang KM et al. Association between chronic obstructive pulmonary disease and employment by industry and occupation in the US population: a study of data from the Third National Health and Nutrition Examination Survey. Am J Epidemiol 2002; 156: 738–746
Hnizdo E, Murray J. Risk of pulmonary tuberculosis relative to silicosis and exposure to silica dust in South African gold miners. Occup Environ Med 1998; 55: 496–502
Hnizdo E, Sluis-Cremer GK, Abramowitz JA. Emphysema type in relation to silica dust exposure in South African gold miners. Am Rev Respir Dis 1991; 143: 1241–1247
Hnizdo E, Sluis-Cremer GK, Baskind E, Murray J. Emphysema and airway obstruction in non-smoking South African gold miners with long exposure to silica dust. Occup Environ Med 1994; 51: 557–563
Kroidl RF, Nowak D, Seysen U. Bewertung und Begutachtung in der Pneumologie. Stuttgart: Thieme, 2000
Krzyzanowski M, Kauffmann F. The relation of respiratory symptoms and ventilatory function to moderate occupational exposure in a general population. Results from the French PAARC study of 16,000 adults. Int J Epidemiol 1988; 17: 397–406
Kühne W. Über Zusammenhänge zwischen Lungenemphysem und Silikose. Int Arch Gewerbepath Gewerbehyg 1963; 20: 36–40
Lebowitz M. Occupational exposures in relation to symptomatology and lung function in a community population. Environ Res 1977; 14: 56–59
Leigh J, Driscoll TR, Cole BD et al. Quantitative relation between emphysema and lung mineral content in coalworkers. Occup Environ Med 194; 51: 400–407
Liu Y, Steenland K, Rong Y et al. Exposure-Response Analysis and Risk Assessment for Lung Cancer in Relationship to Silica Exposure. A 44-Year Cohort Study of 34,018 Workers. Am J Epidemiol. 2013; 178 (9):1424–1433.
Mastrangelo G, Fedeli U, Fadda E et al. Occupational chronic obstructive pulmonary disease: Italian law (decree no. 336/1994) and epidemiological evidence. Med Lav 2004; 95: 11–16
Meyer FJ, Borst MM, Buschmann HC et al. Belastungsuntersuchungen in der Pneumologie [Exercise testing in respiratory medicine]. Pneumologie. 2013 ;67 (1): 16–34.
Morfeld P, Piekarski C. Epidemiologie der Pneumokoniose und der chronischen Bronchitis im Steinkohlenbergbau. Bundesanstalt für Arbeitsschutz und Arbeitsmedizin Dortmund, Berlin, ed. Bremerhaven: Wirtschaftsverlag N. W., 1998. (Schriftenreihe der Bundesanstalt für Arbeitsschutz und Arbeitsmedizin; Sonderschrift S45)
Nowak D. Konsensuspapier zur Begutachtung der neuen Berufskrankheit „Chronische obstruktive Bronchitis/Emphysem bei Steinkohlenbergleuten“ (BK 4111). Pneumologie 1999; 53: 150–154
Ochmann U, Kotschy-Lang N, Raab W et al. Long-term efficacy of pulmonary rehabilitation in patients with occupational respiratory diseases. Respiration. 2012; 84 (5): 396–405
Ochmann U, Jörres RA, Nowak D. Long-term efficacy of pulmonary rehabilitation: a state-of-the-art review. J Cardiopulm Rehabil Prev. 2012; 32 (3):117–126.
Ruckley VA, Gauld SJ, Chapman JS. Emphysema and dust exposure in a group of coal workers. Am Rev Respir Dis 1984b; 129: 528–532
Smidt U. Derzeitiger Stand der Begutachtung der Silikose. Prax Klin Pneumol 1987;41:616-8
Smidt U. Bericht über die 2. Arbeitstagung „Silikosebegutachtung“ im Krankenhaus Bethanien, Moers, am 7.6.1978. Prax Pneumol. 1979;33:48–51
Smidt U. Bericht über die 3. Arbeitstagung „Silikosebegutachtung“ im Krankenhaus Bethanien, Moers, am 28.10.1981. Prax Pneumol 1982; 36: 438–440
Smidt U, von Nieding G. Arbeitstagung zum Thema „Begutachtung der Silikose“ in Moers, Krankenhaus Bethanien, am 16. Juni 1976. Prax Klin Pneumol 1977; 31: 609-615
Schneider J, Arhelger R, Funk M. Spiroergometric parameters at maximal exercise testing assessed functional respiratory impairment in asbestos-induced fibrosis. Clin Respir J. 2014;8 (2):175–184.
Tamura T, Suganuma N, Hering KG et al. Relationships (I) of International Classification of High-resolution Computed Tomography for Occupational and Environmental Respiratory Diseases with the ILO International Classification of Radiographs of Pneumoconioses for parenchymal abnormalities. Ind Health. 2015; 53 (3): 260–270
Viegi G, Prediletto R, Paoletti P et al. Respiratory effects of occupational exposure in a general population sample in north Italy. Am Rev Respir Dis 1991; 143: 510–515
Werner B, Nowak D. Berufsbedingte Bronchitis. Atemw-Lungenkrkh 2008; 34: 73–79
Worth G, Brille D, Dijkstra C. The aetiology and pathogensis of bronchitis. Discussion by invitation. In: Orie NGM, Sluiter HJ (Hrsg) Bronchitis. Assen/NL: Royal Vangorcum, 1961b; 61–79
Worth H, Breuer HWM. Deutsche Gesellschaft für Pneumologie: Empfehlungen zur Durchführung und Bewertung von Belastungsuntersuchungen in der Pneumologie. Pneumologie 1998; 52: 225–231
Anhang
Low Dose-Mehrzeilen-Volumen-CT mit HRCT des Thorax (LD HRCT)
(Protokoll 06.2016 Diagnostik und Begutachtung bei berufsbedingten Erkrankungen der Lunge)
Ziel der Protokollempfehlung ist eine möglichst große Vereinheitlichung von CT Untersuchungen, auch bei Anwendung unterschiedlichster Scanner.
Die Endpunkte sind:
lückenlose Abdeckung der Lunge und Pleura
isotrope Voxel zur Rekonstruktion in allen Raumebenen
gute Bildqualität
eff. Dosis
Definition Low-Dose-CT
Die eff. Dosis der CT-Untersuchung liegt bei einem BMI von 24 deutlich unter 1 mSv (s. ICRP 89: Definition Normpatient: männlich 176 cm/73 kg; weiblich 160 cm/60 kg – BMI 24)
Durchführung der Untersuchung/Dokumentation/Beurteilung
Vorbemerkung: Bei jeder Anwendung ionisierender Strahlung sind die Vorgaben der Röntgenverordnung zu berücksichtigen. Die „Rechtfertigende Indikation“ muss deshalb durch den durchführenden Arzt geprüft werden (§ 23 RöV).
Indikationen zum Einsatz dieses Untersuchungsprotokolls:
gesicherte berufliche Exposition und Thoraxübersichtsaufnahme mit Anzeigekriterien einer berufsbedingten Lungenerkrankung
erweiterte Vorsorge bei ehemals hoch asbestexponierten Versicherten mit einem fortgesetzten oder längstens 15 Jahre zurückliegenden Nikotinabusus von mindestens 30 py
Dieses Protokoll wird nicht bei primärem Verdacht auf einen Tumor der Lunge und nicht zum Nachweis oder Ausschluss einer Berufskrankheit bei schon bekanntem Lungentumor eingesetzt. In einem solchen Fall wird das Protokoll: „Mehrzeilen-Volumen-HRCT des Thorax mit i.v. KM-Gabe im Rahmen der Diagnostik und Begutachtung von berufsbedingten Tumorerkrankungen der Lunge“ angewendet!
Gerätevoraussetzung: Mehrzeilen-CT-Gerät (MSCT) mit mindestens 16 Zeilen
Hinweis: Das Untersuchungsprotokoll muss geeignet sein, die Voraussetzung der Definition des LD CT zu erfüllen.
Die Parameter der Untersuchungsprotokolle können geräteabhängig variieren. Unabhängig von dem eingesetzten CT Gerät müssen aber mindestens die in Tabelle 14 angegebenen Parameter erfüllt sein.
Anmerkung 1: Anpassung der Dosiseinstellungen nach BMI:
Anmerkung 2: Um zu annähernd ähnlichen Ergebnissen hinsichtlich räumlicher Auflösung und Bildrauschen zu gelangen, empfiehlt sich je nach Gerätehersteller die Verwendung folgender Faltungskerne:
Anmerkung 3: Bei GE-Geräten Verwendung der nominellen Schichtdicke 1,25 mm nur bei Rekonstruktion im „Full“-Modus (effektive Schichtdicke: 1,14 mm); alternativ: nominelle Schichtdicke 0,625 mm mit Rekonstruktion im „Plus“-Modus (effektive Schichtdicke: 0,93 mm)
Ergänzung: Bei V. a. Hypostasephänomen ergänzend Bauchlage:
exemplarische Schichten nur in den Unterfeldern
Dokumentation nur im Lungenfenster
Dokumentation: gesamte Untersuchung obligatorisch auf CD-ROM im DICOM Standard.
Befundauswertung:
Schriftlicher Befund mit differenzierter Beurteilung aller Veränderungen
Obligatorisch ist zusätzlich die Dokumentation der Veränderungen des Parenchyms und der Pleura nach ICOERD (internationaler Klassifikationsbogen)
(AG „ Arbeits- und umweltbedingte Erkrankungen“ der DRG/04-2002; Modifikation 06.2016)
Beurteilung Bildqualität – HRCT Klassifikation nach ICOERD
Die Bildqualität wird in 4 Stufen eingeteilt, sie ist auf die Beurteilung der arbeitsbedingten pulmonalen Erkrankungen und die qualifizierte Kodierung nach ICOERD fokussiert.
Ein gewichtsadaptiertes Low-Dose-Protokoll (s. Untersuchungsprotokoll) wird vorausgesetzt. Die Dokumentation des Patientenprotokolls ist obligatorisch (Definition HRCT: Schichtdicke 1 mm bis maximal 1,5 mm s. Webb-Müller-Naidich 4th Edition).
1 = keine Einschränkung bei Beurteilung und Kodierung:
Definition:
Rekonstruktion im Lungen- und Mediastinalfenster
jeweils korrekte Wahl des Kernels
axial kontinuierliche Rekonstruktion 1–1,5 mm Lunge
Mediastinum 3 mm, axial und koronal
Datensatz insgesamt so dokumentiert, dass koronale, sagittale und MIP-Rekonstruktionen im Lungenfenster ggf. nachträglich angefertigt werden können
2 = Beurteilung und Kodierung eingeschränkt möglich:
Definition:
Rekonstruktion im Lungen- und Mediastinalfenster
jeweils korrekte Wahl des Kernels
aber
axial kontinuierliche Rekonstruktion > 2 bis 4 mm;
Kombination von Spirale mit maximal 4 mm rekonstruiert u. sequentielles HRCT;
ergänzendes sequentielles HRCT überschreitet nicht einen Schichtabstand von 10 mm
Mediastinum >3 bis
Artefakte, die eine Beurteilung in diagnoserelevanten Arealen einschränken
3 = Beurteilung und Kodierung erheblich eingeschränkt:
Definition:
Rekonstruktion im Lungen- und Mediastinalfenster
jeweils korrekte Wahl des Kernels
aber
Kombination von Spirale mit 5 mm rekonstruiert u. sequentielles HRCT;
das ergänzende sequentielle HRCT überschreitet einen Schichtabstand von 10 mm, bzw. nur exemplarische Schichten wurden aufgenommen oder selektiv dokumentiert
nur sequentielles CT oder ausschließlich sequentielle Aufnahmen in Bauchlage
Mediastinum 6 mm, keine axiale Rekonstruktion
Dokumentation nur im Weichteil-/oder im Lungenfenster
Kernel nicht an die dokumentierten Fenster angepasst (z.B. Rekonstruktion der Lunge mit glättendem Kernel)
anhand des vorliegenden Datensatzes keine sekundären, diagnostisch verwertbaren Rekonstruktionen (z.B. koronale, sagittale und MIP-Rekonstruktion) möglich
Artefakte, die eine Beurteilung in diagnoserelevanten Arealen von Lunge oder Pleura stark einschränken
4 = Bildmaterial für Beurteilung und Kodierung unbrauchbar:
Definition:
für Kodierung nicht zu verwenden, wenn in diagnostisch relevanten Arealen Lunge und Pleura nicht zu beurteilen sind
ggf. ergänzender Kommentar
Arbeitsmed Sozialmed Umweltmed 2016; 51: 868–897
Fußnoten
1 Campus Benjamin Franklin, Charité – Universitätsmedizin Berlin
2 Landesamt für Umwelt- und Arbeitsschutz, Saarbrücken
3 Institut für Pathologie (Direktor: Prof. Dr. med. Rainer M. Bohle), Universitätsklinikum des Saarlandes, Homburg (Saar)
4 Klinikum Westfalen, Knappschaftskrankenhaus, Dortmund
5 BDT – Institut für bildgebende Diagnostik und Therapie, MVZ, Erlangen
6 Institut und Poliklinik für Arbeits-, Sozial- und Umweltmedizin (Direktor: Prof. Dr. med. Dennis Nowak), Klinikum der Universität München, Mitglied, Comprehensive Pneumology Center Munich, German Centre for Lung Research (DZL, Deutsches Zentrum für Lungenforschung)
7 Institut für Pathologie (Direktorin: Prof. Dr. med. Andrea Tannapfel), Ruhr-Universität Bochum
8 Abteilung Pneumologie – Universitätsklinik, Ruhrlandklinik, Westdeutsches Lungenzentrum, Universitätsklinikum Essen
9 Klinik für Pneumologie, Allergologie, Klinische Immunologie, Zentrum für Schlaf- und Beatmungsmedizin, Lungenzentrum (DKG), Moers
10 Institut für Arbeitsmedizin und Sozialmedizin (Direktor: Prof. Dr. med. Thomas Kraus), Uniklinikum der RWTH Aachen
11 Deutsche Gesetzliche Unfallversicherung, Referat Berufskrankheiten, Berlin
12 Patientenvertreter, Berlin
1 Anlage 1 zur Berufskrankheitenverordnung (BKV [1]), zuletzt geändert am 22.12.2014

![<p>
<span class="GVSpitzmarke"> Tabelle 1: </span>
Umwandlung der in den Studien der Tabellen 2–9 verwendeten ILO-Klassifikationen 1958, 1968, 1971 in die aktuelle ILO-Klassifikation 2000 [2] (in Analogie zu [31]). Die ILO 1980 und die ILO 2000 [2] entsprechen sich hinsichtlich der kleineren Schatten, hinsichtlich der großen Schatten weist letztere lediglich eine Änderung der Zeichnung auf [10]
</p>
Tabelle 1:
Umwandlung der in den Studien der Tabellen 2–9 verwendeten ILO-Klassifikationen 1958, 1968, 1971 in die aktuelle ILO-Klassifikation 2000 [2] (in Analogie zu [31]). Die ILO 1980 und die ILO 2000 [2] entsprechen sich hinsichtlich der kleineren Schatten, hinsichtlich der großen Schatten weist letztere lediglich eine Änderung der Zeichnung auf [10]](/sites/default/files/styles/teaser_image_full__s/public/ulmer/de-asu/image/binarydata_original_741444.jpg?itok=zRu-YHld)

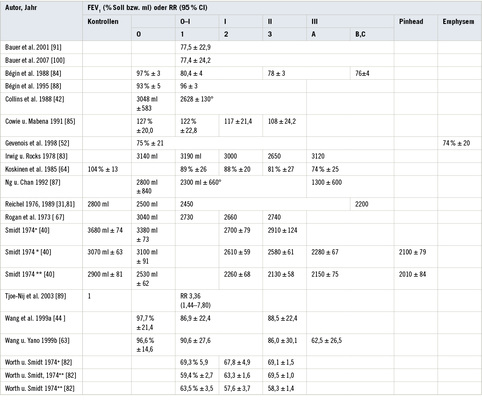

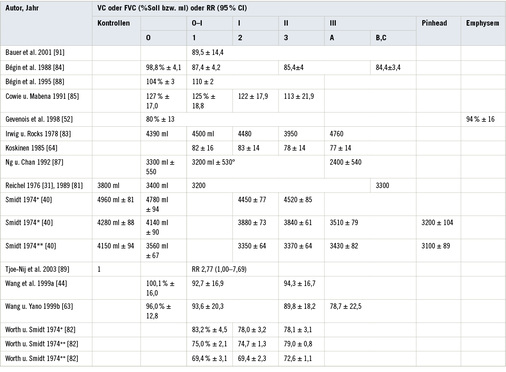
![<p>
<span class="GVSpitzmarke"> Tabelle 6: </span>
Atemwegswiderstand R
<sub>t</sub>
[Auswertung n. Ulmer] bei Quarzstaub- und Kohlengrubenmischstaub-Exponierten. Anmerkungen:
<sup>+</sup>
Altersgruppe 20–39 J., *Altersgruppen 40–49 J., **Altersgruppe 50–60 J.,
<sup>++</sup>
Altersgruppe 40–59 J.,
<sup>+++</sup>
Altersgruppe 60–79 J., Altersgruppen a) 20–35 J., b) 30–50 J., c) 50–60 J., d) > 70 J.; I Mittleres Alter 27,5 J., II Mittleres Alter 45,6 J.; & z. T. Doppelpublikation.
</p>
Tabelle 6:
Atemwegswiderstand R
t
[Auswertung n. Ulmer] bei Quarzstaub- und Kohlengrubenmischstaub-Exponierten. Anmerkungen:
+
Altersgruppe 20–39 J., *Altersgruppen 40–49 J., **Altersgruppe 50–60 J.,
++
Altersgruppe 40–59 J.,
+++
Altersgruppe 60–79 J., Altersgruppen a) 20–35 J., b) 30–50 J., c) 50–60 J., d) > 70 J.; I Mittleres Alter 27,5 J., II Mittleres Alter 45,6 J.; & z. T. Doppelpublikation.](/sites/default/files/styles/image_gallery__s/public/ulmer/de-asu/image/binarydata_original_741449.jpg?itok=IPoTfhxh)
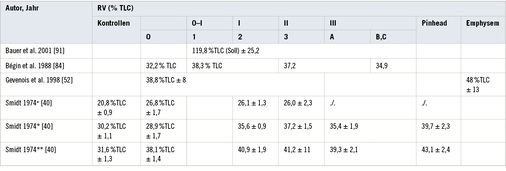


![<p>
<span class="GVSpitzmarke"> Tabelle 10: </span>
Distribution of radiological readings of reader 2, by autopsy grade of silicosis, and the SE and SP values [13]
</p>
Tabelle 10:
Distribution of radiological readings of reader 2, by autopsy grade of silicosis, and the SE and SP values [13]](/sites/default/files/styles/image_gallery__s/public/ulmer/de-asu/image/binarydata_original_741453.jpg?itok=B9gOeCrA)