Radiologie der Gonarthrose – konventionelle Röntgendiagnostik und Schnittbildgebung
Die Gonarthrose ist eine komplexe Gelenkerkrankung mit typischen radiologischen Veränderungen, die sich in der konventionellen Bildgebung sehr gut darstellen lassen (Gelenkspaltverschmälerungen, Osteophyten, subchondrale Sklerose, Geröllzysten). Initiale degenerativ bedingte Kniebinnen-veränderungen von Knorpel, Meniski und Bändern, aber auch Knochenmark-läsionen lassen sich mit der Magnetresonanztomographie darstellen, so dass der Betrachter ein Bild über das Gesamtausmaß der Degeneration erhält und die Behandlung entsprechend adaptiert werden kann. Die Kenntnis über das Vorliegen solcher Läsionen kann helfen, den potenziellen Krankheits-verlauf abzuschätzen.
Schlüsselwörter: Kniegelenk – Gonarthrose – Gelenkdegeneration – Bildgebung
Gonarthrosis radiology: cross-sectional imaging in conventional diagnostic radiography
Gonarthrosis is a complex joint disease with typical radiological changes, which can be readily depicted by conventional radiography (joint space narrowing, osteophytes, subchondral sclerosis, subchondral cysts). Initial degenerative internal derangements of the knee joint can comprise cartilage, meniscal, ligamentous and bone marrow lesions, which can be visualized by magnetic resonance tomography. This technique provides an insight into the full extent of the joint disease and enables treatment to be suitably adapted, since knowledge of such lesions may help in estimating the progression of the disease.
Keywords: knee joint – gonarthrosis – joint degeneration – imaging
ASU Arbeitsmed Sozialmed Umweltmed 2015; 50: 130–137
Gonarthrose
Die Arthrose ist ein multifaktorieller komplexer Krankheitsprozess, der charakteristische pathologische und radiologische Veränderungen ausbildet. Diese Veränderungen können, müssen aber nicht klinisch symptomatisch sein (Arden 2006). Die Diagnose kann demzufolge sowohl gestellt werden, wenn das passende klinische Beschwerde-bild (Gelenkschmerz und Gelenksteifigkeit) oder strukturelle Gelenk-veränderungen vorliegen oder bei einer Kombination beider Komponenten. Für den Beweis struktureller Veränderungen ist eine Bild-gebung notwendig (Arden et al. 2006). Diese hat die Aufgabe, die degenerativen Veränderungen entsprechend ihrer Ausprägung einzustufen und ggf. Hinweise auf die Ursache zu bieten, die für die nachfolgende Therapie eine Rolle spielen könnte.
Röntgendiagnostik, Einstellungen, Methodik, Art und Ort der Veränderungen
Die Methode der Wahl zur Begutachtung, ob eine Arthrose vorliegt, ist die Projektionsradiographie in mindestens 2 Ebenen. Diese ist ubiquitär verfügbar und kostengünstig.
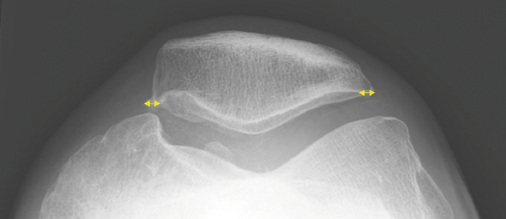
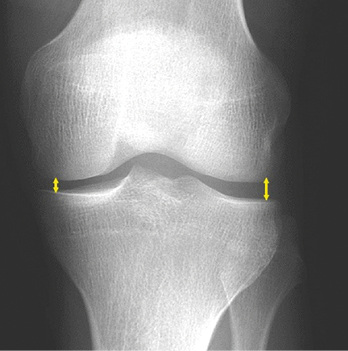
Die Basisaufnahmen bestehen aus einer anterior-posterioren (a.p., gestrecktes Bein, Zentrierung auf die Patella) und einer latera-len (streng seitlichen) Aufnahme im Stehen. Diese zwei Aufnahmen bieten eine Ansicht des medialen und lateralen Femorotibialgelenks, die seitliche zusätzlich eine Einsicht in das Patellofemoralgelenk. Die Aufnahme unter Belastung im Stehen ist zur Beurteilung einer Arthrose essenziell, da nur so, eine tatsächliche Gelenkspaltverschmälerung herausgearbeitet werden kann. Würde man die Aufnahme im Liegen durchführen, würde sich das Gelenk entspannen, der Gelenkspalt weiten und die reelle Beurteilung einer potenziellen Reduktion des Gelenkspalts maskiert werden. Für eine dedizierte Darstellung des Patellofemoralgelenks kann eine zusätzliche axiale Aufnahme (in 60° Flexion) angefertigt werden.
Eine systematische Beurteilung umfasst die Bildanalyse unterschiedlicher Komponenten:
- Achsenstellung des Gelenks, Abweichungsrichtung, Torquierung;
- Knochenstruktur bzgl. ihrer Dichte, Vorliegen von Sklerosen, osteophytären Anbauten, Geröllzysten;
- Gelenkspalt bzgl. Höhenminderung und Lokalisation der Höhen-minderung (symmetrisch vs. asymmetrisch), Knorpel-/Meniskus-verkalkungen;
- Weichteilveränderungen, Gelenkerguss, Verkalkungen.
Röntgenologische Bildbefunde
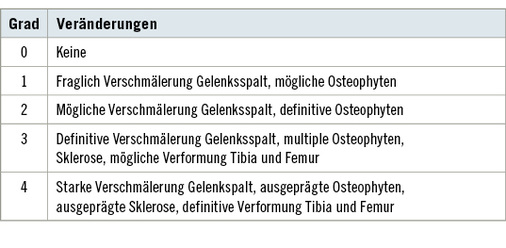
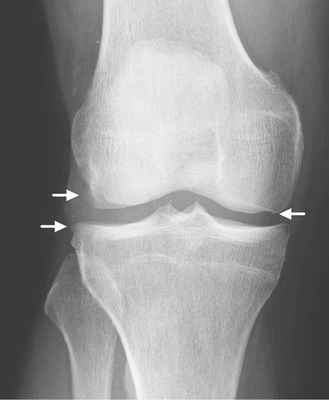
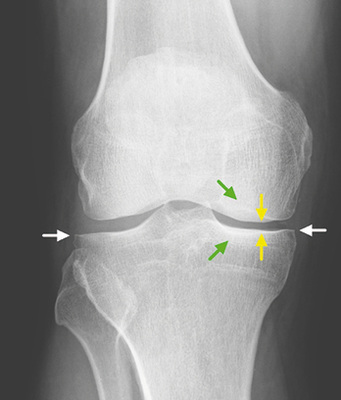
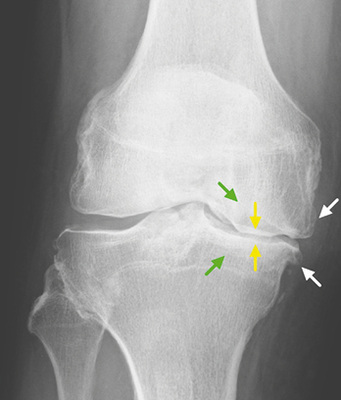
Liegt eine Arthrose vor, lassen sich 4 typische Befunde in unterschiedlicher Ausprägung je nach Stadium abgrenzen:
- Gelenkspaltverschmälerung, meist asymmetrisch, betont im last-tragenden Bereich. Diese entspricht der indirekten Beurteilung der noch erhaltenen Knorpeldicke. Es muss berücksichtigt werden, dass auch eine Höhenminderung der Menisci zu einer Reduktion des Gelenkspalts führen kann;
- subchondrale Sklerosierung, betont im lasttragenden Bereich;
- osteophytäre Anbauten;
- Geröllzysten.
Je nach Aktivitätsgrad können ein Gelenkerguss, aber auch Gelenkdestruktionen vorliegen.
Röntgenologische Graduierung der Gonarthrose
Der Arthrosegrad wird klassischerweise nach Kellgren und Lawrence eingestuft ( Tabelle 1 , Beispiele Abb. 1–4 ) (Kellgren u. Lawrence 1957). Dieser basiert auf den oben beschriebenen radiologischen Arthrosezeichen, wurde 1957 erstmals publiziert und 1963 als Bildatlas für alle Gelenke herausgegeben, um die Graduierung zu erleichtern.
Die Kellgren-Lawrence-Skala wird bis heute in epidemiologischen und klinischen Studien zur Patientenselektion und Stratifizierung in Gruppen eingesetzt. Sie besitzt allerdings Limitationen, die man sowohl als Anwender als auch als Leser von Studien, die die Skala benutzen, kennen sollte, um die erhobenen Daten einschätzen zu können.
Definition der arthrotischen Veränderungen
Die ursprünglichen Publikation der Kellgren-Lawrence-Skala bietet keine genaue Definition, wann eine Gelenkspaltverschmälerung oder ein Osteophyt als solche charakterisiert wird. Daher ist die Einstufung der anatomischen Veränderungen subjektiv breit inter-pretierbar, wodurch die Skala unter einer durchaus relevanten Interreader-Variabilität leidet. Diese lässt sich nicht vollständig vermeiden, aber reduzieren, indem derselbe Befunder oder zwei Befunder in Konsensus die Einteilung vornehmen. Man muss daher beachten, dass die Nutzung dieser Skala zwar nicht das Ergebnis von Vergleichen zwischen Untersuchungsgruppen stört, aber die primäre Einteilung der Patienten und somit die Prävalenz der einzelnen Arthrosegruppen in Studien verfälscht sein kann (Kellgren u. Lawrence 1957).
Neben der fehlenden genauen Definition der anatomischen Veränderungen (Kellgren u. Lawrence 1957), existieren zudem in der Literatur unterschiedliche Variationen der ursprünglichen Beschreibung der Kellgren-Lawrence-Grade (Schiphof et al. 2008), die ebenfalls zu unterschiedlicher Gradeinstufung von degenerativen Veränderungen führen können (Schiphof et al. 2011).
Übertragen auf den Kontext der Begutachtung, ob eine berufsbedingte Gonarthrose vorliegt, bedeutet dies, dass der beurteilte Schädigungsgrad durch unterschiedliche Begutachter ebenfalls variieren kann. Es ist daher vonnöten sich auf eine Definition der Veränderungen sowie der Einteilung zu einigen, um eine systematische Begutachtung der radiologischen Veränderungen zu gewährleisten.
Eine interdisziplinäre Konsensusarbeitsgruppe, die auf Einla-dung der Deutschen Gesetzlichen Unfallversicherung (DGUV) in den letzten Jahren an einer Begutachtungsempfehlung für die Berufserkrankung Gonarthrose (BK 2112) gearbeitet hat, hat sich mit diesen Fragen beschäftigt und 2014 eine Empfehlung für die Merkmale Osteo-phyt und Gelenkspaltverschmälerung herausgegeben (Interdisziplinäre Arbeitsgruppe zur Begutachtung der BK 2112; 2014), um eine einheitlichere und objektivere Graduierung zu ermöglichen.
Konsensusempfehlung BK 2112 Merkmal „definiter“ Osteophyt
Ein definiter Osteophyt ist eine knöcherne Ausziehung einer Größe 2 mm ab antizipierter Knochenform des Gelenkrands ( Abb. 5 , Beispiele auch Nagaosa et al. 2000; Altman u. Gold 2007). Patellär sind nur die seitlichen Anbauten als relevant zu werten. Hier ist darauf zu achten, diese nicht mit Sehnenansatzverkalkungen oder Fibroostosen zu verwechseln (Freyschmidt et al. 1978).
Konsensusempfehlung BK 2112 Gelenkspalt-verschmälerung
Basierend auf Normwerte nach Lanyon (1998), der Gelenkspaltmessungen an 86 Frauen und 39 Männern ohne Kniebeschwerden und ohne Osteophyten durchgeführt hatte (Altersverteilung 40–75 Jahre, Durchschnittsalter 58 Jahre), einigte sich die Konsensusgruppe auf folgende Werte für eine vorliegende Gelenkspaltverschmälerung: siehe Tabelle 2 für das Femorotibialgelenk und Tabelle 3 für das Patellofemoralgelenk.
Falls eine grenzwertige Gelenkspaltverschmälerung vorliegen sollte, wird empfohlen, bereits vorhandene Magnetresonanztomographie- (MRT-) und/oder Arthroskopiebefunde als aussagekräftigere Methoden im Vergleich zu der Projektionsradiographie zu werten und in die Entscheidung bezüglich des Vorliegens einer Arthrose einzubinden. Sollte eine Klärung durch bereits vorhandene Unter-suchungen nicht möglich sein, sollte ggf. zur Verifizierung eines mög-lichen Knorpelschadens ein ergänzendes MRT angefertigt werden.
Sonderfall „definitive“ Gelenkspaltverschmälerung ohne Osteophyten
Die Kellgren-Lawrence-Skala wird seit jeher kontrovers diskutiert, da sie einen starken Fokus auf osteophytäre Anbauten legt. Dadurch wird die atrophe Form der Arthrose ( Abb. 6 ), bei der es zur Gelenkspaltverschmälerung ohne wesentliche Osteophyten kommt, vernachlässig und kann nicht klar eingestuft werden. Hierfür schlägt die Konsensusarbeitsgruppe BK 2112 (2014) vor, dass diese analog zu Kellgren-Lawrence-Grad 3 oder 4, Letztere wenn eine starke Verschmälerung und definitive Verformungen des Femurs und der Tibia vorliegen, einzustufen.
Konventionelle Röntgenaufnahme als Verlaufskontrolle einer Arthrose
Die konventionelle Röntgenuntersuchung ist als Werkzeug für eine Verlaufsbeurteilung nicht geeignet, da sie strukturelle Veränderungen über die Zeit nicht ausreichend erfasst und die strukturellen Veränderungen nur moderat mit einer klinischen Arthrose korrelieren (Felson et al. 1997; Salaffi et al. 2003).
Initiale kartilaginäre Veränderungen sind nur indirekt über die Gelenkspaltverschmä-lerung abschätzbar. Sie werden in der Literatur quantitative als Gelenkspaltweite (Joint Space Width, JSW) gemessen und ihre Veränderung im Verlauf als Gelenkspalt-verschmälerung (Joint Space Narrowing, JSN). Die natürliche jährliche Gelenkspaltverschmälerung ist mit 0,1–0,15 mm (Standardabweichung 0,1 mm) allerdings sehr gering (Guermazi et al. 2008) und wird zudem auch durch Höhenänderungen der Menisci (Meniskusläsionen, Meniskus-extrusionen) beeinflusst, so dass eine genaue Dickenabschätzung der erhaltenen Knorpelschicht im Kniegelenk mit dem Röntgenbild im Prinzip nicht möglich ist (Crema et al. 2014). Bei dedizierten Frage-stellungen bezüglich des Knorpels sollte daher auf eine direkte Darstellung, z. B. mit Hilfe der Magnetresonanztomographie zurückgegriffen werden.
Knöcherne Veränderungen stellen bereits fortgeschrittene Veränderungen dar, die ebenfalls nur langsam entstehen. Problematisch für eine Verlaufsbeurteilung in Bezug auf eine klinische manifeste Arthrose ist hierbei, dass das Vorliegen von Osteophyten nicht notgedrungen mit einer entsprechenden Klinik einhergehen muss. Unterschiedliche Studien zeigten in ihrer jeweils untersuchten Population, dass 50–75 % der Menschen über 65 Jahren radiologische Zeichen einer Gonarthrose im Röntgenbild zeigen (McAlindon et al. 1992; Tennant et al. 1995; Oliveria et al. 1995), die fast 100 % in einer Population über 75 Jahren erreicht (Altman et al. 1986). Von diesen zeigten jedoch nur 40–60 % klinische Symptome einer Arthrose (McAlindon et al. 1992; Anderson u. Felson 1998; Zhang et al. 1995; Lethbridge-Cejku et al. 1995). Knieschmerz ist also kein sehr guter Prädiktor für eine radiologische Erkrankung. Weitere Studien zeigten zudem, dass es an einer engen Korrelation zwischen dem radiologischen Verlauf und dem klinischem Outcome einer Gonarthrose mangelt (Claessens et al. 1990; Salaffi et al. 1991, 2000; Odding et al. 1996; Hannan et al. 2000).
Magnetresonanztomographie, Einstellungen, Methodik, Art und Ort der Veränderungen
Die Magnetresonanztomographie (MRT) ist aktuell die einzige Technik, die es ermöglicht den Knorpel und Knorpelmatrixverän-derungen direkt und nichtinvasiv darzustellen. Ihr Vorteil ist, dass sie daneben aber auch begleitende weitere Kniebinnenschäden erfasst, die im Rahmen degenerativer Geschehnisse auftreten können, wie meniskeale, ligamentäre und auch ossäre Veränderungen (Resnick et al. 2006).
Im Kontext der Diagnose einer Gonarthrose ist die MRT vor allem von Interesse für eine frühe und detailliertere Darstellung von Knorpelläsionen. Die Sensitivität für die Detektion von Knorpel-läsionen ist dabei abhängig von der Sequenzwahl.
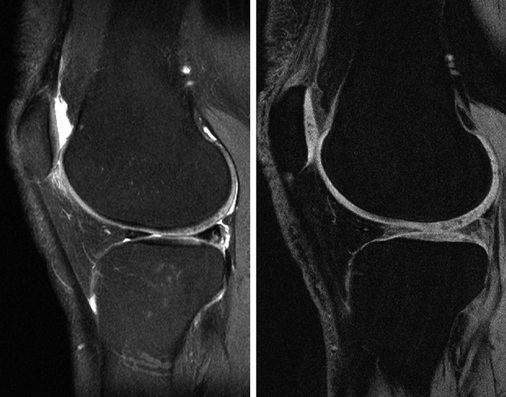
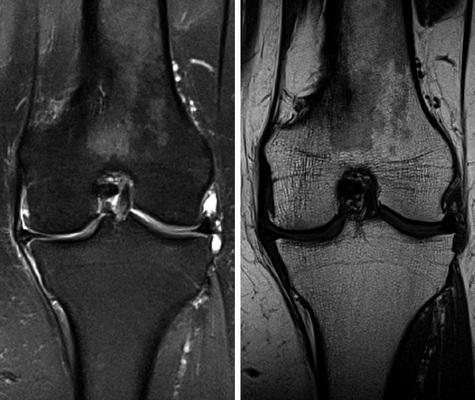
Hierfür sind insbesondere 2 Sequenztypen geeignet. Die erste ist die moderat T2-gewichtete Turbo-Spin-Echo Sequenz, in der der Knorpel ein intermediäres Signal im Vergleich zur Gelenkflüssig-keit zeigt ( Abb. 7 , links). Ihre Sensitivität zur Detektion von Knorpelbinnenläsionen beträgt 94 % (Resnick et al. 2006). Sie wird typischerweise zweidimensional in unterschiedlichen Ebenen akquiriert, in Abhängigkeit davon, welches Gelenk betrachtet werden soll.
Neue technische Entwicklungen erlauben inzwischen auch eine dreidimensionale Akquisition dieser Sequenztechnik, die eine nachträgliche freie Reformation der Bilddaten in allen Raumrichtungen ermöglicht (Notohamiprodjo et al. 2009, 2012).
Eine komplementäre Sequenz, die eine sehr gute Darstellung der Knorpeldicke und des Knorpelvolumens darstellt, ist die T1-gewichtete fettunterdrückte oder wasserangeregte 3D-Gradientenechosequenz (s. Abb. 7, rechts). Auch diese lässt sich in den unterschiedlichen Raumebenen nachträglich reformatieren. Der Knorpel bietet in dieser Technik eine sehr hohe Signalintensität und lässt sich daher sehr gut von dem umgebenen Strukturen, insbesondere vom subchondralen Knochen abgrenzen (Graichen et al. 2000; Glaser et al 2001). Die Sensitivität dieser Sequenz für Knorpelläsionen beträgt ca. 93 %, wobei sie eher geeignet ist Dickenveränderungen darzustellen und nur eingeschränkte Beurteilbarkeit der Matrix selbst bietet, für die eher eine moderat T2-gewichtete Sequenz genutzt werden sollte (Resnick et al. 2006).
Grading der Knorpelveränderungen im MRT
Für die Graduierung der Ausprägung von Knorpelläsionen existieren unterschiedliche Klassifikationen, die sich meist nur in Details unterscheiden und sich an der arthroskopischen Outerbridge-Klassifikation (1961) orientieren.
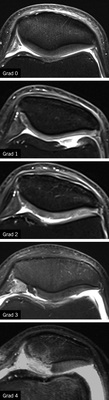
Für die Begutachtung der Knorpelläsionen im Rahmen der BK 2112 wird von der Konsensusarbeitsgruppe der DGUV (2014) empfohlen, die Einteilung nach Vallotton et al. (1995) zu nutzen ( Tabelle 4 , Abb. 8 ).
Diese ist in diesem Szenario vor dem Hintergrund von Bedeu-tung, wenn eine atrophe Form der Arthrose vorliegt, die keine oder nur geringe osteophytäre Anbauten zeigt, aber eine relevante Gelenkspaltverschmälerung vorliegt oder es um Fälle geht, die rein konventionell röntgenologisch nicht sicher einzustufen sind. Die Konsensusarbeitsgruppe zur BK 2112 fordert hier zur Anerkennung einer Gonarthrose Knorpelschäden, die mindestens einen Grad 3 oder 4 nach Vallotton erreichen sowie eine großflächige Ausdehnung innerhalb der betroffenen gegenüber artikulierenden Gelenkflächen des betroffenen Kompartimentes (2014).
Vorteile der MRT gegenüber konventioneller Röntgen-diagnostik
Die MRT erfasst im Gegensatz zu der Röntgendiagnostik begleitende Kniebinnenveränderungen der Menisken, Bänder und des Knochen-marks und bietet dem Betrachter ein umfassendes Bild über das gesamte Ausmaß der Degeneration ( Abb. 9 ).
Zudem ermöglicht es die Darstellung von Knochenmarködem, das in keiner anderen bildgebenden Technik dargestellt werden kann.
Bedeutung des chronischen Knochenmarksödems
Das Knochenmarködem ist eine Entität, die keine eigene Erkran-kung darstellt, sondern als eine Folgeerscheinung verstanden wer-den muss, die sehr unterschiedliche Ursachen haben kann. Sie wurde initial von Wilson (1988) beschrieben. Pathologische Untersuchungen haben seitdem allerdings gezeigt, dass das Knochenmarködem, dass in der MRT sichtbar ist, nicht nur aus Ödem sondern, auch andere pathologischen Entitäten bestehen kann, so dass es in der Literatur inzwischen teilweise auch als Knochenmarkläsionen (englisch „bone marrow lesion“ (BML)) bezeichnet wird (Hunter et al. 2006, 2008; d’Anjou et al. 2008; Manara u. Varenna 2014).
Das Knochenmarködem im Rahmen einer Arthrose entspricht einer Kombination aus Veränderungen, die Fibrosierungen, Nekrosen, Ödem und Einblutungen sowie abnormen Trabekeln beinhalten (Zanetti et al. 2000). Die Knochenmarksödemzonen können innerhalb kurzer Zeit ihre Größe ändern und sind assoziiert mit progredientem Knorpelverlust und fluktuierenden Gelenkschmerzen (Xu et al. 2012). Hierbei sind sowohl das Vorhandensein in der Baseline-Untersuchung, eine Größenzunahme als auch ein Neu-auftreten eines Knochenmarködems unabhängig mit einem höheren Risiko eines Knorpelverlusts in der entsprechenden Region assoziiert (Hunter et al. 2006; Roemer et al. 2009; Kubota et al. 2010; Xu et al. 2012). Weiterhin ist das Knochenmarködem mit der Entstehung subchondraler Zysten assoziiert. Sie ist also als eine präzystische Läsion zu betrachten, kann ihre Größe auch ändern, wenn innerhalb ihrer Zone eine Zyste entsteht; muss sich allerdings nicht zystisch transformieren (Carrino et al. 2006; Crema et al. 2010). Große Ödemzonen in der Baseline-Untersuchung sind zudem mit stärkeren Schmerzen, dem Vorhandensein von Gelenkspalt-verschmälerungen und dem Fortschreiten der Arthrose assoziiert (Driban et al. 2013). Die Regredienz eines Knochenmarködems ist dagegen assoziiert mit einer Schmerzreduktion, allerdings nicht mit einem Risikorückgang für eine gleichzeitig zunehmende Gelenkspaltverschmälerung, also dem Fortschreiten der Erkrankung (Driban et al. 2013).
Knochenmarködeme sollten in flüssigkeitssensitiven Sequenzen, in mehreren Ebenen beurteilt werden, um eine Missinterpretation von Partialvolumeneffekten oder artefaktbedingter ungenügender Fettsättigung zu vermeiden (Xu et al. 2012).
Bedeutung von Vorschäden der Bänder und Menisken
Meniskusveränderungen können zu einer Alteration der Biomechanik und konsekutiven Mehrbelastung des betroffenen Kompartiments führen (Englund et al. 2010). Hierdurch kann der subchondrale Knochen und Knorpel vermehrt beansprucht werden, so dass es plausibel ist, dass Meniskusschäden ein Risikofaktor darstellen kann für Knochenmarkläsionen (Lim et al. 2013) und konsekutiv auch Knorpelläsionen (siehe Absatz hierüber).
Die Bedeutung von Bandverletzungen für die Entstehung einer Arthrose ist für das vordere Kreuzband gut untersucht (Ajuied et al. 2014). Eine Studie zeigte in ihrem Kollektiv, dass Patienten mit vorderen Kreuzbandrissen eine höhere Prävalenz für höhergradige Knorpelläsionen, Meniskusläsionen, Veränderungen des medialen Kollateralbandes, Knochenmarksläsionen und subchondrale Zysten besitzen (Hovis et al. 2012; Guermazi et al. 2014). Die Prävalenz für eine Gonarthrose nach isolierter vorderer Kreuzbandruptur beträgt je nach Studie 0–13 %, wenn assoziiert mit Meniskusläsionen steigt sie sogar auf 21–48 % (Øiestad et al. 2009). Daher hat eine Reparatur der Bandverletzung eine relevante Bedeutung für die Reduktion des Risikos einer Gelenkdegeneration (Ajuied et al. 2014).
Literatur
Ajuied A, Wong F, Smith C, Norris M, Earnshaw P, Back D, Davies A: Anterior cruciate ligament injury and radiologic progression of knee osteoarthritis: a systematic review and meta-analysis. Am J Sports Med 2014 42: 2242–2252.
Altman R, Asch E, Bloch D, Bole G, Borenstein D, Brandt K, Christy W, Cooke TD, Greenwald R, Hochberg M et al.: Development of criteria for the classifica-tion and reporting of osteoarthritis. Classification of osteoarthritis of the knee. Diagnostic and Therapeutic Criteria Committee of the American Rheumatism Association. Arthritis Rheum 1986; 29: 1039–1049.
Altman RD, Gold GE: Atlas of individual radiographic features in osteoarthritis, revised. Osteoarthritis Cartilage 2007; 15 Suppl A: A1–56.
Anderson JJ, Felson DT: Factors associated with osteoarthritis of the knee in the first national Health and Nutrition Examination Survey (HANES I). Evidence for an association with overweight, race, and physical demands of work. Am J Epidemiol 1988; 128: 179–189.
Arden N, Nevitt MC: Osteoarthritis: epidemiology. Best Pract Res Clin Rheumatol 2006; 20: 3–25.
Carrino JA, Blum J, Parellada JA, Schweitzer ME, Morrison WB: MRI of bone marrow edema-like signal in the pathogenesis of subchondral cysts. Osteoarthritis Cartilage 2006; 14: 1081–1085.
Claessens AA, Schouten JS, van den Ouweland FA, Valkenburg HA: Do clinical findings associate with radiographic osteoarthritis of the knee? Ann Rheum Dis 1990; 49: 771–774.
Crema MD, Roemer FW, Zhu Y, Marra MD, Niu J, Zhang Y, Lynch JA, Javaid MK, Lewis CE, El-Khoury GY, Felson DT, Guermazi A: Subchondral cystlike lesions develop longitudinally in areas of bone marrow edema-like lesions in patients with or at risk for knee osteoarthritis: detection with MR imaging – the MOST study. Radiology 2010; 256: 855–862.
Crema MD, Nevitt MC, Guermazi A, Felson DT, Wang K, Lynch JA, Marra MD, Torner J, Lewis CE, Roemer FW: Progression of cartilage damage and meniscal pathology over 30 months is associated with an increase in radiographic tibio-femoral joint space narrowing in persons with knee OA – the MOST study. Osteo-arthritis Cartilage 2014; 22: 1743–1747.
d‘Anjou MA, Troncy E, Moreau M, Abram F, Raynauld JP, Martel-Pelletier J, Pelletier JP: Temporal assessment of bone marrow lesions on magnetic resonance imaging in a canine model of knee osteoarthritis: impact of sequence selection. Osteoarthritis Cartilage 2008; 16: 1307–1311.
Driban JB, Price L, Lo GH, Pang J, Hunter DJ, Miller E, Ward RJ, Eaton CB, Lynch JA, McAlindon TE: Evaluation of bone marrow lesion volume as a knee osteoarthritis biomarker--longitudinal relationships with pain and structural changes: data from the Osteoarthritis Initiative. Arthritis Res Ther 2013; 15: R112.
Englund M, Guermazi A, Roemer FW, Yang M, Zhang Y, Nevitt MC, Lynch JA, Lewis CE, Torner J, Felson DT: Meniscal pathology on MRI increases the risk for both incident and enlarging subchondral bone marrow lesions of the knee: the MOST Study. Ann Rheum Dis 2010; 69: 1796–1802.
Felson DT, McAlindon TE, Anderson JJ, Naimark A, Weissman BW, Aliabadi P, Evans S, Levy D, LaValley MP: Defining radiographic osteoarthritis for the whole knee. Osteoarthritis Cartilage 1997; 5: 241–250.
Freyschmidt J, Liebig J, Saure D, Fritsch R: New aspects concerning exposure factors during direct geometrical X-ray magnification (author‘s transl). Rofo 1978; 128: 479–485.
Glaser C, Faber S, Eckstein F, Fischer H, Springer V, Heudorfer L, Stammberger T, Englmeier KH, Reiser M: Optimization and validation of a rapid high-resolution T1-w 3D FLASH water excitation MRI sequence for the quantitative assessment of articular cartilage volume and thickness. Magn Reson Imaging 2001; 19: 177–185.
Graichen H, Springer V, Flaman T, Stammberger T, Glaser C, Englmeier KH, Reiser M, Eckstein F: Validation of high-resolution water-excitation magnetic resonance imaging for quantitative assessment of thin cartilage layers. Osteoarthritis Cartilage 2000; 8: 106–114.
Guermazi A, Burstein D, Conaghan P, Eckstein F, Hellio Le Graverand-Gastineau MP, Keen H, Roemer FW: Imaging in osteoarthritis. Rheum Dis Clin North Am 2008; 34: 645–687.
Guermazi A, Roemer FW, Crema MD, Englund M, Hayashi D: Imaging of non-osteochondral tissues in osteoarthritis. Osteoarthritis Cartilage 2014; 22: 1590–1605.
Hannan MT, Felson DT, Pincus T: Analysis of the discordance between radiographic changes and knee pain in osteoarthritis of the knee. J Rheumatol 2000; 27: 1513–1517.
Hovis KK, Alizai H, Tham SC, Souza RB, Nevitt MC, McCulloch CE, Link TM: Non-traumatic anterior cruciate ligament abnormalities and their relationship to osteoarthritis using morphological grading and cartilage T2 relaxation times: data from the Osteoarthritis Initiative (OAI). Skeletal Radiol 2012; 41: 1435–1443.
Hunter DJ, Zhang Y, Niu J, Goggins J, Amin S, LaValley MP, Guermazi A, Genant H, Gale D, Felson DT: Increase in bone marrow lesions associated with cartilage loss: a longitudinal magnetic resonance imaging study of knee osteo-arthritis. Arthritis Rheum 2006; 54: 1529–1535.
Hunter DJ, Lo GH, Gale D, Grainger AJ, Guermazi A, Conaghan PG: The re-liability of a new scoring system for knee osteoarthritis MRI and the validity of bone marrow lesion assessment: BLOKS (Boston Leeds Osteoarthritis Knee Score). Ann Rheum Dis 2008; 67: 206–211.
Interdisziplinäre Arbeitsgruppe zur Begutachtung der BK-Nr. 2112 (Gonarthrose): Begutachtungsempfehlung für die Berufskrankheit Nummer 2112 (Gonarthrose). St. Augustin: Deutsche Gesetzliche Unfallversicherung (DGUV), 2014.
Kubota M, Ishijima M, Kurosawa H, Liu L, Ikeda H, Osawa A, Takazawa Y, Ka-wasaki T, Saita Y, Kimura Y, Kaneko K: A longitudinal study of the relationship between the status of bone marrow abnormalities and progression of knee osteo-arthritis. J Orthop Sci 2010; 15: 641–646.
Lanyon P, O‘Reilly S, Jones A, Doherty M: Radiographic assessment of sympto-matic knee osteoarthritis in the community: definitions and normal joint space. Ann Rheum Dis 1998; 57: 595–601.
Lethbridge-Cejku M, Scott WW Jr, Reichle R, Ettinger WH, Zonderman A, Costa P, Plato CC, Tobin JD, Hochberg MC: Association of radiographic features of osteo-arthritis of the knee with knee pain: data from the Baltimore Longitudinal Study of Aging. Arthritis Care Res 1995; 8: 182–188.
Lim YZ, Wang Y, Wluka AE, Davies-Tuck ML, Teichtahl A, Urquhart DM, Cicut-tini FM: Are biomechanical factors, meniscal pathology, and physical activity risk factors for bone marrow lesions at the knee? A systematic review. Semin Arthritis Rheum 2013; 43: 187–194.
Manara M, Varenna M: A clinical overview of bone marrow edema. Reumatismo 2014; 66: 184–196.
McAlindon TE, Cooper C, Kirwan JR, Dieppe PA: Knee pain and disability in the community. Br J Rheumatol 1992; 31: 189–192.
Nagaosa Y, Mateus M, Hassan B, Lanyon P, Doherty M: Development of a logic-ally devised line drawing atlas for grading of knee osteoarthritis. Ann Rheum Dis 2000; 59: 587–595.
Notohamiprodjo M, Horng A, Pietschmann MF, Müller PE, Horger W, Park J, Crispin A, del Olmo JR, Weckbach S, Herrmann KA, Reiser MF, Glaser C: MRI of the knee at 3T: first clinical results with an isotropic PDfs-weighted 3D-TSE-sequence. Invest Radiol 2009; 44: 585–597.
Notohamiprodjo M, Horng A, Kuschel B, Paul D, Li G, Raya JG, Reiser MF, Glaser C: 3D-imaging of the knee with an optimized 3D-FSE-sequence and a 15-channel knee-coil. Eur J Radiol 2012; 81: 3441–3449.
Odding E, Valkenburg HA, Algra D, Vandenouweland FA, Grobbee DE, Hof-man A: The association of abnormalities on physical examination of the hip and knee with locomotor disability in the Rotterdam Study. Br J Rheumatol 1996; 35: 884–890.
Øiestad BE, Engebretsen L, Storheim K, Risberg MA: Knee osteoarthritis after anterior cruciate ligament injury: a systematic review. Am J Sports Med 2009; 37: 1434–1443.
Oliveria SA, Felson DT, Reed JI, Cirillo PA, Walker AM: Incidence of sympto-matic hand, hip, and knee osteoarthritis among patients in a health maintenance organization. Arthritis Rheum 1995; 38: 1134–1141.
Outerbridge RE The etiology of chondromalacia patellae. J Bone Joint Surg Br 1961; 43-B: 752–757.
Resnick D, Kang HS, Prettenklieber ML: Internal Derangement of Joints, 2. Aufl. Philadelphia: Saunders, 2006.
Roemer FW, Guermazi A, Javaid MK, Lynch JA, Niu J, Zhang Y, Felson DT, Lewis CE, Torner J, Nevitt MC; MOST Study investigators: Change in MRI-detected subchondral bone marrow lesions is associated with cartilage loss: the MOST Study. A longitudinal multicentre study of knee osteoarthritis. Ann Rheum Dis 2009; 68: 1461–1465.
Salaffi F, Cavalieri F, Nolli M, Ferraccioli G: Analysis of disability in knee osteo-arthritis. Relationship with age and psychological variables but not with radio-graphic score. J Rheumatol 1991; 18: 1581–1586.
Salaffi F, Piva S, Barreca C, Cacace E, Ciancio G, Leardini G, Mannoni A, Minari C, Occhi P, Pianon M, Punzi L, Re KA, Scarpa R, Sulli A, Troise-Rioda W: Valida-tion of an Italian version of the arthritis impact measurement scales 2 (ITALIAN-AIMS2) for patients with osteoarthritis of the knee. Gonarthrosis and Quality of Life Assessment (GOQOLA) Study Group. Rheumatology (Oxford). 2000; 39: 720–727.
Salaffi F, Carotti M, Stancati A, Grassi W: Radiographic assessment of osteo-arthritis: analysis of disease progression. Aging Clin Exp Res 2003; 15: 391–404.
Schiphof D, de Klerk BM, Kerkhof HJ, Hofman A, Koes BW, Boers M, Bierma-Zeinstra SM: Impact of different descriptions of the Kellgren and Lawrence classi-fication criteria on the diagnosis of knee osteoarthritis. Ann Rheum Dis 2011; 70: 1422–1427.
Schiphof D, Boers M, Bierma-Zeinstra SM: Differences in descriptions of Kellgren and Lawrence grades of knee osteoarthritis. Ann Rheum Dis 2008; 67: 1034–1036.
Tennant A, Fear J, Pickering A, Hillman M, Cutts A, Chamberlain MA: Pre-valence of knee problems in the population aged 55 years and over: identifying the need for knee arthroplasty. BMJ 1995; 310: 1291–1293.
Vallotton JA, Meuli RA, Leyvraz PF, Landry M: Comparison between magnetic resonance imaging and arthroscopy in the diagnosis of patellar cartilage lesions: a prospective study. Knee Surg Sports Traumatol Arthrosc 1995; 3: 157–162.
Wilson AJ, Murphy WA, Hardy DC, Totty WG: Transient osteoporosis: transient bone marrow edema? Radiology 1988; 167: 757–760.
Xu L, Hayashi D, Roemer FW, Felson DT, Guermazi A: Magnetic resonance imag-ing of subchondral bone marrow lesions in association with osteoarthritis. Semin Arthritis Rheum 2012; 42: 105–118.
Zanetti M, Bruder E, Romero J, Hodler J: Bone marrow edema pattern in osteo-arthritic knees: correlation between MR imaging and histologic findings. Radiology 2000; 215: 835–840.
Zhang N, Shi Q, Zhang X: An epidemiological study of knee osteoarthritis. Zhonghua Nei Ke Za Zhi 1995; 34: 84–87.
Verfasserin
Dr. med. Annie Horng
Institut für Klinische Radiologie
Universitätsklinikum LMU München – Campus Großhadern
Marchioninistraße 15 – 81377 München
Fußnoten
Institut für Klinische Radiologie (Leiter: Prof. Dr. med. Dr. h.c. Maximilian Reiser, FACR, FRCR), Universitätsklinikum der Ludwig-Maximilians-Universität München