D. Bury
H.M. Koch
T. Weiß
T. Brüning
(eingegangen am 18.06.2019, angenommen am 19.08.2019)
ASU Arbeitsmed Sozialmed Umweltmed 2019; 54: 662–665
Exposure biomarkers for the UV filters octocrylene and 2-ethylhexyl salicylate
Objectives: The studies presented describe biomarkers for measuring exposure to the widespread organic UV filters octocrylene (OC) and 2-ethylhexyl salicylate (EHS), as well as a sensitive analytical method for their determination in urine.
Methods: The formation and excretion of each of three specific octocrylene and 2-ethylhexyl salicylate metabolites were investigated quantitatively after oral dosing in three volunteers each. The applicability of the metabolites as exposure biomarkers was investigated in a dermal pilot study (n=1) and in a pilot population from the general population (n=35). Urinary biomarker concentrations were determined using online-SPE-LC-MS/MS.
Results: After oral dosing, 45% of the OC dose was excreted as 2-cyano-3,3-diphenylacrylic acid, 0.13% as dinor octocrylene carboxylic acid, and 0.008% as 5-hydroxy-octocrylene. 0.28% of EHS was excreted as 5-hydroxy-2-ethylhexyl salicylate, 0.24% as 5-carboxy-2-ethylpentyl salicylate, and 0.11% as 5-oxo-2-ethylhexyl salicylate. For both OC and EHS at least one of these metabolites could be quantified in 91% of urine samples from the pilot population. The highest OC biomarker concentrations were measured for sunscreen users and the highest EHS biomarker concentrations for users of sunscreens or personal care products with sun protection factor. After dermal application, EHS biomarkers were markedly increased for several days. In contrast, OC biomarker levels were only slightly increased. Daily intakes for the pilot population were calculated using the toxicokinetic data.
Conclusions: The newly developed human biomonitoring method is a valuable tool for measuring occupational as well as background OC and EHS exposures. The extent of occupational exposures to these UV filters can thus be robustly quantified. The toxicokinetic data allow systemic UV filter intakes to be estimated. A quantitative risk assessment will thus be possible if toxicologically derived threshold values are available.
Keywords: human biomonitoring – UV filter – octocrylene – ethylhexyl salicylate – biomarker
Expositions-Biomarker für die UV-Filter Octocrylen und 2-Ethylhexylsalicylat
Zielstellungen: In den vorgestellten Studien werden Expositionsbiomarker für die weit verbreiteten organischen UV-Filter Octocrylen (OC) und 2-Ethylhexylsalicylat (EHS) sowie ein empfindliches analytisches Verfahren für ihre Bestimmung in Urin beschrieben.
Methoden: Die Bildung und Ausscheidung von je drei spezifischen Octocrylen- und 2-Ethylhexylsalicylat-Metaboliten wurde nach oraler Dosierung an je drei Probanden quantitativ untersucht. Die Anwendbarkeit der Metaboliten als Expositions-Biomarker wurde in einer dermalen Pilotstudie an einem Probanden sowie in einer Pilotpopulation (n=35) aus der Allgemeinbevölkerung untersucht. Die Analyse der Biomarker erfolgte mittels Online-SPE-LC-MS/MS.
Ergebnisse: Nach oraler Dosierung wurden 45 % der OC-Dosis als 2-Cyano-3,3-diphenylacrylsäure, 0,13 % als Dinor-Octocrylen-Carbonsäure und 0,008 % als 5-Hydroxy-Octocrylen ausgeschieden. EHS wurde zu 0,28 % als 5-Hydroxy-2-ethylhexylsalicylat, zu 0,24 % als 5-Carboxy-2-ethylpentylsalicylat und zu 0,11 % als 5-Oxo-2-ethylhexylsalicylat ausgeschieden. Für beide UV-Filter konnten in jeweils 91 % der Urinproben der Pilotpopulation Gehalte von mindestens einem dieser Metaboliten quantifiziert werden. Die höchsten Gehalte wurden im Falle von OC für Anwender von Sonnenschutzmitteln und im Falle von EHS für Anwender von Kosmetika mit UV-Schutz und/oder Sonnenschutzmitteln gemessen. Für EHS wurden nach experimenteller dermaler Anwendung deutlich erhöhte Biomarker-Gehalte über einen Zeitraum von mehreren Tagen gemessen. Im Gegensatz dazu stiegen OC-Biomarker-Gehalte nur wenig an. Anhand der toxikokinetischen Daten wurden exemplarisch tägliche Aufnahmen für die Pilotpopulation berechnet.
Schlussfolgerungen: Die entwickelte Human-Biomonitoring-Methode stellt ein geeignetes Werkzeug für die Erfassung arbeits- und umweltmedizinisch relevanter OC- und EHS-Belastungen dar. Das Ausmaß beruflicher Belastungen gegenüber diesen UV-Filtern kann somit robust quantifiziert werden. Die toxikokinetischen Daten erlauben die Abschätzung der in den Körper aufgenommenen UV-Filtermengen. Bei Vorliegen noch abzuleitender toxikologisch begründeter Grenzwerte wird somit eine quantitative Risikobewertung möglich sein.
Schlüsselwörter: Human-Biomonitoring – UV-Filter – Octocrylen – Ethylhexylsalicylat – Biomarker
Einleitung
Bei Tätigkeiten im Freien (berufliche, wie private) werden Sonnenschutzmittel angewendet, um Risiken durch den UV-Anteil der Sonnenstrahlung (Sonnenbrand, Hautalterung und Hautkrebs) zu minimieren. Der UV-Schutz in Sonnenschutzmitteln wird durch UV-Filter erreicht, die diesen Anteil der Sonnenstrahlung entweder reflektieren oder absorbieren. Einige organische UV-Filter stehen allerdings im Verdacht, allergische Reaktionen hervorzurufen oder hormonartig zu wirken (z. B. Gilbert et al. 2013; Balázs et al. 2016). So liegen beispielsweise für die beiden weltweit in großen Mengen eingesetzten UV-Filter Octocrylen (2-Ethylhexyl-2-cyano-3,3-diphenylacrylat; OC) und 2-Ethylhexylsalicylat (EHS) Hinweise auf eine mögliche hormonelle Wirksamkeit aus In-vitro-Studien vor (Kunz u. Fent 2006; Balázs et al. 2016; Miller et al. 2001; Morohoshi et al. 2005; Jiménez-Díaz et al. 2013). Im Falle von OC konnte dieser Verdacht im Tierversuch allerdings nicht bestätigt werden (European Chemicals Agency). Für EHS ist eine Stoffbewertung auf europäischer Ebene hinsichtlich möglicher hormonartiger Wirkungen geplant, aber noch nicht angelaufen (European Chemicals Agency – CoRAP). Für OC berichten außerdem mehrere Studien über photoallergische Kontaktdermatitiden (z. B. The European Multicentre Photopatch Test Study Taskforce 2012).
Zielsetzung
In den hier vorgestellten Studien werden erstmals spezifische Metaboliten von OC und EHS beschrieben, die als Expositionsbiomarker geeignet sind, sowie ein empfindliches analytisches Verfahren für deren Bestimmung in Urin.
Eine objektive Risikobewertung setzt neben der Kenntnis des Gefährdungspotenzials der eingesetzten UV-Filter auch Kenntnis über die Expositionshöhe bzw. die systemisch verfügbare Dosis voraus. Da die Exposition primär durch Anwendung von Sonnenschutzmitteln und anderen Kosmetika auf der Haut erfolgt, ist zur Expositionsabschätzung das Human-Biomonitoring das Mittel der Wahl. Bis vor kurzem standen jedoch für OC und EHS weder geeignete Biomarker noch Analysenverfahren zur Verfügung.
Methoden
Im Rahmen eines Kooperationsprojekts mit dem Umweltbundesministerium (BMU) und dem Verband der Chemischen Industrie (VCI) (nähere Details s. Danksagung) erhielten je drei gesunde männliche Probanden eine exakt bemessene orale Dosis von jeweils ca. 5 mg Octocrylen bzw. 2-Ethylhexylsalicylat (Bury et al. 2019a, b). Zusätzlich wurde eine anwendungsnahe dermale Pilotstudie (Auftragung von 10,9 g einer kommerziell erhältlichen Sonnencreme mit 2 % OC und 5 % EHS) an einem männlichen Probanden durchgeführt. Urinproben wurden über 48 h (orale Studien) bzw. 96 h (dermale Studie) vollständig gesammelt.
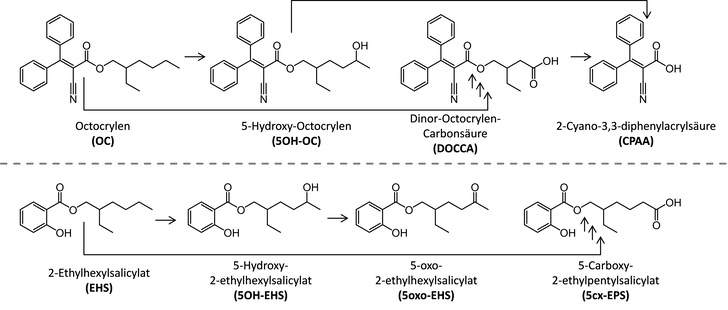
Die OC-Metaboliten CPAA, 5OH-OC und DOCCA sowie die EHS-Metaboliten 5OH-EHS, 5oxo-EHS und 5cx-EPS (s. Abb. 1) wurden nach enzymatischer Spaltung der Glucuronide mittels Online-SPE-LC-MS/MS identifiziert und analysiert. Die Eignung der Metaboliten als Biomarker wurde außerdem in einer Pilotpopulation (n=35; 24 Frauen, 11 Männer; Alter: 23 bis 59 Jahre) ohne bekannte berufliche OC- und EHS-Exposition untersucht (Bury et al. 2018, 2019c). Die Anwendung von Sonnenschutzmitteln und anderen Kosmetika mit UV-Schutz im Vorfeld zur Probensammlung wurde mittels Fragebogen erfasst.
Ergebnisse und Diskussion
Nach oraler Dosierung wurden jeweils drei spezifische Metaboliten beider UV-Filter identifiziert (➥ Abb. 1). Da es sich um zuvor nicht beschriebene Metaboliten handelte, mussten analytische Standards in Auftragssynthese hergestellt werden.
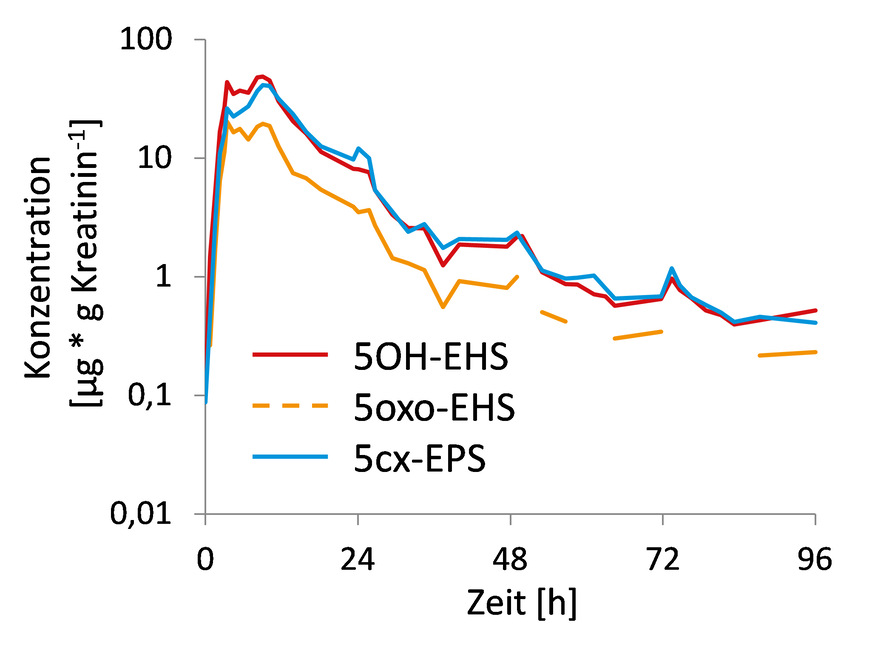
Sowohl für OC als auch für EHS waren in über 90 % der Urinproben der Pilotpopulation ein oder mehrere ihrer Biomarker nachweisbar und auch quantifizierbar (Bury et al. 2018, 2019c). Die höchsten Octocrylen-Biomarker-Gehalte wurden in Urinproben derjenigen Probanden gemessen, die in den vorangegangenen fünf Tagen Sonnenschutzmittel angewendet hatten (n=3). Dennoch war nach dermaler Applikation lediglich ein moderater, aber auch langsamerer Anstieg der Gehalte der Octocrylen-Biomarker CPAA und 5OH-OC zu erkennen (Bury et al. 2019a). Dies deckt sich mit der geringen Hautgängigkeit von Octocrylen in vitro (Hayden et al. 2005; Potard 1999). Da bei der dermalen Pilotstudie eine Aufnahme der UV-Filter über den Mund weitestgehend vermieden wurde, könnten die höheren Biomarkergehalte die in der Pilotpopulation für Sonnencreme-Anwender beobachtet wurden, auf eine größere Bedeutung einer zusätzlichen oralen Aufnahme (z. B. bei Gesichtsanwendung über Lippen/Mund, durch Essen von Lebensmitteln mit eingecremten Händen; Rauchen) hinweisen. Hier besteht weiterer Klärungsbedarf. Für EHS wurden in der Pilotpopulation bei Verwendung von Kosmetika mit UV-Schutz (inklusive Sonnencreme) innerhalb von fünf Tagen vor Abgabe der Urinprobe (n=11) höhere Biomarkergehalte gemessen als bei den übrigen Probanden. In der dermalen Pilotstudie (➥ Abb. 2) zeigte sich ein rascher Anstieg der Gehalte aller drei EHS-Biomarker innerhalb weniger Stunden nach Anwendung (Maxima im Bereich von 3 bis 10 Stunden) mit erwartungsgemäß langsamem Abfall der Konzentrationen über den Beobachtungszeitraum von vier Tagen (Bury et al. 2019c).
Die aus der oralen Dosierungsstudie gewonnenen Toxikokinetikdaten bilden die Grundlage für eine Expositionsabschätzung mittels Human-Biomonitoring. So ermöglicht die Kenntnis der Anteile, zu denen die beiden UV-Filter nach oraler Aufnahme in ihre entsprechenden Biomarker verstoffwechselt und über den Urin ausgeschieden werden (Konversionsfaktoren), die Abschätzung der jeweils in den Körper aufgenommenen Mengen der UV-Filter. Octocrylen wurde im Mittel der drei Probanden zu 45 % als CPAA, 0,13 % als DOCCA und 0,008 % als 5OH-OC über den Urin ausgeschieden. EHS wurde zu 0,28 % als 5OH-EHS, 0,24 % als 5cx-EPS und 0,11 % als 5oxo-EHS ausgeschieden. Auf Basis dieser Konversionsfaktoren wurden nach dermaler Applikation 3,0 % der aufgetragenen EHS-Menge in den Körper aufgenommen. Dieser Wert ist in guter Übereinstimmung mit der in vitro ermittelten dermalen biologischen Verfügbarkeit von 1,82 ± 1,5 % (unveröffentlichte Studie der Symrise AG). Die ermittelten Konversionsfaktoren wurden angewendet, um auf Basis der Pilotpopulation erstmals exemplarisch tägliche Aufnahmedosen abzuschätzen. Die höchsten Werte lagen, bei 74 µg/(kg * d) Octocrylen und 63 µg/(kg * d) EHS. Derzeit fehlen allerdings toxikologisch begründete Grenzwerte (z. B. tolerierbare tägliche Aufnahmen – „tolerable daily intake“ , TDI), um auf Basis solcher Daten eine Risikobewertung vorzunehmen.
Schlussfolgerungen
Mit den entwickelten Human-Biomonitoring-Methoden stehen geeignete Werkzeuge für die quantitative Erfassung arbeitsmedizinisch und umweltmedizinisch relevanter Octocrylen- und 2-Ethylhexylsalicylat-Belastungen zur Verfügung. Die gewonnenen toxikokinetischen Daten erlauben die Abschätzung der in den Körper dermal und ggf. oral aufgenommenen Mengen der UV-Filter. Bei Vorliegen noch abzuleitender toxikologisch begründeter Grenzwerte wird somit eine quantitative Risikobewertung möglich sein, anhand derer Handlungsempfehlungen basierend auf einer Nutzen-Risiko-Abwägung gegeben werden können.
Ethikkommissions-Votum: Für die vorgestellten Studien lagen Vota der Ethikkommission der Medizinischen Fakultät der Ruhr-Universität Bochum vor (Registrier-Nummern: 3867−10 und 4288−12).
Danksagung: Die vorgestellten Studien wurden im Rahmen eines auf zehn Jahre angelegten Kooperationsprojekts zwischen dem Bundesumweltministerium (BMU) und dem Verband der Chemischen Industrie e.V. (VCI) durchgeführt. In diesem durch das Umweltbundesamt (UBA) koordinierten Projekt sollen für 50 Substanzen Expositionsbiomarker, sowie Human-Biomonitoring-Verfahren für deren Analyse entwickelt werden.
Interessenkonflikt: Die Autoren geben an, dass keine Interessenkonflikte vorliegen.