Die Arthrose ist multifaktoriell verursacht und vor allem auf Veränderungen mit dem Lebensalter, genetische Anlagen und metabolische Prozesse des Knorpelstoffwechsels begründet. Mechanische Faktoren der Belastung ordnen sich in diese Bedingungen ein, indem sie je nach Höhe und Dauer zu einer vorzeitigen oder verstärkten Arthrose beitragen oder als plötzliche so genannte Impulsbelastungen Initialschäden setzen können. Schäden des hyalinen Gelenkknorpels sind in zwei Formen (degenerativer Knorpelschaden durch sinkende Matrixsynthese und Apoptose, traumatischer Knorpelschaden) pathophysiologisch entscheidend. Gesunde Gelenke sind zur Bewältigung hoher physischer Belastungen fähig, ohne geschädigt zu werden. Die beruflichen Risiken sind belastungs- und somit gelenkspezifisch. Nicht immer stehen epidemiologisch nachgewiesene Krankheitsrisiken in Übereinstimmung mit den vermuteten Kausalzusammenhängen.
Beim Übergewicht ist der Gelenkknorpel der großen tragenden Gelenke – Knie, Hüfte, Fußgelenk – Belastungen ausgesetzt, die Arthrosen weitgehend mechanisch erklären können. Kniegelenke sind bei gleicher metabolischer Konstellation stärker vom Übergewicht betroffen als Hüftgelenke. Den Einfluss metabolischer Faktoren auf die Genese zeigen Beziehungen zu Parametern des Fettstoffwechsels, zu Entzündungsmediatoren, zum Vitamin-D-Stoffwechsel, zu freien Sauerstoff- und Stickstoff-Radikalen sowie zu Mikro-RNA.
Das Alter ist global der führende Faktor für die Arthrose. Mit steigendem Alter sinkt die Belastbarkeit des Knorpelgewebes und damit steigt das Schädigungsrisiko des Knorpels der Gelenke.
Der Einfluss von Sport ist ambivalent: Die große Belastungstoleranz von gesundem Knorpel führt dazu, dass mittlere Laufbelastungen keine erheblichen Schäden an den Gelenken verursachen und zur muskulären Stabilisierung und Verbesserung der Propriozeption beitragen. Extreme Sportbelastungen verbunden mit traumatischen Ereignissen erhöhen dagegen das Arthroserisiko.
Insgesamt ist festzustellen, dass sich viele pathogenetische Prozesse der Entstehung der Arthrose noch in der Klärungsphase der Forschung befinden. Das betrifft insbesondere die Zusammenhänge mit Arbeitsbelastungen hinsichtlich der Art, Höhe und Dauer dieser Belastungen.
Was ist eine Arthrose?
Arthrosen zählen weltweit zu den häufigsten orthopädischen Erkrankungen (Driban et al. 2015). Dies kann alle Gelenke des menschlichen Körpers betreffen, bei den großen Gelenken vor allem die Hüfte, das Kniegelenk und das Sprunggelenk. Bei den kleinen Gelenken betrifft die Arthrose vor allem die Fingergelenke, das Großzehengrundgelenk sowie auch die Wirbelgelenke.
Als Arthrose („Arthrosis deformans“) wird eine chronische schmerzhafte, zunehmend funktionsbehindernde Gelenkveränderung infolge eines Missverhältnisses von Tragfähigkeit und Belastung bezeichnet.
Als Stadien kann man allgemein unabhängig von Einteilungen für einzelne Gelenke unterscheiden:
- Präarthrose: Es handelt sich um ultrastrukturelle Veränderungen, vor allem innerhalb des hyalinen Knorpels, die sich der bisher verfügbaren Diagnostik (Röntgen, MRT, Arthroskopie) entziehen. Dabei kann angenommen werden, dass bei einem großen Teil derjenigen Patienten, die unter Gelenkproblemen ohne fassbaren objektiven Befund (funktionelle Beschwerden) leiden, solche Mechanismen bereits eine Rolle spielen.
- Latente Arthrose, die durch gezielte (insbesondere bildgebende) Untersuchung nachweisbar ist, jedoch noch klinisch stumm bleibt;
- aktivierte, symptomatische Arthrose mit klinischen Zeichen der Überbeanspruchung des Gelenks;
- Gelenkversagen, Gelenkkollaps.
Im angloamerikanischen Sprachraum wird in der Regel der Begriff „Osteoarthris“ verwendet. Dieser Begriff ist in Bezug zur Pathophysiologie, mit Ausnahme rheumatischer Erkrankungen oder postinfektiöser Zuständen inkorrekt. Die Arthrose ist primär eine nichtentzündliche Erkrankung. Allerdings geht die aktivierte symptomatische Arthrose häufig mit Symptomen einher, die den klassischen Entzündungszeichen nach Galen entsprechen: Tumor (Erguss und Schwellung), Calor (Erwärmung), gelegentlich sogar mit Beteiligung der Schleimbeutel (Rubor) und einer aufgehobenen Funktion/Gelenkversagen im Sinne einer Functio laesa.
Im deutschsprachigen Raum wird die „Arthrose“ aufgrund des Umstands, dass ein Gelenk mechanisch beansprucht wird, oft als „Verschleißerkrankung“ definiert. Im naturwissenschaftlich-philosophischen und wissenschaftstheoretischen Sinn ist dies ebenso nicht korrekt.
Der Begriff Verschleiß stammt aus der Technologie/Materialkunde. Er ist definiert als „fortschreitender Materialverlust aus der Oberfläche eines festen Körpers (Grundkörper), hervorgerufen durch mechanische Ursachen, d. h. Kontakt- und Relativbewegung eines festen, flüssigen oder gasförmigen Gegenkörpers“, also den Masseverlust (Oberflächenabtrag) einer Stoffoberfläche durch schleifende, rollende, schlagende, kratzende, chemische und thermische Beanspruchung (DIN 50320). Erst nach Resektion des Gelenks im Rahmen einer Endoprothesenimplantation, bei dem es zu einer mechanischen Beanspruchung von „Werkstoffen“ kommt, wäre auch die Aufnahme des Verschleißbegriffes in der Orthopädie korrekt (Tribologie).
Klinische Zeichen beginnen mit der Anamnese: Typisch für eine Arthrose sind Belastungsschmerzen, Anlaufschmerzen und Morgensteifigkeit, Gelenkknirschen (Krepitationen), Ruheschmerzen im fortgeschrittenen Stadium, aber auch verspannte Muskeln und Sehnen sowie Bewegungseinschränkungen und Schonhaltung. Bei ausgeprägter Arthrose kommen Gelenkentzündungen (aktivierte Arthrose) und Gelenkerguss (insbesondere bei Kniearthrose) mit Gelenkschwellungen sowie Muskelschwäche und Instabilität des Gelenks hinzu. Diese Einteilung stützt sich insbesondere auf das am häufigsten von einer Arthrose betroffene große Gelenk, das Kniegelenk, und sie kann in entsprechender Weise auf andere, auch kleinere Gelenke übertragen werden.
Zu den Arthrosen wird allgemein nicht die Arthrose der kleinen Wirbelgelenke, der sog. Facettengelenke als Spondylarthrose, gezählt. Sie folgt jedoch den gleichen Kriterien wie andere Arthrosen und ist zugleich häufigster Auslöser von spezifischen durch Bandscheibenschäden verursachten Rückenschmerzen. Sie erklärt die Mehrzahl der tatsächlich mit einer dauerhaften Bandscheibenschädigung mit Verschmälerung des Zwischenwirbelraums und veränderten Beziehungen der benachbarten Gelenkflächen zueinander verknüpften lokalen Rückenschmerzen.
Für die klinische Untersuchung des Betriebsarztes steht die Methode fokus (Funktionsorientierte Körperliche Untersuchungssystematik von Spallek u. Kuhn 2009) zur Verfügung. Sie berücksichtigt die anamnestischen und klinischen Zeichen der Arthrosen großer Gelenke, bezieht jedoch keine bildgebende Diagnostik ein.
Eine Diagnose von Arthrosen allein aufgrund von Anamnese und klinischen Zeichen zu stellen, ist nur in fortgeschrittenen klinischen Stadien diagnostisch sicher, auch wenn das in einem Teil der epidemiologischen Studien, z. B. auf der Basis von Telefonumfragen, geschieht. Andererseits ist die bildgebende Diagnostik allein ebenso in ihren Möglichkeiten eingeschränkt. Beginnende, aber auch fortgeschrittene morphologische Zustandsbilder können selbst unter erhöhten physischen Belastungen ohne klinische Relevanz bleiben. Andererseits stellen Röntgenuntersuchungen nur in der Strahlung schattengebende Veränderungen dar, die bei der Arthrose mit Verschmälerung des Gelenkspalts und der Anlagerung von Osteophyten (ab Kellgren Grad 2 gelingt eine sichere Einstufung) in der Regel bereits ein fortgeschrittenes Stadium der Arthrose anzeigen. Das CT stellt in dieser Hinsicht keinen Vorteil gegenüber dem konventionellen Röntgen dar. Konventionelles Röntgen ist deshalb bei der Klärung des klinischen Verdachts einer Arthrose weiterhin die Methode der Wahl. Die Kernspintomographie ist dagegen geeignet, durch die Darstellung des Knorpels und weiterer Gelenkstrukturen frühzeitiger zeitweilige reversible Funktionsstörungen zu erkennen. Sie ist deshalb besser und schonender als die invasive Arthroskopie zur Diagnostik von Knorpeldefekten geeignet. Der prognostische Wert vieler zeitweiliger im MRT erkennbarer Veränderungen ist dagegen unsicher.
Häufigkeit des Vorkommens von Arthrosen
Objektive Daten zur Häufigkeit von Arthrosen sind in Deutschland nahezu nicht vorhanden. In epidemiologischen Studien wird der Begriff „Arthrose“ in unterschiedlicher Weise verwendet. Groß angelegte bevölkerungsbasierte Querschnitts- bzw. Längsschnittuntersuchungen basieren häufig auf Befragungen. Dazu werden verschiedene anamnestische und klinische Kriterien verwendet. Das Robert-Koch-Institut schätzt aus einer Telefonbefragung die Arthroseprävalenz in Deutschland, unabhängig von Lokalisation und Lebensalter, bei Männern auf 17,9 % und bei Frauen auf 22,6 % (Rabenberg 2013 – Gesundheitsberichterstattung des Bundes). Die daraus resultierenden direkten und indirekten Kosten werden auf 5–6 Euro/Person und Jahr geschätzt. Vergleichbare Zahlen geben Hootman et al. (2006) aus dem National Health Interview Survey 2003 der USA mit 17,3 % (Männer) und 21,6 % (Frauen) an.
Bedingt durch unterschiedliche Definitionen des Begriffs „Arthrose“ variieren Angaben bezüglich der Häufigkeiten, aber auch der Risikofaktoren in der Literatur erheblich. Schäden im Bereich des hyalinen Gelenkknorpels sind das entscheidende pathophysiologische Moment dieser Erkrankung. Dabei sind zwei Formen der Knorpelschädigung zu unterscheiden,
- der durch sinkende Syntheseleistung der Matrix und Apoptose bedingte „degenerative Knorpelschaden“ und
- der im Rahmen von Verletzungen der Gelenke auftretende „traumatische Knorpelschaden“.
Beide Formen dieser Schädigung können sich aufgrund der erlebten Belastungen im Lebensverlauf allerdings überschneiden. In vielen epidemiologischen und klinischen Untersuchungen wird nicht zwischen beiden pathophysiologisch grundsätzlich unterschiedlichen Entitäten unterschieden.
Das American College of Rheumatology (ACR) definiert die Gonarthrose beispielsweise als Kombination folgender Symptome: Knieschmerz und Krepitus (Morgensteifigkeit über 30 Minuten) und Alter über 38 Jahre. Dabei wird eine Sensitivität in Bezug auf eine radiologische Arthrose von 89 % und eine Spezifität von 88 % angegeben. Die Koxarthrose wird definiert: Schmerzen in der Leiste und Innenrotation
In den meisten epidemiologischen Untersuchungen zur Bestimmung von assoziierten bzw. Risikofaktoren für Arthrosen werden radiologische Kriterien (subchondrale Sklerose, Gelenkspaltverschmälerung, Osteophyten, Destruktion des Gelenks) verwendet. Dazu haben sich verschiedene Klassifikationen etabliert. Die älteste und bekannteste Klassifikation wurde von Kellgren und Lawrence (1957) vorgeschlagen. Diese Klassifikationen haben im Laufe der Jahre aber auch erhebliche Modifikationen erfahren. Ausgehend von diesen Klassifikationen werden die Arthrosen oftmals als „leicht“ (KL = 0/1), „moderat“ (KL = 1/2-3) oder „schwer“ (KL = 3/4) definiert. Allein diese unscharfen Möglichkeiten einer Definition des Arthrosebegriffs verdeutlichen, wie hoch die Inter-Observer-Varianz bei der Bestimmung der Arthrose ist.
In den letzten Jahrzehnten wurde die Kernspintomographie (MRT) zu einem wesentlichen Instrument in der Diagnostik von Knorpelschäden. Die MRT ist die einzige Methode, mit der es nichtinvasiv möglich ist, Knorpelschäden relativ sicher nachzuweisen. Allerdings hängen Sensitivität und Spezifität von der technischen Ausstattung (Leistungsfähigkeit der MRT-Geräte variiert zwischen 1,0 Tesla und 3,0 Tesla), der unterschiedlichen Validität je nach Knorpeldicke (Patella versus kleine Gelenke) und von der jeweils verwendeten Gradeinteilung ab.
Bereits in der ersten groß angelegten Querschnittsuntersuchung konnten Kellgren und Lawrence zeigen, dass in etwa 30 % der Fälle radiologisch nachweisbarer Arthrose des Knie- und Hüftgelenks keinerlei klinische Symptome bestanden.
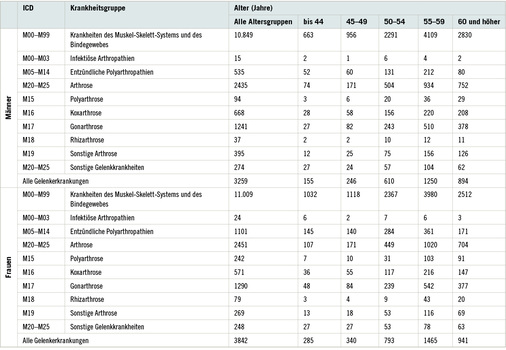
Eine Information über das Auftreten arbeitsrelevanter Arthrosen bietet unter dem Vorbehalt, dass sich die Gründe der Erwerbsunfähigkeit auch an den realen Möglichkeiten zur Ausübung der beruflichen Tätigkeit spiegeln, die Statistiken der Deutschen Rentenversicherung über die Ursachen der Erwerbsunfähigkeit. Bezogen auf die Fälle wegen Erwerbsunfähigkeit (jeweils 1. Diagnose) ergaben sich für das Jahr 2014 die in Tabelle 1 dargestellten Häufigkeiten bei Erkrankungen der Gelenke (nach Statistik der Deutschen Rentenversicherung – Rentenzugang des Jahres 2014, Band 203). Daraus geht hervor:
- Der Anteil der Gelenkerkrankungen an allen Rentenursachen wegen Muskel-Skelett-Erkrankungen beträgt bei Männern 30,0 % bei Frauen 34,9 %.
- Etwa zwei Drittel (bei Männern 65,7 %, bei Frauen 62,6 %) treten nach dem 54. Lebensjahr ein.
- Die Gonarthrose und die Koxarthrose dominieren unter den Gelenkerkrankungen mit Anteilen von 58,6 % bei den Männern und 48,4 % bei den Frauen. Im Erwerbsalter ist die Gonarthrose etwa doppelt so häufig wie Koxarthrose.
Zur Pathophysiologie der Arthrose
Der Gelenkknorpel ist die entscheidende Struktur für die Funktion jedes Gelenks und deshalb ist das Verständnis von seiner Funktion entscheidend für die Betrachtung der Arthrose und des Risikos ihrer Entstehung. Gesunder Knorpel hat eine relativ hohe mechanische Belastbarkeit zwischen 5 und 30 MPa (= 5–30 N/mm2), die proportional zum Grad der histologischen Schädigung abnimmt. Entsprechend der mechanischen Belastung des jeweiligen Gelenks ist die hyaline Knorpelschicht des Gelenks unterschiedlich dick, zwischen bis zu 15 mm retropatellar und 0,2 mm an den Fingergelenken. Dicker Knorpel an den Hauptbelastungszonen ist in der Regel weicher als dünner Knorpel in den wenig belasteten Zonen.
Allerdings kann dies nicht auf alle Gelenke übertragen werden. So finden sich auf der Medialseite des Talus die höchsten Druckbelastungen aller Gelenke des menschlichen Körpers. Gerade hier beträgt die durchschnittliche Dicke des Knorpels nur maximal 1,5 mm. Histologisch ist jedoch bekannt, dass in diesem Bereich der hyaline Gelenkknorpel einen anderen Zonenaufbau hat als z. B. der Knorpel des Kniegelenks. Hier finden sich mehr flache Chondrozyten, die eher das Aussehen eines Fibrozyten haben, und in diesem Bereich ist der Kollagen-II-Gehalt wesentlich höher als im Kniegelenk. Dies mag ein Beleg dafür sein, dass die Kenntnisse über die Pathophysiologie für die einzelnen Gelenke des menschlichen Körpers nicht unkritisch miteinander vergleichbar sind. Bei den meisten Gelenken/Gelenkflächen des menschlichen Körpers wurde die biochemische und histologische Struktur bislang nur sehr wenig untersucht.
Der Gehalt an Knorpelzellen macht nur etwa 5 % der Knorpelmasse aus, der Rest besteht aus wasserreicher extrazellulärer Matrix (ca. 70 % Wasser) mit Kollagen (60 % der Trockenmasse), Proteoglykanen (30 % der Trockenmasse) und weiteren Proteinen (Nichtkollagen-/Nicht-Proteoglykan-gebundene Proteine – 10% der Trockenmasse).
Die degenerativen Veränderungen sind bei der Arthrose nicht auf den Knorpel beschränkt, sondern erfassen die Synovia und Gelenkkapsel, den angrenzenden subchondralen Knochen und die gesamte benachbarte Struktur einschließlich der Gelenke. Die Synovia und die von ihr produzierte Gelenkflüssigkeit versorgen durch Diffusion den Knorpel mit Sauerstoff und Nährstoffen, beseitigen Stoffwechselendprodukte und tragen zur Reduktion der Reibung im Gelenk bei. Bei der durch Degeneration bedingten Reduktion des Knorpelpuffers reagiert der subchondrale Knochen durch eine Sklerose mit Sinterung des Knochens und Neuformation der Trabekelstruktur sowie Dickenzunahme der Tidemark (Grenzschicht Knorpel/Knochen) sowie Kalzifikation der unteren Knorpelschichten. Bei fortschreitender Degeneration treten zunehmend randständige Exophyten (Osteophyten) auf, die als biologische Antwort auf die zunehmende Druckbelastung der Gelenkflächen gedeutet werden und der Flächenvergrößerung dienen soll.
Als Ursachen der Arthrose gelten je nach Auffassung der Autoren das Alter, die Fettsucht, Gelenktraumata, Gelenkinstabilität, genetische Faktoren mit Beziehungen zu metabolischen oder endokrinen Erkrankungen (Mobasheri 2015), aber auch Über- und Fehlbelastungen durch plötzliche hohe „Impulsbelastungen“ mit der Folge von Mikrotraumen sowie repetitive oder lang dauernde Belastungen mit der Folge eines gestörten Verhältnisses zwischen Ermüdung und Regeneration des hyalinen Knorpels.
Alter und Arthrose
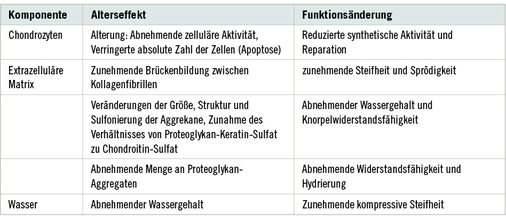
Das Alter ist global betrachtet der führende Faktor für die Entstehung einer Arthrose, wobei diese Veränderungen individuell aufgrund der weiteren hauptsächlichen Faktoren unterschiedlich in Erscheinung treten. Die Entwicklung des Knorpels unterliegt ebenso wie andere Gewebe einem Prozess natürlicher Alterung ( Tabelle 2), darunter der sog. zellulären Apoptose. Aus der Alterungsforschung ist heute bekannt, dass der Verlust der Zellzahl in den Geweben durch zwei Mechanismen hervorgehoben wird:
- die Verkürzung der DNA-Telomere bei jedem Replikationszyklus und damit schließlich die Unfähigkeit zur Zellteilung, die zum „programmierten Zelltod“ führt,
- die Behinderung der Atmungskette durch Kumulation freier Radikale (hier bietet sich ein möglicher therapeutischer Ansatz).
Die Alterung betrifft die Knorpelzellen, aber auch die Matrix (Luria u. Chu 2014; Hwang u. Kim 2015; s. auch Tabelle 2). Alternde Menschen haben deshalb ein generell erhöhtes Arthroserisiko. Dieses unterscheidet sich auf Grund der sehr komplexen Prozesse individuell je nach persönlicher genetischer Ausstattung: Während bei gleichen Lebensumständen einige Personen frühzeitig zur Arthrose neigen, tritt sie bei einigen Personen erst sehr spät ein.
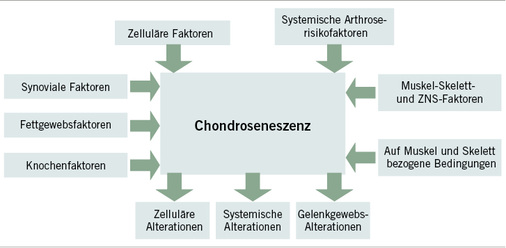
Für den Prozess der Alterung des Knorpels verwenden Mobasheri et al. (2015) den Begriff der Chondroseneszenz ( Abb. 1). Sie bezeichnen damit die Verbindung zwischen intrinsischen Faktoren der Apoptose und extrinsischen Faktoren wie Belastungen, die zu einem veränderten sekretorischen Verhalten der Chondrozyten führen.
Mechanische Belastungen als Teil der Ursachen
Ein Gelenk unterliegt natürlich einer biomechanischen Beanspruchung: Druckbelastung, Scherbelastung und Reibung. Scherbelastung und Reibung sind in einem physiologisch-intakten, bandstabilen Gelenk zu vernachlässigen, so dass der Gelenkknorpel im Wesentlichen auf Druck beansprucht wird. Diese Belastungen führen innerhalb des Gewebes (vor allem im hyalinen Gelenkknorpel) dazu, dass die Struktur kleinere mechanisch bedingte Schädigungen erleidet, diese aber aufgrund der regenerativen Fähigkeiten des Gewebes durch Aktivierung der Synthese wieder ausgeglichen werden. Dabei ist sogar ein gewisser „Trainingseffekt“ der Gewebe möglich (Wolf-Transformationsgesetz). Überschreitet hingegen die Beanspruchung des Gewebes (Knorpels) die Regenerationsfähigkeit oder lässt, bedingt durch verschiedene Mechanismen (z. B. Alter) diese Regenerationsfähigkeit nach, so kommt es zu einem Missverhältnis von Belastung und Belastbarkeit. Dieser Pathomechanismus ist der entscheidende beim Zustandekommen der „idiopathischen/primären“ Arthrose und dürfte gleichermaßen bei allen Gelenken des menschlichen Körpers ablaufen.
Ein weiterer wesentlicher Mechanismus beim Zustandekommen von Arthrosen stellt die Gelenkzerstörung durch eine Verletzung dar. Geht man von der Definition aus, dass eine schwere Arthrose einem „Gelenkkollaps“ entspricht, so führen bereits schwere Verletzungen zu dieser Situation. Gelingt es, unfallchirurgisch das zerstörte Gelenk (nahezu) in seiner Funktion und Anatomie wieder herzustellen, so verbleibt häufig dennoch ein erhöhtes Risiko, eine dem Altersdurchschnitt vorangehende Arthrose in diesem Gelenk zu erleiden (präarthrotische Deformierung nach Hackenbroch, sog. sekundäre Arthrose).
Aus arbeitsmedizinischer Sicht interessiert die Rolle der physischen Belastungen im Arbeitsprozess. Physische Belastungen durch äußere Einflüsse bei der Arbeit, im Sport oder in der Freizeit können zur Entstehung oder Verstärkung einer Arthrose beitragen, können also Teil der Ursachen sein.
Alle Erkenntnisse der Physiologie zeigen zunächst, dass gesunde Gelenke zur Bewältigung hoher physischer Belastungen fähig sind, ohne dadurch geschädigt zu werden. Als Beispiel soll die Belastung der Kontaktflächen der Tibia des Kniegelenks beim Gehen bzw. Treppensteigen dienen, wo nach biomechanischen In-vivo-Messungen zeitweilig das Doppelte bzw. Dreifache des Körpergewichts, bei schneller Ausführung auch deutlich mehr als Druckkraft auftritt. Experimentelle Daten zum Knorpelstoffwechsels unter mechanischer Belastung belegen, dass geringe Belastungen weder katabole noch Entzündungsreaktionen im Knorpel auslösen, hohe Belastungen dagegen ggf. sehr ausgeprägt (Sanchez-Adams 2014).
Belastungen durch Sport
Dem Sport wird eine ambivalente Rolle in der Entstehung der Arthrose beigemessen (Hügle u. Valderrabano 2011). Einerseits trägt der Sport bei besonders intensiver Ausübung, ungenügender muskulärer Vorbereitung und sportartspezifischen Risiken durch Stöße, ruckartige Belastungen, Stürze und anderen Gelenktraumen zur Entstehung der Arthrose bei. In einem aktuellen Review haben Driban et al. (2015) im Vergleich zwischen Sportlern (n = 3759) und Nichtsportlern (n = 4730) eine Prävalenz radiologisch bestätigter Kniearthrosen von 7,7 % bzw. 7,3 % festgestellt. Signifikante Risikoerhöhungen zeigten sich bei Fußballspielern (OR = 3,5), Langstreckenläufern (OR = 3,3), Gewichthebern (OR = 6,9) und Wrestling-Kämpfern (OR = 3,8). Langzeitiges Gehen bewirkte dagegen bei 1179 Studienteilnehmern (darunter 59 % Frauen) im Alter von durchschnittlich 67,0 ± 7,6 Jahren (BMI 29,8 ± 5,3), die 6981 (± 2630) Schritte/Tag gingen, über 2 Jahre keine Gonarthrose bzw. Verstärkung einer milden Gonarthrose bis Grad Kellgren II (Øiestad 2015).
Andererseits wirkt sportliches Training sowohl direkt positiv auf die Erhaltung der normalen Physiologie des Knorpels, allerdings erweist sich Knorpel als nicht trainierbar im Sinn einer funktionellen Adaptation mit wesentlicher Verbesserung seiner Voraussetzungen zur Bewältigung von Belastungen wie Verdickung belasteter Knorpelflächen oder Zunahme der Zahl der Chondrozyten (Eckstein 2006). Die Diskrepanz zwischen morphologischer Veränderung im Gelenk und der Ausprägung einer klinisch relevanten Arthrose wird durch Sport auch verringert, indem die Propriozeption und damit die optimale Ausführung von Bewegungen im Gelenk erhalten und trainiert werden.
Schließlich trägt Sport als Therapie der Arthrose zur Schmerzreduktion bei, fördert die Beweglichkeit und wirkt der Muskelatrophie entgegen. Training beeinflusst aber auch den Spiegel von Interleukin (IL)-10, das antiinflammatorisch sowohl in der Gelenkflüssigkeit als auch im synovialen Gewebe wirkt.
Berufliche physische Belastungen
Mechanische Belastungen im Berufsleben als Ursachen von Arthrosen sind am besten am Knie- und Hüftgelenk untersucht, wenngleich auch hier noch erhebliche Erkenntnislücken bestehen.
Für die beruflichen Belastungen am Kniegelenk hat die Arbeitsgruppe um Spahn im Zusammenhang mit der Verursachung bzw. Begutachtung der Gonarthrose als Berufskrankheit eine Übersicht der Epidemiologie bei kniebelastenden Tätigkeiten angegeben. Der Zusammenhang zwischen arbeitsbedingten Einwirkungen im Knien oder vergleichbaren Kniebelastungen sowie einem signifikant erhöhten Gonarthroserisiko ließ sich nach der obigen Literaturübersicht sowohl in Querschnitts- als auch Fall-Kontroll- und Kohortenstudien nachweisen.
Für den Zusammenhang sprechen Querschnittsstudien bei Berufsgruppen, die einer Kniegelenksbelastung durch Arbeiten im Knien oder Hocken ausgesetzt sind, beispielsweise untertägige Steinkohlebergleute (Kellgren 1957; Lawrense 1955), Bodenleger und Maler (Jensen 2000; Vingard 1991, 1992) sowie Werftschweißer und Schiffsbauer (Kasch 1986; Lindberg 1987). In Studien von Sandmark et al. (2000) sowie Klußmann (2010) ließ sich bei Männern eine Dosis-Wirkungs-Beziehung zwischen arbeitsbedingten Belastungen im Knien und Hocken sowie dem Gonarthroserisiko nachweisen. In der Kohortenstudie von Felson et al. (1991) fand sich bei kniegelenksbelastenden Tätigkeiten im Knien, Hocken oder Kriechen sowie durch häufiges Heben und Tragen von Lastgewichten von mindestens 11 kg ein signifikant erhöhtes Gonarthroserisiko.
Nicht immer stehen epidemiologisch zweifelsfrei nachgewiesene erhöhte Krankheitsrisiken in Übereinstimmung mit den vermuteten Kausalzusammenhängen, die beim Kniegelenk von einem lokal erhöhten Druck auf den Kniegelenksknorpel ausgehen müssten. Die Studie von Klussmann et al. (2010) sowie die Studien von Neubauer et al. (2009) und Spahn et al. (2010) fanden keine signifikanten Unterschiede in der Verteilung der Knorpelschäden in verschiedenen Teilen des Kniegelenks zwischen den Exponierten (statische Kniebelastungen im Sinne der BK-Nr. 2112) und Nichtexponierten. Sie belegen, dass arbeitsbedingt durch Knien, Hocken oder Fersensitz belastete Beschäftigte keine andere Verteilung der Knorpelschäden im Kniegelenk aufweisen als Personen ohne diese Belastungen, somit existiert kein belastungstypisches Verteilungsmuster der Gonarthrose. Dem entsprechen auch biomechanische Erkenntnisse über die Druckbelastung im Kniegelenk beim Knien und Hocken (Glitsch 2009).
Für das Hüftgelenk hat eine interdisziplinäre Gruppe unter der Autorenschaft von Sulsky (2012) in einem Review vergleichbare Zusammenhänge zwischen beruflichen physischen Belastungen und der Koxarthrose untersucht. Es bestanden wie bei vielen anderen epidemiologischen Studien erhebliche Defizite bei der Messung dieser Belastungen im Zusammenhang zwischen physischen Belastungen und Schädigungen des Muskel-Skelett-Systems. Dennoch ergaben sich auch hier Hinweise darauf, dass Expositionen mit schwerer körperlicher Arbeit besonders durch schwere Lasten das Risiko für die Arthrose des Hüftgelenks erhöhen. Für das Treppensteigen und das Springen war der Zusammenhang nicht klar, wogegen es keinen Zusammenhang zwischen der Arthrose des Hüftgelenks und der Arbeit im Sitzen oder Gehen gibt.
In einem systematischen Review zur Frage, ob Gelenkunfälle, sportliche und physische Aktivität, Fettsucht oder berufliche Aktivitäten Prädiktoren der Arthrose sind, kommen Richmond et al. (2013) nach Auswertung von 43 geeigneten aus ursprünglich 1294 Publikationen zu dem Ergebnis, dass insbesondere die Unfälle am Knie (OR 3,8/CI 2,0–7,2) und an der Hüfte (OR 5,0/CI 1,4–18,2) zur Arthrose beitragen. Ähnliche Zusammenhänge werden auch am Sprunggelenk vermutet, jedoch besteht hier ein Defizit bei verfügbaren Publikationen.
Übergewicht
Übergewicht und Fettsucht imponieren zunächst als äußere Zusatzlast auf die Gelenke der unteren Extremitäten, so dass es naheliegend ist, Zusammenhänge der Arthrose zu untersuchen.
Grundsätzlich ist anzumerken, dass auch der Knorpel der Gelenke als lebendes aktives Gewebe ein Optimum seiner Entwicklung zwischen
- regelmäßiger Belastung mit hinreichender Entlastung,
- einer möglichen Überforderung durch plötzliche extreme oder auch dauernde hohe Belastungen mit unterschiedlichen Schädigungsprozessen sowie
- der Unterforderung mit einem Mangel der Adaptation an regelmäßig wirkende Belastungen
ausgesetzt ist.
Durch die Lebensweise insgesamt ist somit der Gelenkknorpel besonders der großen tragenden Gelenke – Kniegelenk, Hüftgelenk, Fußgelenk – unterschiedlichen Prozessen seiner Erhaltung oder seiner Schädigung ausgesetzt, die auch weitgehend mechanisch erklärt werden können.
In einer australischen Kohortenstudie aus dem TEP-Register (Wang 2009) wurden 41.528 Personen (17.049 Männer) zwischen 27 und 75 Jahren über 10 Jahre beobachtet. Darunter fanden sich in 10 Jahren 541 Fälle von Knie- (Alter 68,1 ± 6,9) sowie 468 Fälle von Hüftendoprothesen (Alter 67,3 ± 7,2). Die Adipositas zeigt ein erheblich geringeres Hüft-TEP-Risiko gegenüber dem Knie-TEP-Risiko ( Tabelle 3).
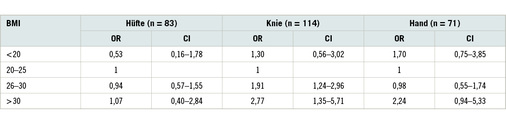
Den zusätzlichen Zusammenhang mit den nicht gewichtstragenden Handgelenken haben Grotle et al. (2008) in einem 10-Jahres-Längsschnitt auf der Basis der Bevölkerungsbefragung einer norwegischen Gemeinde untersucht. Von den ursprünglichen 2891 Teilnehmern (Response 63 %) konnten nach 10 Jahren 1854 Personen erreicht werden. Die Ergebnisse ( Tabelle 4) zeigen, dass das Kniegelenk bereits ab einem BMI > 25 von einem signifikanten Anstieg der Arthrose betroffen ist, dass Hüftgelenk dagegen nicht wesentlich. Die Handgelenksarthrosen erreichen für die Adipositas (BMI > 30) mit einer OR von 2,24 und einem CI von 0,94–5,33 fast die Signifikanzgrenze.
Eine Metaanalyse zum Zusammenhang zwischen Körpergewicht und Gonarthrose von Zheng u. Chen (2015) aus 14 ausgewählten Studien zeigte.
- Für Übergewichtige betrug das Gonarthroserisiko 2,45 (95 % CI 1,88–3,20).
- Für Fettsüchtige (BMI ab 30) betrug das Gonarthroserisiko 4,55 (95 % CI 2,90–7,13)
- Das Risiko einer Gonarthrose steigt je einer Stufe von +5 BMI um 35 %.
Insgesamt ist davon auszugehen, dass Übergewicht wahrscheinlich direkt für die Arthrose am Kniegelenk relevant ist. So zeigt auch eine Studie die größere Inzidenz der Kniebeschwerden bei Schwangeren mit großem gegenüber geringem Zuwachs an Gewicht im Verlauf der Schwangerschaft (Spahn et al. 2015).
Genetische Faktoren bei der Arthroseentstehung
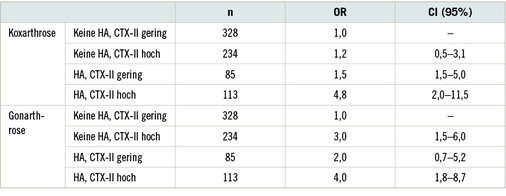
Zur Darstellung der genetisch geprägten Beziehung zwischen verschiedenen Manifestationsorten der Arthrose hatte bereits 2005 Dahaghin im Rahmen der Rotterdam-Arthrose-Studie in einem Follow-up von 1235 Personen von mindestens 55 Jahren ohne Knie- oder Hüftarthrose deren Auftreten innerhalb der nächsten 6,6 Jahre in Abhängigkeit von einer Handarthrose sowie einem genetischen Biomarker (CTX-II = C-Telopeptides of Type II Collagen) untersucht. Insgesamt bekamen 19,7 % der Personen mit und 10,0 % ohne Handarthrose eine Gonarthrose (OR 2,1/CI 1,3–3,3). Das entsprechende Risiko der Koxarthrose lag bei einer OR von 3,0 (CI 1,6–5,4). Die Beziehungen zum Biomarker sind in Tabelle 5 dargestellt.
Vergleichbare epidemiologische Ergebnisse hatte auch die Ulmer Osteoarthrose-Studie (Günther et al. 1998) gezeigt.
In der Ages-Reykjavik-Study (Jonsson 2011) wurde die Schwere der Handarthrose bei Personen untersucht, die eine Totalendoprothese der Knie- oder Hüftgelenke erhalten hatten (2195 Männer und 2975 Frauen, mittleres Alter 76 ± 6 Jahre). Nur drei Faktoren zeigten signifikante Assoziationen: das Übergewicht (BMI), die Schwere der Handarthrose und die Hüftendoprothese. Das höchste Quintil des BMI hatte ein fünffaches Risiko für Knieendoprothesen, verglichen mit dem niedrigsten Quintil (8 % vs. 1,6 %). Eine schwere Handarthrose hatte ein 2,4faches Risiko im Vergleich zu denen ohne Handarthrose (8 % vs. 3,3 %). Es gab jedoch keine statistische Interaktion zwischen BMI und Handarthrose. Exemplarisch soll hier nur das Ergebnis von Klussmann dargestellt werden: In einer deutschen Fall-Kontroll-Studie zur Gonarthrose (Klussmann et al. 2010 – 739 Fälle/571 Kontrollen) war das Risiko einer Gonarthrose erhöht, wenn auch Eltern oder Geschwister an einer Gonarthrose litten (OR 2,2; 95 % CI 1,4–3,4).
Geschlechtsunterschiede der Prävalenz von Knie- und Hüftarthrose stellten Plotnikoff et al. (2015) in einer kanadischen Bevölkerungsstudie (Querschnitt) u. a. für Übergewichtige (BMI > 25) bzw. Fettsüchtige (BMI > 30) fest:
- Bei Männern lag die OR für die Gonarthrose bei 1,90 bzw. 2,90 (beide nicht signifikant), für die Koxarthrose bei 0,81 bzw. 0,99 (beide nicht signifikant).
- Bei Frauen lag die OR für die Gonarthrose bei 1,83 bzw. 6,72 (CI 2,45–18,45, signifikant), für die Koxarthrose bei 2,79 bzw. 6,67 (CI 1,84–24,28, signifikant).
Sie bestätigen das deutlich höhere Arthroserisiko der Frauen gegenüber den Männern, jedoch für die Frauen kein höheres Risiko einer Arthrose des Knie- gegenüber dem Hüftgelenk bei Adipositas.
Aus dem dänischen Knie-Arthroplastik-Register wurden 576 Zwillinge mit einer primären Kniearthrose (358 Frauen, 218 Männer) untersucht (Skousgaard 2016). Es wurde festgestellt, dass die genetische Komponente bei Frauen stärker ausgeprägt war. Insgesamt sollen 18 % der Ursachen auf genetische Gründe, 61 % auf eine „allgemeinsame Umweltkomponente“ (i. S. der allgemeinen Lebensweise) sowie 21 % auf eine „individuelle Komponente“ (i. S. der persönlichen Lebensweise, wohl auch beruflichen Tätigkeit) zurückzuführen sein.
Arthrose als Folge metabolischer Störungen
Bei der Suche nach den Unterschieden zwischen anlagebedingter und belastungsabhängiger Entstehung der Arthrosen ist in den letzten Jahren die Suche nach Stoffwechselveränderungen bei Personen mit Arthrose, darunter insbesondere solcher in Verbindung mit einem metabolischen Syndrom in den Vordergrund getreten.
Loeser (2013) zeigt in einem Review, dass das Wissen um die Rolle der Entzündung bei der Entstehung der Arthrosen derzeit schnell wächst. So gibt es Hinweise, dass proinflammatorische Mediatoren durch alle Gewebsstrukturen eines beeinträchtigten Gelenks hergestellt werden. Im Vordergrund stehen momentan Themen der Epigenetik, der Wnt-Signale der sog. „Signaltransduktion“ zur Übertragung von Einflüssen auf die Zellen durch Proteine, der Entzündungsfaktoren, der Lubricine (PRG4) als Proteoglykane auf der Knorpeloberfläche, des FGF (Fibroblast Growth Factor) zur Regelung des Zellwachstums des Knorpels sowie der Regulation des Knochenwachstums.
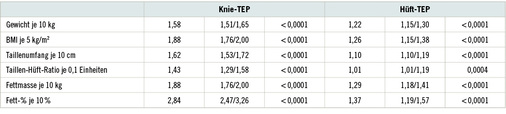
Den Einfluss metabolischer Faktoren auf die Genese der Arthrose haben Wang et al. (2014) in einem aktuellen Review dargestellt (s. Infokasten). Sie zeigen Beziehungen zu Parametern des Fettstoffwechsels, zu Entzündungsmediatoren, zum Vitamin-D-Stoffwechsel, zu freien Sauerstoff- und Stickstoffradikalen sowie zu Mikro-RNA.
Kluzek et al. (2015) fragten in einem Review, ob die Arthrose eine metabolische Erkrankung sei. Sie recherchierten in PubMed die englischsprachige Literatur zwischen Juni 1975 und Oktober 2014 nach den Begriffen „OA/Osteoarthrose“, „MetS/metabolic syndrome“ und „metabolism“, ergänzt durch eine Handsuche und Referenzliteratur aus der Recherche. Es fanden 124 Quellen Berücksichtigung. Sie fanden, dass die symptomatische Hand- und Knie-OA eng mit systemischer metabolischer Fehlregulation assoziiert ist. Der Beitrag von biomechanischen und systemischen Effekten von übermäßigem Fettgewebe ist schwer zu schätzen und unterscheidet sich wahrscheinlich in jedem Gelenk. Die erhöhte Sekretion proinflammatorischer Adipokine ist bei Fettsucht, generell bei älteren Personen und bei Frauen in der Postmenopause, nachzuweisen. Hohe mechanische Belastungen durch die Fettsucht halten die Autoren für eine Teilursache der Gonarthrose und Koxarthrose, die jedoch weder die Beziehung zur Handarthrose noch die Unterschiede zwischen beiden Arthrosen großer Gelenke erklären können. Eine symptomatische Gonarthrose oder Koxarthrose kann zumindest teilweise durch die vom Fettgewebe verursachten Stoffwechselstörungen erklärt werden.
Schlussfolgerungen
- Die Übersichtsdarstellung aktueller Forschungsergebnisse und Statistiken zeigt, dass die Arthrose eine multifaktoriell verursachte Erkrankung ist, die vor allem auf Veränderungen mit dem Lebensalter, auf genetische Anlagen und metabolische Prozesse des Knorpelstoffwechsels begründet ist.
- Mechanische Faktoren der Belastung ordnen sich in diese Bedingungen ein, indem sie je nach Höhe und Dauer zu einer vorzeitigen oder verstärkten Arthrose beitragen oder als plötzliche sog. Impulsbelastungen Initialschäden setzen können, die bei Erreichen des subchondralen Knochens nicht mehr vollkommen reparabel sind.
- Mit steigendem Alter und Beginn von Altersumbauprozessen sinkt die Belastbarkeit des Knorpelgewebes und damit steigt das Schädigungsrisiko des Knorpels der Gelenke.
- Obwohl allen Arthrosen ein gemeinsames biologisches Muster der Entstehung zugrunde liegt, zeigen sie auch lokale Besonderheiten: Die Kniegelenke sind bei gleicher metabolischer Konstellation stärker vom Übergewicht betroffen, was auch auf eine mechanische Teilwirkung schließen lässt, die sich so am Hüftgelenk kaum findet.
- Der Einfluss von Sport ist ambivalent einzuschätzen: Die große Belastungstoleranz von gesundem Knorpel führt dazu, dass mittlere Laufbelastungen trotz hoher Kraftspitzen beim Aufsetzen und Abstoßen der Beine keine erheblichen Schäden an den Gelenken verursachen und zusätzlich zur muskulären Stabilisierung und Verbesserung der Propriozeption beitragen. Extreme Sportbelastungen insbesondere verbunden mit traumatischen Ereignissen erhöhen dagegen das Arthroserisiko.
- Insgesamt ist festzustellen, dass sich viele pathogenetische Prozesse der Entstehung der Arthrose noch in der Klärungsphase der Forschung befinden. Das betrifft insbesondere die Zusammenhänge mit Arbeitsbelastungen hinsichtlich der Art, Höhe und Dauer dieser Belastungen. Davon abzugrenzen sind Fragen der Eignung von Personen mit einer Arthrose für die weitere Beschäftigung unter erhöhten körperlichen Belastungen.
Literatur
Driban JB, Hootman JM, Sitler MR, Harris K, Cattano NM: Is Participation in Certain Sports Associated With Knee Osteoarthritis? A Systematic Review. J Athl Train Jan. 9, 2015 [Epub ahead of print].
Grotle M, Hagen KB, Natvig B, Dahl FA, Kvien TK: Obesity and osteoarthritis in knee, hip and/or hand: an epidemiological study in the general population with 10 years follow-up. BMC Musculoskelet Disord 2008; 2: 132.
Mobasheri A, Matta C, Zákány R, Musumeci G: Chondrosenescence: definition, hallmarks and potential role in the pathogenesis of osteoarthritis. Maturitas 2015; 80: 237–244.
Spahn G, Peter M, Hofmann GO, Schiele R: Knorpelschaden des Kniegelenks und berufliche Belastung. Ergebnisse einer arthroskopischen Studie. Z Orthop Unfall 2010; 148: 292–299.
Sulsky SI, Carlton L, Bochmann F, Ellegast R, Glitsch U, Hartmann B, Pallapies D, Seidel D, Sun Y: Epidemiological Evidence for Work Load as a Risk Factor for Osteoarthritis of the Hip: A Systematic Review. PLoS ONE 2012; 7: e31521.
Wang Y, Simpson JA, Wluka AE, Teichtahl AJ, English DR, Giles GG, Graves S, Cicuttini FM (2009): Relationship between body adiposity measures and risk of primary knee and hip replacement for osteoarthrosis: a prospective cohort study. Arthritis Research & Theapy 2009; 11: R31.
Die vollständige Literaturliste kann beim Autor oder beim Verlag angefordert werden.
Info
Mögliche metabolische oder triggernde Effekte der Osteoarthrose (nach Wang et al. 2014)
- Körperzusammensetzung: Körperfett ist enger als der BMI mit der Kniearthrose verbunden
- Adipokine: Zirkulierende Leptine sind verbunden mit höherem Verlust an Kniegelenksknorpel
- Zytokine: IL-6, TNF-alpha, IL-17 und IL-18 sind mit Kniegelenksknorpelverlust verbunden
- Akutphase-Entzündungskomponenten: CRP ist verbunden mit geringerem Knorpelvolumen
- Nährstoffe: Lipide werden im histologisch geschädigten Knorpel deponiert, HDL und Statine stehen in Beziehung zu sinkendem Risiko, Hyperglykämie hat nachteilige Effekte auf den Knorpel, Diabetes mellitus ist ein unabhängiger Risikofaktor für Arthrose
- Vitamin-D-Defizit: Vitamin-D-Defizit kann durch Entzündungen beeinflusst werden
- Reaktive Stickstoff- und Sauerstoffverbindungen: Beide können Arthrose verstärken in Verbindung mit proinflammatorischen Zytokinen
- Mikro-RNA: Sie sind verknüpft mit Entzündungsprozessen des Knorpels und der Knorpelentwicklung
Für die Autoren
Prof. Dr. med. Bernd Hartmann
Steinbeker Grenzdamm 30 d
22115 Hamburg