MdE-Bemessung bei der BK 1318
Durch die Einführung der BK 1318 („Erkrankungen des Blutes, des blutbildenden und lymphatischen Systems durch Benzol“) 2009 konnte in der Beurteilung des Kausalzusammenhangs und damit der Anerkennung als Berufskrankheit bei diesen Erkrankungen eine Vereinheitlichung erreicht werden. Die Praxis zeigt allerdings, dass die Beurteilung der Folgen einer BK 1318 und die daraus resultierende Einschätzung der Minderung der Erwerbsfähigkeit (MdE) immer noch sehr uneinheitlich sind. In diesem Bei-trag wird ein Vorschlag für eine nach Krankheitsbildern und typischen Krankheits- und Therapiefolgen differenzierte Betrachtung zur MdE vorgestellt.
Schlüsselwörter: Benzol – BK 1318 – Minderung der Erwerbsfähigkeit – Begutachtung
Occupational disease no. 1318 and reduction in earning capacity
In 2009, occupational disease no. 1318 (diseases of the blood and the hematopoietic and lymphatic system caused by benzene) was included on the German list of occupational diseases. The assessment of a causal relationship between benzene exposure and diseases of the blood and the hematopoietic and lymphatic system is well standardized. However, there are still considerable differences concerning the assessment of the reduction in earning capacity. We present a proposal for standardized assessment criteria considering typical disorders and therapies.
Keywords: benzene – occupational disease no. 1318 – reduction in earning capacity – assessment
ASU Arbeitsmed Sozialmed Umweltmed 2016; 51: 211–218
Einleitung
Erkrankungen durch Benzol wurden 1925 unter der BK-Ziffer 1303 in die Berufskrankheitenliste aufgenommen. Standen lange Zeit die akut toxischen Folgen des Benzols im Vordergrund, so sind in den letzten Jahren die durch Benzol induzierten bösartigen Erkrankungen des blutbildenden und lymphatischen Systems in den Fokus gerückt. Lange wurde kontrovers diskutiert, welche Erkrankungen durch Benzol verursacht werden und welche Einwirkungen geeignet sind, von einem Kausalzusammenhang auszugehen (Hoffmann et al. 2001; Woitowitz et al 2003).
Mit Bekanntmachung des Bundesministeriums für Arbeit und Soziales (BMAS) vom 01. 09. 2007 wurde die wissenschaftliche Begründung für die neu in die Anlage zur Berufskrankheitenverordnung aufzunehmende Berufskrankheit „Erkrankungen des Blutes, des blutbildenden und lymphatischen Systems durch Benzol“ vorgelegt, die als BK 1318 am 01. 07. 2009 eingeführt wurde. Hierdurch konnte in weiten Teilen eine Vereinheitlichung in der Beurteilung des Kausal-zusammenhanges und der Anerkennungspraxis erreicht werden, allerdings zeigt die Erfahrung der letzten Jahre, dass insbesondere in der Beurteilung der Erkrankungsfolgen und der Einschätzung der Minderung der Erwerbsfähigkeit (MdE) auch bei gleichgelagerten Fällen teils erhebliche Unterschiede auftreten.
Während für andere Berufskrankheiten Begutachtungsempfeh-lungen mit Hinweisen zur MdE-Bemessung erarbeitet wurden (z. B. Falkensteiner Empfehlung für die Beurteilung asbestbedingter Erkrankungen oder Bamberger Empfehlung zur Beurteilung von Haut-erkrankungen), kann der Gutachter in der Bewertung der Folgen einer BK 1318 bislang nur auf die zur Beurteilung der Non-Hodgkin-Lymphome entwickelte, 2001 von Hoffman et al. veröffentlichte MdE-Tabelle zurückgreifen. So gut dieser Vorschlag seinerzeit auch war, so muss festgestellt werden, dass durch den medizinischen Fortschritt in der Behandlung bösartiger Tumorerkrankungen diese MdE-Tabelle heutige Krankheitsverläufe und Therapien nur unzureichend abbildet. Für die übrigen Krankheitsbilder der BK 1318 liegen keine allgemein akzeptierten Maßstäbe vor. Hinweise zur Beurteilung der Folgen einer BK 1318 können auch der Anlage zu § 2 der Versorgungsmedizin-Verordnung (VersMedV) entnommen werden, wobei zu beachten ist, dass der Beurteilung in der Versorgungsmedizin andere Maßstäbe zugrunde liegen als der Beurteilung im Unfallversicherungsrecht. Im Folgenden möchten wir deshalb einen aktuellen Vorschlag für die MdE-Bemessung bei Krankheitsbildern der BK 1318 vorstellen, der alle malignen Erkrankungen, die als BK 1318 entschädigt werden können, erfasst und differenziert unterschiedliche therapeutische Ansätze und deren Auswirkungen berücksichtigt.
Rechtliche Aspekte
Die Minderung der Erwerbsfähigkeit richtet sich nach dem Umfang der sich aus der Beeinträchtigung des körperlichen und geistigen Leistungsvermögens ergebenden verminderten Arbeitsmöglichkeiten auf dem gesamten Gebiet des Erwerbslebens (§ 56 Abs. 2 Satz 1 SGV VII). Somit sind die individuellen gesundheitlichen Folgen des Versicherungsfalles und die daraus entstehenden Einschränkungen auf dem allgemeinen Arbeitsmarkt zu bewerten. Wie z. B. in der Falkensteiner Empfehlung sehr gut dargestellt, handelt es sich hierbei um eine Funktionsbewertung, die in drei Schritten erfolgt:
- 1.Feststellung des Umfangs und Schweregrades gesundheitlicher Einschränkungen infolge der Berufskrankheit.
- 2.Erstellung eines „negativen Leistungsbildes“ – welche Arbeitsmöglichkeiten sind durch die Folgen der Berufskrankheit verschlossen?
- 3.MdE-Bemessung auf Basis des „negativen Leistungsbildes“ – Beurteilung des Anteils der Arbeitsmöglichkeiten auf dem gesam-ten Gebiet des Erwerbslebens, der durch die Folgen der Berufskrankheit verschlossen ist.
Bei bösartigen Tumorerkrankungen müssen zudem besondere Ge-sichtspunkte beachtet werden. Zwar finden die als „Heilungsbewäh-rung“ bekannten Grundsätze des sozialen Entschädigungsrechts im Recht der gesetzlichen Unfallversicherung keine Anwendung, allerdings sind die besonderen Umstände bösartiger Tumorerkrankungen durchaus zu berücksichtigen wie das Bundessozialgericht 2004 feststellte:
„Bei derartigen Erkrankungen sind bei der Schätzung der MdE entsprechend den Verhältnissen des Einzelfalls ggf. bestehende be-sondere Aspekte der Genesungszeit wie das Vorliegen einer Dauertherapie, ein Schmerzsyndrom mit Schmerzmittelabhängigkeit, An-passung und Gewöhnung an den ggf. reduzierten Allgemeinzustand, die notwendige Schonung zur Stabilisierung des Gesundheitszustandes, psychische Beeinträchtigungen (Antriebsarmut, Hoffnungslosigkeit), soziale Anpassungsprobleme usw., die Auswirkungen auf die Erwerbsfähigkeit haben, wie auch sonst bei der MdE-Bewertung zu berücksichtigen […]. Für eine Art „Risikozuschlag” oder „Gefährdungs-MdE” wegen der Prognoseunsicherheiten hinsichtlich der Entwicklung der Krankheit ist in der auf die verminderten Arbeitsmöglichkeiten bezogenen MdE-Schätzung in der gesetzlichen Unfallversicherung kein Raum, weil auf die Beeinträchtigung des körperlichen und geistigen Leistungsvermögens im Zeitpunkt der Entscheidung abzustellen ist und erst in Zukunft möglicherweise eintretende Schäden grundsätz-lich nicht zu berücksichtigen sind […]. Allerdings ist eine schon bestehende Rückfallgefahr, die bereits vor dem Eintritt des eigentlichen Rückfalls die Erwerbsfähigkeit mindert, bei der Bemessung der gegenwärtigen MdE zu berücksichtigen […]. Dies gilt auch für die anderen genannten Aspekte und ist bei der MdE-Bewertung zu beachten. Ebenso wenig wie jedoch das allgemeine Rezidivrisiko eine pauschale MdE-Erhöhung zu begründen vermag, sondern nur besondere Aspekte der Genesungszeit, führt der bloße Ablauf einer bestimmten rezidivfreien Zeit in der gesetzlichen Unfallversicherung automatisch zu einer MdE-Herabsetzung. Es bedarf vielmehr einer Besserung der zuvor der MdE-Bemessung zugrunde gelegten Funktionsbeeinträchtigungen bzw. besonderen Aspekte, die die Erwerbsfähigkeit beeinflussen“ (BSG, Urteil vom 22. Juni 2004 – B 2 U 14/03 R –, SozR 4-2700 § 56 Nr. 1, BSGE 93, 63–69).
In der Vergangenheit wurden bei der Bemessung der MdE bei bösartigen Tumorerkrankungen oft 5-Jahres-Überlebenszeiten zugrunde gelegt (z. B. Lungenkarzinome) und analog zur Heilungsbewährung meist eine MdE von 100 % für drei bis fünf Jahre an-genommen. Neben der Problematik, dass Grundsätze der Heilungs-bewährung in dieser Form nicht auf das Unfallversicherungsrecht übertragbar sind, stammt diese Vorgehensweise aus einer Zeit, als die Prognose von bösartigen Tumorerkrankungen meist infaust und die Therapiemöglichkeiten begrenzt waren. Allerdings gibt es in neuerer Zeit Ansätze, diese Praxis zu verlassen und die MdE individuell nach den bestehenden Einschränkungen zu beurteilen (z. B. Larynxkarzinome). Bei den malignen Erkrankungen des blutbildenden und lymphatischen Systems besteht zudem die Besonderheit, dass auch über längere Zeiträume teils komplette Remissionen erreicht werden können, ohne dass von einer Heilung ausgegan-gen werden kann. Dies betrifft insbesondere einige Formen der Non-Hodgkin-Lymphome. Bei der Beurteilung solcher Krankheitsverläufe stößt eine MdE-Beurteilung allein auf Grundlage des Remissionsstatus bzw. des Therapieansatzes (kurativ vs. nichtkurativ) an ihre Grenzen. Auch können bei einer solchen Vorgehensweise Besonderheiten der eingesetzten Therapieformen nicht berücksichtigt werden.
Eine differenziertere Beurteilung ist erforderlich, die einerseits den besonderen Aspekten einer Genesungszeit Rechnung trägt, andererseits aber bei der MdE-Einschätzung tatsächlich auf die individuellen gesundheitlichen Folgen des Versicherungsfalles und die daraus entstehenden Einschränkungen auf dem allgemeinen Arbeitsmarkt abstellt.
Bemerkungen zur Begutachtung
Die Therapie der malignen Erkrankungen des blutbildenden und lymphatischen Systems ist vielschichtig. Neben Strahlentherapie und klassischen Chemotherapeutika kommen zunehmend gezielte Therapien wie monoklonale Antikörper, Immunmodulatoren, Zytokine und sog. „small molecule drugs“ wie z. B. Tyrosinkinase-inhibitoren oder Proteasominhibitoren zum Einsatz. Auch wurden die Indikationen zur Durchführung autologer und allogener Blutstammzelltransplantationen bei diesen Erkrankungen in den letzten Jahren ausgeweitet. Zur Beurteilung der MdE und Abschätzung therapieassoziierter Einschränkungen sind deshalb Kenntnisse zu heutigen Therapieformen und deren Nebenwirkungsspektrum beim Gutachter unerlässlich.
Zu berücksichtigen sind beispielsweise
- das Vorliegen einer B-Symptomatik (Fieber > 38 Grad Celsius, Nachtschweiß, Gewichtsverlust > 10 % in den letzten 6 Monaten),
- Folgen von Blutbildveränderungen (Müdigkeit, Atemnot, Blutungsneigung, gehäufte Infekte),
- Organschäden durch die Erkrankung oder die durchgeführte Chemotherapie,
- Folgen einer sekundären Hämochromatose,
- Bestrahlungsfolgen,
- Kortikosteroidfolgen (Katarakt, Osteopenie etc.),
- eine Fatigue-Symptomatik,
- Konzentrations- und Merkfähigkeitsstörungen („Chemobrain“),
- therapieassoziierte Zweittumore (beispielsweise erhöhtes Hautkrebsrisiko),
- die psychische Belastung durch eine Tumorerkrankung, Schmerzen etc.
Dies erklärt, warum spezielle Untersuchungen wie z. B. Untersuchun-gen des Immunstatus (Immunglobuline quantitativ, zellulärer Immunstatus/Lymphozytentypisierung) insbesondere bei berichteter Infektanfälligkeit oder auch die Bestimmung des Eisenhaushalts bei polytransfundierten Versicherten zur Abklärung einer sekundären Hämochromatose sinnvoll sind. Im Einzelfall können Zusatzbegutachtungen z. B. auf neurologisch-psychiatrischem Fachgebiet zur Abklärung einer Polyneuropathie, einer Cancer-related Fatigue oder anderer krankheitsassoziierter psychischer Störungen erforderlich sein.
Eine erste gutachterliche Untersuchung zur Feststellung der Krankheitsfolgen mit individueller Einschätzung der MdE ist etwa 6 Monate nach Abschluss der ersten intensiven Therapie sinnvoll. Hierbei ist eine Erholungsphase berücksichtigt, in der regelhaft mit Beeinträchtigungen durch z. B. Blutbildveränderungen, Leistungsminderung etc. zu rechnen ist. Üblicherweise ist davon auszugehen, dass nach dieser Zeit eine Stabilisierung des Allgemeinzustandes erreicht ist und die dann noch vorliegenden Folgen der Erkrankung/Therapie beurteilt werden können. Bei Versicherten, die eine allogene Blutstammzelltransplantation erhalten haben, ist regelhaft mit einer längeren Erholungsphase zu rechnen, so dass hier eine erste gutachterliche Untersuchung bzw. die individuelle Einschätzung der MdE auf Grundlage der bestehenden Gesundheitsstörungen i. d. R. erst 12 Monate nach Therapieabschluss erfolgen sollte. In speziellen Fällen wie z. B. bei Versicherten mit einer chronischen myeloischen Leukämie (CML) unter Tyrosinkinaseinhibitortherapie ist eine gutachterliche Untersuchung auch unter laufender Therapie sinnvoll, da es sich hier um langfristig angelegte, meist eher nebenwirkungsarme Therapieregime handelt, bei denen die MdE auch unter 100 % liegen kann.
Regelmäßige Nachbegutachtungen sind erforderlich, da Folgen der Therapie wie Organtoxizitäten auch noch nach Jahren auftreten können (z. B. Kardiomyopathie nach Anthrazyklintherapie). Besonders sollte auf Zweittumoren geachtet werden. Es besteht ein erhöhtes Risiko für die Entwicklung von Zweittumoren teils aufgrund der durchgeführten Therapie, teils aufgrund der Erkrankung. So ist beispielsweise das gehäufte Auftreten von Hauttumoren bei Lymphom-patienten gut belegt (Review: Brewer et al. 2014)
Sonderfall: Begutachtung nach Aktenlage
Eine Begutachtung lediglich nach Aktenlage ist sicherlich nicht ideal und sollte daher die Ausnahme und nicht der Regelfall sein, aller-dings lassen die Umstände gelegentlich keine persönliche Untersuchung des Versicherten zu. Bei der Begutachtung nach Aktenlage ist der Gutachter in besonderem Maße auf eine umfangreich recherchierte Akte angewiesen. Neben Informationen zu den arbeits-technischen Ermittlungen mit Expositionsszenario oder Abschätzung der ppm-Benzoljahre, Informationen zu Krankheits-/AU-Zeiten (KV) und Informationen zu arbeitsmedizinischen Vorsorgeuntersuchungen ist hier ein besonderes Augenmerk auf die medi-zinischen Informationen zu richten. So muss die Akte in jedem Fall Kopien der histologischen Untersuchungen enthalten, um das Krankheitsbild richtig zuordnen zu können. Laborbefunde soll-ten soweit zurück reichend wie möglich recherchiert werden. Eine umfassende Darstellung der Krankengeschichte ist erforderlich. Berichte mit standardisierten Angaben zum Allgemeinzustand (WHO/ECOG [0–4], Karnofsky-Index [100–10 %]) sind bei der Begutachtung nach Aktenlage sehr hilfreich, da in den Arzt- und Krankenhausentlassungsberichten die subjektiven Beschwerden des Patienten häufig nur sehr kurz oder ggf. auch gar nicht geschildert werden.
MdE-Tabellen
Die Behandlung und Prognose und die daraus resultierenden MdE-relevanten Einschränkungen sind bei den Krankheitsbildern des blutbildenden und lymphatischen Systems sehr unterschiedlich, so dass eine Gliederung nach den großen Krankheitsgruppen sinnvoll ist. Die Tabellen sind in ihrer Systematik gleich aufgebaut und sollen Hinweise zu den typischen Einschränkungen und deren Bewertung geben. Auf Besonderheiten wird bei den einzelnen Tabellen eingegangen.
Da sich die Therapieformen hinsichtlich ihrer Verträglichkeit und Nebenwirkungen heute stark unterscheiden, ist bei langfristig angelegten Therapieformen eine differenzierte MdE-Beurteilung auch unter laufender Chemo-/Immuntherapie sinnvoll. In den Tabellen sind beispielhaft vergleichsweise nebenwirkungsarme Therapie-formen aufgeführt, die in der Regel keine MdE von 100 % bedingen. Allerdings kann die MdE im Einzelfall, je nach Verträglichkeit, auch bei diesen Therapieformen höher liegen als dort angegeben.
Non-Hodgkin-Lymphome (NHL)
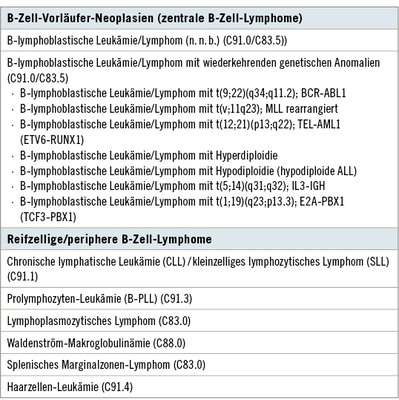
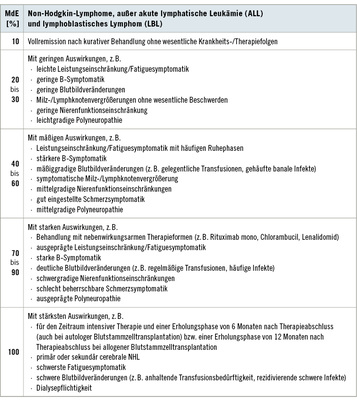
Die Gruppe der Non-Hodgkin-Lymphome umfasst eine Vielzahl von Erkrankungen mit sehr unterschiedlicher Prognose. Auffallend ist die zunehmende Inzidenz dieser Erkrankungen in den letzten Jahrzehnten. In Deutschland schätzt man die Inzidenz auf 10–15/100 000. Das Altersmedian für Non-Hodgkin-Lymphome liegt bei rund 70 Jahren (RKI 2010). Überwiegend handelt es sich um B-Zell-Lymphome. Klassifiziert werden Non-Hodgkin-Lymphome gemäß WHO ( Tabelle 1). Im deutschsprachigen Raum hat sich zusätzlich die Unterscheidung in indolente (niedrigmaligne) und aggressive (hochmaligne) Non-Hodgkin-Lymphome gehalten. Die Gruppe der niedrigmalignen Non-Hodgkin-Lymphome umfasst etwa 70 % aller Non-Hodgkin-Lymphome. Das follikuläre Lymphom ist das häufigste niedrigmaligne Non-Hodgkin-Lymphom. Niedrigmaligne Non-Hodgkin-Lymphome werden meist in fortgeschrittenen Stadien (nach Ann Arbor III oder IV) diagnostiziert und sind dann i. d. R. nicht mehr kurativ behandelbar. Allerdings konnte durch die Etablierung neuer, meist Antikörper-gestützter Therapien eine Verbesserung der Behandlungsmöglichkeiten und Verlängerung der therapiefreien Intervalle und „Chronifizierung“ der Erkrankungen erreicht werden. Aggressive Non-Hodgkin-Lymphome sind rasch verlaufende Erkrankungen, bei denen die intensive Therapie kurativ ausgerichtet ist. Der häufigste Subtyp ist das diffus großzellige B-Zell-Lymphom. In der MdE-Tabelle der Non-Hodgkin-Lymphome ( Tabelle 2) haben wir bewusst auf die Unterscheidung in niedrig- und hochmalige Non-Hodgkin-Lymphome verzichtet, da sich diese Einteilung nicht an der WHO-Klassifikation orientiert.
In der Regel ist bei allen Non-Hodgkin-Lymphomen unabhängig vom Remissionsstatus von leichten Beeinträchtigungen, z. B. durch Infektanfälligkeit, Leistungsminderung oder auch die psychische Belastung durch eine (unheilbare) Krebserkrankung auszugehen, wodurch den Versicherten bestimmte Tätigkeiten (z. B. Tätigkeiten mit Infektionsgefährdung, körperlich schwere Tätigkeiten) verschlossen sind. Dies rechtfertigt die Bewertung mit einer MdE von mindestens 20 %. Bei Versicherten mit kurativ behandeltem Non-Hodgkin-Lymphom ohne gravierende Krankheits- oder Therapiefolgen kann die MdE in Einzelfall auch unter 20 % liegen, wobei hier jedoch regelhaft eine MdE von 10 % anzunehmen ist.
Für den Zeitraum intensiver Therapie (inkl. Hochdosischemo-therapie mit autologer Blutstammzelltransplantation) und einen Zeitraum von 6 Monaten nach Therapieabschluss, i. S. einer Erholungsphase mit noch herabgesetzter Leistungsfähigkeit, Blutbildveränderungen etc., ist eine MdE von 100 % angemessen. Bei Versicherten, die eine allogene Blutstammzelltransplantation erhalten haben, ist eine Erholungsphase von 12 Monaten anzunehmen. Bei weniger intensiven Therapieformen (z. B. Rituximab mono, Chloram-bucil, Lenalidomid) kann je nach Therapieverträglichkeit die MdE zwischen 70 und 100 % liegen. Einen Sonderfall stellen primäre oder sekundäre cerebrale NHL dar, bei denen aufgrund der weiter-hin sehr schlechten Prognose und der meist starken Beeinträchti-gungen in den meisten Fällen eine dauerhafte MdE von 100 % angemessen erscheint.
Myelodysplastische Syndrome und myeloproliferative Neoplasien
Myelodsyplastische Syndrome (MDS)
Myelodysplastische Syndrome sind eine sehr heterogene Gruppe von Erkrankungen, deren Ursprung die hämatopoetische Stammzelle ist. Wurde traditionell die FAB-(French-American-British)-Klassifikation angewandt, so werden diese Erkrankungen heute eben-falls nach WHO klassifiziert. Typischerweise treten die Erkrankungen in höherem Lebens-alter auf mit einem Altersmedian von 70 Jah-ren und einer Inzidenz von 3–5/100 000. Bei den über 70-Jährigen liegt die Inzidenz bei > 20/100 000 (Aul et al. 1992; Germing et al. 2004). Gekennzeichnet sind die Erkrankun-gen durch Zytopenien infolge einer ineffek-tiven Hämatopoese und Dysplasien der my-eloischen Zellreihe mit einem erhöhten Risiko für die Entwicklung einer akuten mye-loischen Leukämie. Die therapeutischen Maßnahmen sind vielfältig und reichen von supportiver Therapie über immunmodulatorische Therapien und klassische Chemo-therapie bis zur allogenen Blutstammzell-transplantation. Zu beachten ist, dass die Vielzahl der Patienten zum Diagnosezeitpunkt bereits transfusionsbedürftig ist und im Krankheitsverlauf zahlreiche Erythrozytenkonzentrate transfundiert werden. Diese Patienten weisen ein hohes Risiko für die Entwicklung einer sekundären Hämochromatose mit Organschäden auf.
Myeloproliferative Neoplasien (MPN)
Bei diesen Krankheitsbildern handelt es sich um klonale Erkrankun-gen der pluripotenten Blutstammzelle. Es können eine, zwei oder auch alle drei Zellreihen betroffen sein. Anfangs findet sich meist ein hyper-zelluläres Knochenmark mit vermehrter Proliferation und Ausreifung der einzelnen Zelllinien. Im weiteren Verlauf kann eine Fibrosierung des Knochenmarks auftreten, die zur Ausbildung einer extra-medullären Blutbildung, oft mit Hepatosplenomegalie, führen kann. Die Inzidenz liegt bei 1–2/100 000, der Altersmedian liegt bei 60 bis 65 Jahren (Titmarsh et al. 2014).
Lange konnte nur die BCR-ABL-positive chronische Leukämie eindeutig diagnostiziert und von den anderen myeloprolifertiven Neoplasien abgegrenzt werden. Mittlerweile sind weitere klonale Marker identifiziert (JAK2-, CALR- und MPL-Mutationen), die die Diagnose dieser Erkrankungen und Abgrenzung zu reaktiven Veränderungen ermöglichen. Allerdings können Polycythaemia vera (PV), essentielle Thrombozythämie (ET) und primäre Myelofibrose (PMF) nur unter Berücksichtigung des klinischen Bildes und teils erst nach längerer Verlaufsbeobachtung differenziert werden. Da alle MPN jedoch Erkrankungen der sog. Gruppe B lt. wissenschaftlicher Begründung zur BK 1318 sind, ist der eindeutige Nachweis einer MPN auch ohne klare Subklassifizierung ausreichend, um zur Kausalzusammenhangsfrage Stellung nehmen zu können.
Während bei der Polycythaemia vera und der essentiellen Thrombozythämie die Vermeidung thromboembolischer Ereignisse z. B. durch Aderlasstherapie (Polycythaemia vera) bzw. Thrombozytenaggregationshemmer und zytoreduktive Therapien im Vordergrund stehen, richtet sich die Therapie der primären Myelofibrose nach den Krankheitsauswirkungen und umfasst zytoreduktive Therapien, supportive Maßnahmen oder auch JAK-Inhibitoren. Allen drei Krank-heitsbildern gemeinsam ist, dass die allogene Blutstammzelltransplantation derzeit der einzige kurative Therapieansatz ist.
Für die BCR-ABL-1-positive chronische myeloische Leukämie steht seit Einführung der Tyrosinkinaseinhibitoren eine spezifische Therapie zur Verfügung. Es können Remissionen auf hämatologischer, zytogenetischer und molekularer Ebene erreicht werden. Auch wenn molekulare Remissionen erreicht wer-den, sind derzeit noch Fragen u. a. zu optimalen Therapieschemata und Therapiedauer bei Patienten mit gutem Ansprechen offen.
Die speziellen Umstände der Therapie mit Tyrosinkinaseinhibitoren spiegeln sich in den Versorgungsmedizinischen Grundsätzen der Versorgungsmedizin-Verordnung mit abgestuften GdS-Sätzen in Abhängig-keit vom Remissionsstatus wider. Im Unfall-versicherungsrecht lässt sich eine Staffelung der MdE nach Remissionsstatus jedoch nicht plausibel machen, es ist auf die tatsächlichen Auswirkungen der Krankheit bzw. der Therapie abzustellen.
Myelodysplastische / myeloproliferative Neoplasien
Hierbei handelt es sich um eine Gruppe von Erkrankungen, die Eigenschaften sowohl der myelodysplastischen Syndrome als auch der myeloproliferativen Neoplasien vereinen. Die Erkrankungen wurden nach älteren Klas-sifikationen teils den myelodysplastischen Syndromen (z. B. CMML), teils den myeloproliferativen Neoplasien (z. B. atypische CML) zugeordnet. Die Behandlungsoptio-nen gleichen denen der myelodysplastischen Syndrome bzw. der myeloproliferativen Neo-plasien ( Tabelle 3).
Akute Leukämien
Es handelt sich um schwere, lebensbedrohliche Krankheitsbilder, die durch eine zunehmende Insuffizienz der Hämatopoese infolge einer blastären Knochenmarkinfiltration gekennzeichnet sind.
Akute Leukämien werden heute gemäß WHO klassifiziert, wobei in dieser Klassifikation zytogenetische, molekulargenetische wie auch morphologische Veränderungen berücksichtigt werden. Es hat sich gezeigt, dass dem Karyotyp der Blasten der wichtigste unabhängige Prognosefaktor zukommt. Gelegentlich finden sich in Arztbriefen zusätzlich Angaben zur Klassifikation nach FAB (French-American-British). In dieser Klassifikation erfolgt die Einteilung nach zytomorphologischen und zytochemischen Charakteristika.
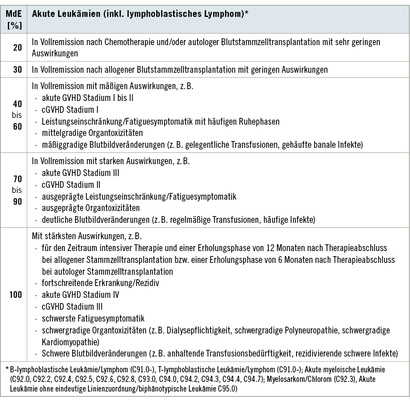
Während die akute myeloische Leukämie (AML) die typische Leukämie des Erwachsenenalters mit einer Inzidenz von 3,7/100 000 und einem medianen Erkrankungsalter von rund 70 Jahren ist (Juliusson et al. 2009), ist die akute lymphatische Leukämie die typische Leukämie des Kindesalters. Bei beiden Erkrankungen finden sich jedoch in höherem Lebensalter zunehmende Erkrankungszahlen. Eine Besonderheit der akuten myeloischen Leukämie ist, dass ihr oft ein myelodysplastisches Syndrom vorangeht. Die Folgen der medikamentösen Therapie der akuten Leukämien sind meist mit denen bei anderen Erkrankungen des blutbildenden und lymphatischen Systems vergleichbar. Zusätzlich bestehen Besonderheiten bedingt durch spezielle Therapieformen wie die allogene Blutstammzell-transplantation. Bei Patienten mit allogener Blutstammzelltransplantation ist insbesondere auf Einschränkungen bedingt durch eine Transplantat-gegen-Wirt-Reaktion (Graft-versus-Host-Disease, GVHD) zu achten. Die akute Form betrifft bis zu 60 % der Patienten nach allogener Blutstammzelltransplantation und ist für 15–30 % der Sterbefälle verantwortlich (Ferrara et al. 2009). Haut, Gastrointestinaltrakt und Leber sind die Hauptmanifestationsorte der akuten GVHD. Nach aktueller Definition der Natio-nal Institutes of Health (NIH) werden die klassische akute GVHD bis Tag 100 nach allogener Blutstammzelltransplantation, die „late-onset“ akute GVHD (nach 100 Tagen) und die persistierende und rekurrierende akute GVHD voneinander differenziert. Vier Schweregrade werden unterschieden (Grad I–IV; leicht, moderat, schwer, lebensbedrohlich) (Przepiorka et al. 1994; Glucksberg et al. 1974).
Die chronische GVHD (cGVHD) tritt bei etwa der Hälfte der Patienten auf und manifestiert sich in der Regel 2 bis 18 Monate nach allogener Blutstammzelltranplantation. Die NIH-Konsensusgruppe hat acht häufig betroffene Organsysteme definiert: Haut, Augen, Mundschleimhaut, Leber, Gastrointestinaltrakt, Genitalien, Lunge so-wie Gelenke und Faszien. Bei der Definition der drei Schweregrade (mild, moderat, schwer) wird die Zahl der betroffenen Organsysteme ebenso wie der Schweregrad der Organmanifestation berücksichtigt (Ja-gasia et al. 2015; Filipovich et al 2005).
Sowohl die Diagnose als auch die Therapie der akuten und chronischen GVHD sind dem behandelnden Zentrum vorbehalten, allerdings ist der Schweregrad einer bestehenden GVHD aufgrund der teils gravierenden Auswirkungen ein wichtiges Kriterium in der MdE-Einschätzung. Aus diesem Grund haben wir die GVHD explizit in die MdE-Tabelle einbezogen.
Bei Patienten, bei denen nach durchgeführter Chemotherapie oder autologer Blutstammzelltransplantation eine komplette Remission der Erkrankung vorliegt ist analog zu den Patienten mit NHL regelhaft eine MdE von mindestens 20 % aufgrund leichter Einschränkungen mit Leistungsminderung etc. anzunehmen. Bei Patienten, die eine allogene Blutstammzelltransplantation erhielten und sich in kompletter Remission der Erkrankung befinden, bestehen regelhaft stärkere Einschränkungen, die eine MdE von mindestens 30 % rechtfertigen ( Tabelle 4).
Fazit
Die hier vorgelegten MdE-Tabellen sollen eine differenziertere Be-urteilung der MdE bei Erkrankungen des blutbildenden und lymphatischen Systems durch Benzol (BK 1318) ermöglichen. Wir hoffen, dass sie als Anhaltspunkte für eine einheitlichere Beurteilung der MdE sowohl den Gutachtern als auch den Unfallversicherungsträgern und Sozialgerichten Hilfestellung leisten können. Zu beachten ist jedoch, dass, auch wenn Besonderheiten einzelner Therapieformen berücksichtigt sind, die individuelle Beurteilung des Versicherten durch einen erfahrenen Gutachter weiterhin die wesentliche Grundlage für die MdE-Einschätzung sein muss.
Literatur
Aul C, Gattermann N, Schneider W: Age-related incidence and other epidemiological aspects of myelodysplastic syndromes. Br J Haematol 1992; 82: 358–367.
Brewer JD, Habermannn T, Shanafelt TD: Lymphoma-associated skin cacer: incidence, natural history, and clinical management. Int J Dermatol 2014; 53: 267–274.
Deutsche Gesetzliche Unfallversicherung (DGUV): Empfehlung für die Begutachtung der Berufskrankheiten der Nummern 1315 (ohne Alveolitis), 4301 und 4302 der Anlage zur Berufskrankheiten-Verordnung (BKV) – Reichenhaller Empfehlung – Berlin November 2012.
Ferrara JL, Levine JE, Reddy P, Holler E: Graft-versus-host disease. Lancet 2009; 373: 1550–1156.
Filipovich AH, Weisdorf D, Pavletic S et al.: National Institutes of Health consensus development project on criteria for clinical trials in chronic graft-versus-host disease: I. Diagnosis and Staging Working Group report. Biol Blood Marrow Transplant 2005; 11: 945–956.
Germing U, Strupp C, Kundgen A, Bowen D, Aul C, Haas R, Gattermann N: No increase in age-specific incidence of myelodysplastic syndromes. Haematologica 2004; 89: 905–910.
Glucksberg H, Storb R, Fefer A, Buckner CD, Neiman PE, Clift RA, Lerner KG, Thomas ED: Clinical manifestations of graft-versus-host disease in humanrecipients of marrow from HL-A-matched sibling donors. Transplantation 1974; 18: 295–304.
Hoffmann J, Bolt HM, Kerzel A, Prager HM, Schiele R, Tannapfel A, Triebig G, Weber: Benzol-verursachte Malignomedes hämatolymphatischen Systems als Berufskrankheit BK 1303. Arbeitsmed Sozialmed Umweltmed 2001; 36: 475–483.
Jagasia MH, Greinix HT, Arora M et al.: National Institutes of Health Consensus Development Project on Criteria for Clinical Trials in Chronic Graft-versus-Host Disease: I. The 2014 Diagnosis and Staging Working Group report. Biol Blood Marrow Transplant. 2015; 21: 389–401.
Juliusson G1, Antunovic P, Derolf A, Lehmann S, Möllgård L, Stockelberg D, Tidefelt U, Wahlin A, Höglund M: Age and acute myeloid leukemia: real world data on decision to treat and outcomes from the Swedish Acute Leukemia Registry. Blood 2009; 113: 4179–4187.
Przepiorka D, Weisdorf D, Martin P, Klingemann HG, Beatty P, Hows J, Thomas ED: 1994 Consensus Conference on Acute GVHD Grading. Bone Marrow Transplant 1995; 15: 825–828.
Robert Koch-Institut (RKI): Krebs in Deutschland 2009/2010. Eine gemeinsame Veröffentlichung des Robert Koch-Instituts und der Gesellschaft der epidemiologischen Krebsregister in Deutschland e. V., 9. Ausgabe. Berlin: RKI, 2013.
Titmarsh GJ, Duncombe AS, McMullin MF, O’Rorke M, Mesa R, De Vocht F, Horan S, Fritschi L, Clarke M, Anderson LA: How common are myeloproliferative neoplasms? A systematic review and meta-analysis. Am J Hematol 2014; 89: 581–587.
Woitowitz HJ, Thielmann HW, Norpoth K, Henschler D, Hallier E: Benzol als Ausnahmekanzerogen in der Prävention und seine genotoxischen Folgen: Toxikologische, arbeitsmedizinische und sozialmedizinische Aspekte. Zbl Arbeitsmed 2003; 53: 126–150.
Danksagung: Wir bedanken uns herzlich bei Herrn Prof. Dr. med. Klaus Golka, Leiter der ZE Klinische Arbeitsmedizin, Leibniz-Institut für Arbeitsforschung an der TU Dortmund für die redaktionelle Unterstützung.
Für die Verfasser
Dr. med. Jana Henry
Am Schmöningsberg 1
45721 Haltern am See
Erratum
In dem Beitrag „Wissenschaftliche Stellungnahme zu der Berufskrankheit Nr. 1104 der Anlage 1 zur Berufskrankheiten-Verordnung ‚Erkrankungen durch Cadmium oder seine Verbindungen’“ (ASU 2014; 49: 771–778) hat sich leider ein Druckfehler eingeschlichen: Anstelle von µg wurde versehentlich mg abgedruckt. Richtigerweise lauten die Konzentrationen µg/m3 (Luft) bzw. µg/g Kreatinin (Urin) oder µg/l (Urin).
Wir bitten den Fehler zu entschuldigen und verweisen auf die korrigierte Version im Internet:
www.asu-arbeitsmedizin.com Heftarchiv 2014 Ausgabe 10/2014
Fußnoten
1 Institut für Arbeits-, Sozial- und Umweltmedizin Castrop-Rauxel